摘要: I.5670L·mol-1(2分.漏掉或写错单位扣1分) Ⅱ.(1)2C2H6(g)+7 O2(g)=4CO2(g)+6H2O (l) △H=-3116.6KJ·mol-1 C2H6+18 OH― → 2CO32― +12H2O+14e- [或C2H6+14 OH― → 2CO2+10H2O+14e-] (3)4 OH― →2 H2O +O2↑+4e-氧化铜 4g [或碳酸铜 6.2g或氧化亚铜7.2g]
网址:http://m.1010jiajiao.com/timu3_id_59366[举报]
(2012?奉贤区二模)苯佐卡因(化学名称:对氨基苯甲酸乙酯,结构简式: 简称:EPABA)是白色粉末,味苦而麻,易溶于乙醇,不溶于水.是局部麻醉药,用于手术后创伤止痛,溃疡痛等.苯佐卡因的合成路线如下:(Na2Cr2O7是一种强氧化剂)
简称:EPABA)是白色粉末,味苦而麻,易溶于乙醇,不溶于水.是局部麻醉药,用于手术后创伤止痛,溃疡痛等.苯佐卡因的合成路线如下:(Na2Cr2O7是一种强氧化剂)
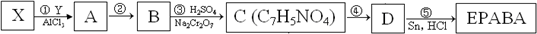
已知:①石油裂解气的某一成分在一定条件下可三聚生成X,A是X的相邻同系物;
②烷基化反应: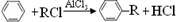 ;
;
③
④酰基化反应: .
.
(1)Y的结构简式:
 .
.
(2)写出有机反应类型:反应③
(3)反应②的另一反应物是
 .
.
(4)写出反应④的化学方程式:
 .
.
(5)检验反应③中的B已完全转化为C的方法是:
(6)甲同学尝试设计合成路线W: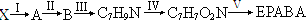 ,却始终没有成功,请分析可能原因:
,却始终没有成功,请分析可能原因:
查看习题详情和答案>>
 简称:EPABA)是白色粉末,味苦而麻,易溶于乙醇,不溶于水.是局部麻醉药,用于手术后创伤止痛,溃疡痛等.苯佐卡因的合成路线如下:(Na2Cr2O7是一种强氧化剂)
简称:EPABA)是白色粉末,味苦而麻,易溶于乙醇,不溶于水.是局部麻醉药,用于手术后创伤止痛,溃疡痛等.苯佐卡因的合成路线如下:(Na2Cr2O7是一种强氧化剂)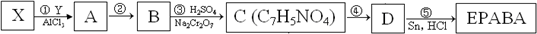
已知:①石油裂解气的某一成分在一定条件下可三聚生成X,A是X的相邻同系物;
②烷基化反应:
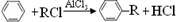 ;
;③

④酰基化反应:
 .
.(1)Y的结构简式:
CH3Cl
CH3Cl
;EPABA有许多同分异构体,其中一种同分异构体G是蛋白质的组成单元之一(含有苯环),且G是人体不能合成的,必须依靠食物摄入,则G的结构简式为

(2)写出有机反应类型:反应③
氧化
氧化
,反应⑤还原
还原
.(3)反应②的另一反应物是
浓硝酸
浓硝酸
,该反应有副产物,写出一种相对分子质量比B大90的副产物的结构简式

(4)写出反应④的化学方程式:


(5)检验反应③中的B已完全转化为C的方法是:
取少量下层液体,滴加1滴酸性高锰酸钾溶液,不褪色
取少量下层液体,滴加1滴酸性高锰酸钾溶液,不褪色
.(6)甲同学尝试设计合成路线W:
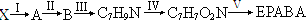 ,却始终没有成功,请分析可能原因:
,却始终没有成功,请分析可能原因:-NH2(氨基)容易被氧化
-NH2(氨基)容易被氧化
,乙同学在甲的合成路线W中插入了两个反应:(a)与乙酸酐(CH3CO)2O反应、(b)与稀硫酸加热回流,于是获得了成功,则反应(b)插入了合成路线W中的第IV
IV
步.(填I、II、III、IV、V) 镁、铝、铁及其化合物在生产和生活中有广泛的应用.
镁、铝、铁及其化合物在生产和生活中有广泛的应用.(1)镁铝合金用在飞机制造业,现有3.90克镁铝合金溶于足量的2mol/L稀硫酸中生成0.2mol氢气,计算并确定镁铝合金中物质的量n(Mg):n(Al)=
1:2
1:2
.(2)硫铁矿的主要成分为FeS2(假设杂质只含SiO2)是生产硫酸的原料.取某硫铁矿10g在足量的空气中煅烧(4FeS2+11O2→2Fe2O3+8SO2),充分反应后冷却,称得固体质量为7.4g(杂质SiO2不反应).该硫铁矿中FeS2的质量分数为
78%
78%
.(3)现有一定量的铁粉和铝粉组成的混合物跟100mL稀硝酸充分反应,反应过程中无任何气体放出,往反应后的澄清溶液中逐渐加入4.00mol?L-1的NaOH溶液,加入NaOH溶液的体积与产生沉淀的质量的关系如图所示(必要时可加热,忽略气体在水中的溶解):纵坐标中A点的数值是
0.856
0.856
(4)炼铁厂生产的生铁常用于炼钢.取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况下).
①计算此钢样粉末中铁和碳的物质的量之比为
50:1
50:1
(最简单的整数比).②再取三份不同质量的上述钢样粉末分别加到100mL相同浓度的稀H2SO4中,充分反应后,测得的实验数据如表所示:
| 实验序号 | I | II | III |
| 加入钢样粉末的质量(g) | 2.812 | 5.624 | 8.436 |
| 生成气体的体积(L)(标准状况) | 1.120 | 2.240 | 2.800 |
1.25mol/L
1.25mol/L
.③若在上述实验II中继续加入m克钢样粉末,计算反应结束后剩余的固体质量为
0<m≤1.406g时,(m+5.624)×
g;
m>1.406g时,(m-1.376)g
| 0.12 |
| 28.12 |
m>1.406g时,(m-1.376)g
0<m≤1.406g时,(m+5.624)×
g;
m>1.406g时,(m-1.376)g
g(保留3位小数)| 0.12 |
| 28.12 |
m>1.406g时,(m-1.376)g
(2009?湖北模拟)如图1所示的转化关系中(部分产物省略),A是由四种短周期元素组成的正盐,H是一种既有氧化性又有还原性的氧化物,D、X分子都是10电子微粒.

试回答下列问题:
(1)A的化学式为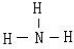
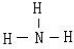 .
.
(2)写出上述转化关系中所有复分解反应的化学方程式:
(3)室温下,向pH=a的D的水溶液中加入等体积pH=b的G的水溶液,且a+b=14,充分反应后溶液中各种离子浓度由大到小的顺序是
(4)已知:t℃时,2H(g)+Y(g)?2I(g);△H=-196.6KJ/mol.
①t℃时,在一压强恒定的密闭容器中,加入4molH和2molY反应,达到平衡后,放出354KJ的热量,则Y的转化率约为
②若在图2的平衡体系中,再加入wmol气态的I物质,t℃时达到新的平衡,此时H物质的物质的量n(H)=
查看习题详情和答案>>

试回答下列问题:
(1)A的化学式为
(NH4)2SO3
(NH4)2SO3
,D分子的结构式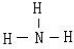
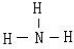
(2)写出上述转化关系中所有复分解反应的化学方程式:
(3)室温下,向pH=a的D的水溶液中加入等体积pH=b的G的水溶液,且a+b=14,充分反应后溶液中各种离子浓度由大到小的顺序是
c(NH4+)>c(NO3-)>c(OH-)>c(H+)
c(NH4+)>c(NO3-)>c(OH-)>c(H+)
.(4)已知:t℃时,2H(g)+Y(g)?2I(g);△H=-196.6KJ/mol.
①t℃时,在一压强恒定的密闭容器中,加入4molH和2molY反应,达到平衡后,放出354KJ的热量,则Y的转化率约为
90%
90%
(用百分数表示).②若在图2的平衡体系中,再加入wmol气态的I物质,t℃时达到新的平衡,此时H物质的物质的量n(H)=
0.4+0.1w
0.4+0.1w
mol.(填表达式)(2011?沈阳二模)化学----化学与技术模块
海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:
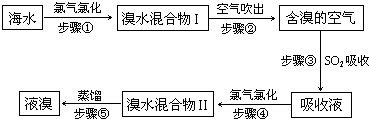
(1)步骤①反应的离子方程式是
(2)步骤③反应的化学方程式是
(3)Br的原子序数是
(4)步骤⑤蒸馏的过程中,温度应控制在80~90℃.温度过高或过低都不利于生产,请解释原因:
(5)为什么不直接用“溴水混合物I”而要用“溴水混合物II”进行蒸馏,得到液溴?
查看习题详情和答案>>
海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:

(1)步骤①反应的离子方程式是
2Br-+Cl2=2Cl-+Br2
2Br-+Cl2=2Cl-+Br2
.(2)步骤③反应的化学方程式是
SO2+Br2+2H2O=2HBr+H2SO4
SO2+Br2+2H2O=2HBr+H2SO4
.(3)Br的原子序数是
35
35
,在周期表中位于4
4
周期ⅤⅡA
ⅤⅡA
族.(4)步骤⑤蒸馏的过程中,温度应控制在80~90℃.温度过高或过低都不利于生产,请解释原因:
温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低
温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低
.(5)为什么不直接用“溴水混合物I”而要用“溴水混合物II”进行蒸馏,得到液溴?
溴水混合物I成分复杂,要获得溴需控制多个温度,操作麻烦
溴水混合物I成分复杂,要获得溴需控制多个温度,操作麻烦
.某同学对第四周期过渡元素产生浓厚的兴趣.想探究是否只有MnO2能催化KClO3受热分解?CuO、Fe2O3、Cr2O3等对氯酸钾的受热分解有没有催化作用?若有催化作用,效率怎样?请你与他一起进行实验探究:
I.课题名称:
Ⅱ.实验仪器:略
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾
Ⅲ.实验步骤:略
Ⅳ.实验数据:
V.实验讨论:
(1)请用编号3的实验数据求得KClO3的分解率:为
(2)在用Cr2O3做实验时,有刺激性气味的气体产生,同时绿色的混合物变成橘黄色(K2Cr2O7).该刺激性气体可能是
A、湿润的蓝色石蕊试纸 B、湿润的碘化钾淀粉试纸
C、湿润的PH试纸 D、湿润的红色石蕊试纸
Ⅵ.实验结论:
查看习题详情和答案>>
I.课题名称:
探究CuO、Fe2O3、Cr2O3等对氯酸钾的受热分解反应的催化作用
探究CuO、Fe2O3、Cr2O3等对氯酸钾的受热分解反应的催化作用
.Ⅱ.实验仪器:略
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾
Ⅲ.实验步骤:略
Ⅳ.实验数据:
| 实验 编号 |
KClO3 (g) |
氧化物 | 产生气体(mL) (已折算为标况) |
耗时(s) | ||
| 化学式 | 质量(g) | 回收 | ||||
| 1 | 0.6 | - | - | - | 10 | 480 |
| 2 | 0.6 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.6 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.6 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.6 | Cr2O3 | 0.20 | 异常 | 67.2 | 188.3 |
(1)请用编号3的实验数据求得KClO3的分解率:为
40.8%
40.8%
%(保留一位小数).(2)在用Cr2O3做实验时,有刺激性气味的气体产生,同时绿色的混合物变成橘黄色(K2Cr2O7).该刺激性气体可能是
Cl2
Cl2
(填化学式),用B
B
检验.(填序号)A、湿润的蓝色石蕊试纸 B、湿润的碘化钾淀粉试纸
C、湿润的PH试纸 D、湿润的红色石蕊试纸
Ⅵ.实验结论:
氯化铁和二氧化锰的催化能力较好
氯化铁和二氧化锰的催化能力较好
.