摘要:2.化学平衡常数K表示可逆反应的进行程度.K值越大.表示 .K值大小与温度的关系是:温度升高.K值 .(填一定增大.一定减小.或可能增大也可能减小). (2)在一体积为10L的容器中.通人一定量的CO和H2O.在850℃时发生如下反应: CO(g)+H2O(g)CO2(g)+H2 CO和H2O浓度变化如右图.则0-4min的平均反应速率v(CO)= mol/ 时.在相同容器中发生上述反应.容器内各物质的浓度变化如右表. ①表中3min-4min之间反应处于 状态, C1数值 0.08mol/L. ②反应在4min-5min问.平衡向逆方向移动.可能的原因是 . 表中5min-6min之间数值发生变化.可能的原因是 . A 增加水蒸气 B 降低温度 C 使用催化剂 D 增加氢气浓度
网址:http://m.1010jiajiao.com/timu3_id_48058[举报]
 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示可逆反应进行的程度越大
可逆反应进行的程度越大
;K值大小与温度的关系是:温度升高,K值可能增大也可能减小
可能增大也可能减小
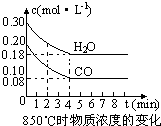
(填“一定增大”、“一定减小”、或“可能增大也可能减小”).(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0 CO和H2O浓度变化如右图,则 0-4min的平均反应速率v(CO)=
0.03mol/(L?min)
0.03mol/(L?min)
,该温度下平衡常数K的数值为1
1
.(3)t1℃(t1>850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如右表.
①表中3min-4min之间反应处于
平衡
平衡
状态; c1数值大于
大于
0.08mol/L (填大于、小于或等于).②反应在4min-5min间,平衡向逆方向移动,可能的原因是
d
d
(单选),表中5min-6min之间数值发生变化,可能的原因是a
a
(单选).a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示(2)一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反
应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g)
根据题意完成下列各题:
①反应达到平衡时,平衡常数
②表达式K=
升高温度,K值
②在500℃,从反应开始到平衡,氢气的平均反应速率v (H2)=
③据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:
 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示可逆反应的进行程度越大
可逆反应的进行程度越大
,K值大小与温度的关系是:温度升高,K值可能增大也可能减小
可能增大也可能减小
.(填一定增大、一定减小、或可能增大也可能减小).(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=
0.03
0.03
mol?L-1?min-1.t℃时物质浓度(mol?L-1)的变化:(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表.
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
平衡
平衡
状态; c 1数值大于
大于
0.08mol?L-1 (填大于、小于或等于).②反应在4min~5min间,平衡向逆方向移动,可能的原因是
d
d
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度.
 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示可逆反应的进行程度越大
可逆反应的进行程度越大
反应进行程度大
反应进行程度大
,K值大小与温度的关系是:温度升高,K值可能增大也可能减小
可能增大也可能减小
(填一定增大、一定减小、或可能增大也可能减小).(2)在一定条件下,二氧化硫和氧气发生如下反应:
2SO2(g)+O2 (g)?2SO3(g)△H<0
①写出该反应的化学平衡常数表达式 K=
| [SO3]2 |
| [SO2]2[O2] |
| [SO3]2 |
| [SO2]2[O2] |
②降低温度,该反应K值
增大
增大
,二氧化硫转化率增大
增大
,化学反应速率 减小
减小
(以上均填增大、减小或不变)③600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间段是
15-20min
15-20min
;25-30min
25-30min
.④据图判断,反应进行至20min时,曲线发生变化的原因是
增加了O2的浓度
增加了O2的浓度
(用文字表达) (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示反应向正向进行的程度越大
反应向正向进行的程度越大
,K值大小与温度的关系是:温度升高,K值可能增大也可能减少
可能增大也可能减少
(填一定增大、一定减小、或可能增大也可能减小).(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.CO和H2O浓度变化如下图所示,则0~4min的平均反应速率v(CO)=
0.03
0.03
mol/(L?min)t1℃时物质浓度(mol/L)的变化
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.006 | 0.266 | 0.104 |
①表中3min~4min之间反应处于
平衡
平衡
状态;C1数值大于
大于
0.08mol/L (填大于、小于或等于).②反应在4min~5min之间,平衡向逆方向移动,可能的原因是
d
d
(单选),表中5min~6min之间数值发生变化,可能的原因是a
a
(单选).a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.