摘要:26.A.B.C.D.E均为有机化合物.它们之间的关系如图所示(提示:RCH=CHR' 在酸性高锰酸钾溶液中反应生成RCOOH和R'COOH.其中R和R'为烷基). 回答下列问题: (1)直链化合物A的相对分子质量小于90.A分子中碳.氢元素的总质量分数为0.814.其余为氧元素.则A的分子式为 , (2)已知B与NaHCO3溶液完全反应.其物质的量之比为1:2.则在浓硫酸的催化下.B与足量的C2H5OH发生反应的化学方程式是 .反应类型为 : (3)A可以与金属钠作用放出氢气.能使溴的四氯化碳溶液褪色.则A的结构简式是 (4)D的同分异构体中.能与NaHCO3溶液反应放出CO2的有 种.其相应的结构简式是 . 答案:(1)C5H10O (2)HOOC-CH2-COOH. HOOC-CH2-COOH + 2C2H5OHC2H5OOC-CH2-COOC2H5 +2H2O, 酯化反应 (3)HO-CH2-CH2-CH=CH-CH3 (4)2,CH3CH2CH2COOH.CH3CH(CH3)COOH
网址:http://m.1010jiajiao.com/timu3_id_47542[举报]
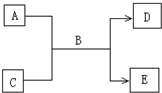 (2009?南充模拟)A、B、C、D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,它们之间有如下的反应关系:
(2009?南充模拟)A、B、C、D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,它们之间有如下的反应关系:(1)常温下,若A为气态单质,C为非金属氧化物,A、C均能使品红溶液褪色,相对分子质量E>D,则:该反应的反应方程式为
Cl2+SO2+2H2O=H2SO4+2HCl
Cl2+SO2+2H2O=H2SO4+2HCl
,检验D中阴离子的方法是先加硝酸酸化无沉淀,再滴加AgNO3溶液有白色沉淀生成,则含Cl-
先加硝酸酸化无沉淀,再滴加AgNO3溶液有白色沉淀生成,则含Cl-
.(2)若A为短周期的金属单质,D为气态单质,C溶液呈强酸性或强碱性时,该反应都能进行.写出反应的离子方程式
2Al+6H+=2Al3++3H2↑
2Al+6H+=2Al3++3H2↑
;2Al+2OH-+H2O=2AlO-+H2↑
2Al+2OH-+H2O=2AlO-+H2↑
.(3)若A、C均为化合物,E为白色沉淀,C为引起温室效应的主要气体,写出E可能的化学式(写两种)
H2SiO3
H2SiO3
、Al ( OH )3
Al ( OH )3
写出生成E的一个离子方程式SiO32-+CO2+H2O=CO32-+H2SiO3↓或 AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
SiO32-+CO2+H2O=CO32-+H2SiO3↓或 AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
.或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
现有六种元素A、B、C、D、E均为周期表中前18号元素,且原子序数依次增大.已知A和B是形成化合物种类最多的两种元素;B元素和C元素通常形成电子数为14或22的化合物.D元素的原子半径是短周期主族元素中最大的;E元素是地壳中含量最高的金属.请回答以下问题:
(1)请画出D的离子结构示意图
 ;由C、A两种元素形成的18电子化合物的电子式为
;由C、A两种元素形成的18电子化合物的电子式为
 ;
;
(2)E的最高价氧化物与D的最高价氧化物的水化物反应的离子方程式:
(3)由以上五种元素两两组合所形成的化合物中,既含有离子键又含有非极性共价键的常见化合物有
查看习题详情和答案>>
(1)请画出D的离子结构示意图




(2)E的最高价氧化物与D的最高价氧化物的水化物反应的离子方程式:
Al2O3+2OH-=2AlO-2+H2O
Al2O3+2OH-=2AlO-2+H2O
;(3)由以上五种元素两两组合所形成的化合物中,既含有离子键又含有非极性共价键的常见化合物有
Na2O2
Na2O2
(填化学式);它的主要用途是供氧剂、漂白剂
供氧剂、漂白剂
,它与水反应的离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑
2Na2O2+2H2O=4Na++4OH-+O2↑
.A、B、C、D、E均为短周期元素,且原子序数逐渐增大.A、D最外层电子数相等且能形成离子化合物,A与B的质子数之和等于C的质子数,A+与 C2-的核外电子数之和等于D+离子的核外电子数,B 原子与 D+离子的核外电子数之和等于 E 原子的核外电子数.
(1)B的元素符号为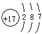
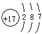 ;由A、C、E三种元素组成的化合物具有漂白性,其电子式为
;由A、C、E三种元素组成的化合物具有漂白性,其电子式为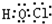
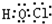 .
.
(2)将少量的D2C2投入到Na2S溶液中,产生浑浊现象,则反应的离子方程式为
(3)A、B、C三种元素可组成多种化合物,请写出两种水溶液呈酸性的化合物,其中甲物质促进水的电离
(4)A与B化合形成10电子化合物丙,A与E化合形成18电子化合物丁;常温下,pH=11的丙溶液与pH=3的丁溶液等体积混合后溶液的pH
(5)A2与C2可构成燃烧电池,若电解质溶液为KOH溶液,该电池的负极反应为
查看习题详情和答案>>
(1)B的元素符号为
N
N
,E的原子结构示意图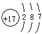
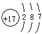
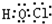
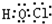
(2)将少量的D2C2投入到Na2S溶液中,产生浑浊现象,则反应的离子方程式为
2H2O+S2-+Na2O2═4OH-+S↓+2Na+
2H2O+S2-+Na2O2═4OH-+S↓+2Na+
.(3)A、B、C三种元素可组成多种化合物,请写出两种水溶液呈酸性的化合物,其中甲物质促进水的电离
NH4NO3
NH4NO3
,物质乙抑制水的电离HNO3
HNO3
;室温下,若两溶液的pH都为4,则两溶液中水电离的氢离子浓度比为:甲:乙=106
106
(4)A与B化合形成10电子化合物丙,A与E化合形成18电子化合物丁;常温下,pH=11的丙溶液与pH=3的丁溶液等体积混合后溶液的pH
>
>
7(填“>”“<”“=”),溶液中离子浓度由大到小的顺序为C(NH4+)>C(Cl-)>C(OH-)>C(H+)
C(NH4+)>C(Cl-)>C(OH-)>C(H+)
.(5)A2与C2可构成燃烧电池,若电解质溶液为KOH溶液,该电池的负极反应为
H2+2e-+2OH-=2H2O
H2+2e-+2OH-=2H2O
.A、B、C、D、E均为可溶于水的固体,组成它们的离子有:
分别取它们的水溶液进行实验,结果如下:
①A溶液与B溶液反应生成白色沉淀和无色气体,沉淀可溶于E溶液;
②A溶液与C溶液反应生成白色沉淀,沉淀可溶于E溶液;
③A溶液与D溶液反应生成白色沉淀,沉淀可溶于盐酸;
④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,
但不消失.
请回答:
(1)写出物质的化学式:B
(2)写出相应的离子方程式:
Ⅰ、A溶液与C溶液反应:
Ⅱ、A溶液与少量E反应:
查看习题详情和答案>>
| 阳离子 | Na+、Mg2+、Al3+、Ba2+ |
| 阴离子 | OH-、Cl-、CO32-、SO42-、HSO4- |
①A溶液与B溶液反应生成白色沉淀和无色气体,沉淀可溶于E溶液;
②A溶液与C溶液反应生成白色沉淀,沉淀可溶于E溶液;
③A溶液与D溶液反应生成白色沉淀,沉淀可溶于盐酸;
④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,
但不消失.
请回答:
(1)写出物质的化学式:B
Al2(SO4)3
Al2(SO4)3
,DBa(OH)2
Ba(OH)2
.(2)写出相应的离子方程式:
Ⅰ、A溶液与C溶液反应:
Mg2++CO32-=MgCO3↓
Mg2++CO32-=MgCO3↓
.Ⅱ、A溶液与少量E反应:
CO32-+H+═HCO3-
CO32-+H+═HCO3-
. 如图是元素周期表的一部分,已知A、B、C、D、E均为短周期元素,D元素最外层电子数为最内层电子数的3倍,下列说法中正确的是( )
如图是元素周期表的一部分,已知A、B、C、D、E均为短周期元素,D元素最外层电子数为最内层电子数的3倍,下列说法中正确的是( )| A、元素A位于第二周期第ⅣA族 | B、原子半径:B>C | C、最高价氧化物对应水化物的酸性:C>E | D、气态氢化物的稳定性:D>B |