网址:http://m.1010jiajiao.com/timu3_id_46179[举报]
某实验小组在进行双氧水分解的实验时发现:大家取不同浓度的双氧水及不同质量的二氧化锰进行的实验,产生气体的速率都不相同,那么过氧化氢分解的最佳催化条件是什么呢?他们决定进行探究。
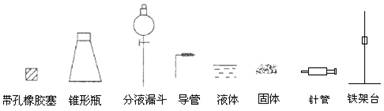
(1)用下列简图,画出实验装置(含试剂)示意图。

(2)小组经过实验,取得如下数据:
|
Z |
0.1 g |
0.3 g |
0.5 g |
|
1.5% |
223 s |
67 s |
56 s |
|
3.0% |
308 s |
109 s |
98 s |
|
4.5% |
395 s |
149 s |
116 s |
(说明:表中X是二氧化锰的质量;Y是指反应停止时的时间;Z是双氧水的质量分数)分析表中数据回答下列问题:
①相同浓度的双氧水的分解速率随着二氧化锰用量的增加而________。
②从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入________g的二氧化锰为较佳选择,理由是
________________________________________________________________________
________________________________________________________________________。
③该小组的小茂同学分析上述数据后得出“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越小,亦即其反应速率越快”的结论,你认为是否正确?________,理由是________________________________________________________________________
________________________________________________________________________。
查看习题详情和答案>>
某实验小组在进行双氧水分解的实验时发现:大家取不同浓度的双氧水及不同质量的二氧化锰进行的实验,产生气体的速率都不相同,那么过氧化氢分解的最佳催化条件是什么呢?他们决定进行探究。
(1)用下列简图,在答题卡的方框中画出实验装置(含试剂)示意图。

(2)小组经过实验,取得如下数据:
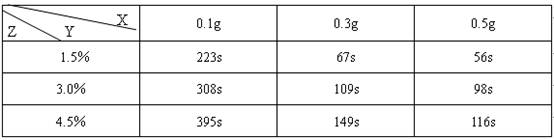
(说明:表中X是二氧化锰的质量;Y是指反应停止时的时间;Z是双氧水的含量)
分析表中数据回答下列问题:
①相同浓度的双氧水的分解速率随着二氧化锰用量的增加而___________。
②从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入______g的二氧化锰为较佳选择,理由是__________________________________________________。
③该小组的小茂同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确_________,理由是__________________________________________________________。
查看习题详情和答案>>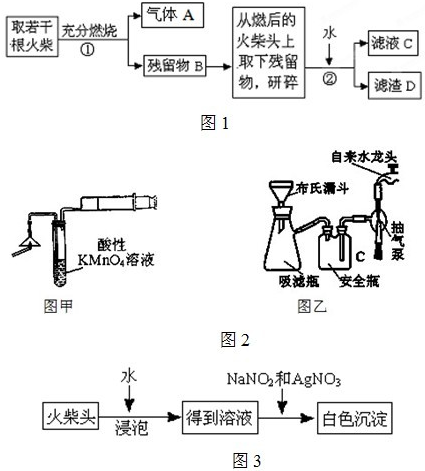
请回答以下问题:
(1)为验证气体A,按图2甲所示进行实验:若能观察到
(2)步骤②的实验操作装置如2乙所示,该操作的名称是
(3)要证明火柴头中含有Cl元素的后续实验步骤是
(4)有学生提出检验火柴头上KClO3另一套实验方案(如图3):有关的离子反应方程式为
(5)该小组猜测滤渣D对双氧水分解制氧气的速率会产生一定的影响,设计并进行了以下5次实验.
| 实验次数 | H2O2溶液质量分数% | H2O2溶液用量/毫升 | 物质D用量/克 | 反应温度/℃ | 收集气体体积/毫升 | 所需时间/秒 |
| ① | 30 | 5 | 0 | 85 | 2 | 3.8 |
| ② | 15 | 2 | 0.1 | 20 | 2 | 2.8 |
| ③ | 15 | 2 | 0.2 | 20 | 2 | 2.2 |
| ④ | 5 | 2 | 0.1 | 20 | 2 | 7.4 |
| ⑤ | 30 | 5 | 0 | 55 | 2 | 10.5 |
(6)写出步骤①中发生反应的化学方程式
| ||
| ||
| ||
| ||
某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S,设计了以下实验流程图:


请回答以下问题:
(1)为验证气体A,按右图所示进行实验:若能观察到 的现象,即可证明火柴头上含有S元素。
(2)写出步骤①中发生反应的化学方程式 。
 (3)步骤②的实验操作装置如右下图所示,该操作的名称是 。
(3)步骤②的实验操作装置如右下图所示,该操作的名称是 。
(4)要证明火柴头中含有Cl元素的后续实验步骤是 。
(5)有学生提出检验火柴头上KClO3另一套实验方案:

|
(6)该小组猜测滤渣D对双氧水分解制氧气的速率会产生一定的影响,设计并进行了以下5次实验。
| 实验次数 | H2O2溶液质量分数% | H2O2溶液用量/毫升 | 物质D用量/克 | 反应温度/℃ | 收集气体体积/毫升 | 所需时间/秒 |
| ① | 30 | 5 | 0 | 85 | 2 | 3.8 |
| ② | 15 | 2 | 0.1 | 20 | 2 | 2.8 |
| ③ | 15 | 2 | 0.2 | 20 | 2 | 2.2 |
| ④ | 5 | 2 | 0.1 | 20 | 2 | 7.4 |
| ⑤ | 30 | 5 | 0 | 55 | 2 | 10.5 |
由上表可知,实验①和⑤能证明温度越高,化学反应速率越快,实验 和
证明物质D的用量越大,反应速率越快。
查看习题详情和答案>>(13分)某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S,设计了以下实验流程图:


请回答以下问题:
(1)为验证气体A,按右图所示进行实验:若能观察到 的现象,即可证明火柴头上含有S元素。
(2)写出步骤①中发生反应的化学方程式 。
(3)步骤②的实验操作装置如右下图所示,该操作的名称是 。
(4)要证明火柴头中含有Cl元素的后续实验步骤是 。
(5)有学生提出检验火柴头上KClO3另一套实验方案:
|
| 实验次数 | H2O2溶液质量分数% | H2O2溶液用量/毫升 | 物质D用量/克 | 反应温度/℃ | 收集气体体积/毫升 | 所需时间/秒 |
| ① | 30 | 5 | 0 | 85 | 2 | 3.8 |
| ② | 15 | 2 | 0.1 | 20 | 2 | 2.8 |
| ③ | 15 | 2 | 0.2 | 20 | 2 | 2.2 |
| ④ | 5 | 2 | 0.1 | 20 | 2 | 7.4 |
| ⑤ | 30 | 5 | 0 | 55 | 2 | 10.5 |
证明物质D的用量越大,反应速率越快。 查看习题详情和答案>>
 X
X Y
Y