题目内容
某实验小组在进行双氧水分解的实验时发现:大家取不同浓度的双氧水及不同质量的二氧化锰进行的实验,产生气体的速率都不相同,那么过氧化氢分解的最佳催化条件是什么呢?他们决定进行探究。
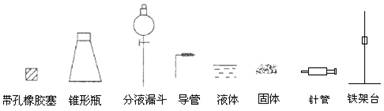
(1)用下列简图,在答题卡的方框中画出实验装置(含试剂)示意图。

(2)小组经过实验,取得如下数据:
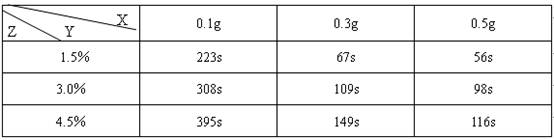
(说明:表中X是二氧化锰的质量;Y是指反应停止时的时间;Z是双氧水的含量)
分析表中数据回答下列问题:
①相同浓度的双氧水的分解速率随着二氧化锰用量的增加而___________。
②从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入______g的二氧化锰为较佳选择,理由是__________________________________________________。
③该小组的小茂同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确_________,理由是__________________________________________________________。
(1)

(2)①加快;
②0.3 ;因为用0.1g的催化剂反应速率明显的小于用0.3g和0.5g的催化剂;用0.5g的催化剂和用0.3g 的催化剂反应速率和反应时间相差不多,但用0.3g的催化剂却节约药品,所以使用0.3g二氧化锰为较佳选择。
③不正确。因为从表中数据可知,相同体积3.0%的双氧水中的溶质含量是1.5%的二倍,但反应的时间却比其反应时间的二倍小得多,由反应速率计算公式(v=△c/△t)可得出,此实验条件下双氧水的浓度越大分解速率越快。

练习册系列答案
相关题目
 I2+O2+H2O
I2+O2+H2O

 I2+O2+H2O可知消耗酸,所以pH升高
I2+O2+H2O可知消耗酸,所以pH升高

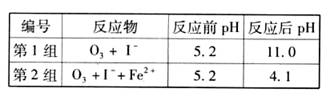
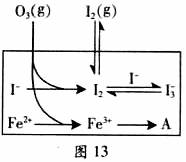 (1)O3将I-氧化成I2的过程由3步反应组成:
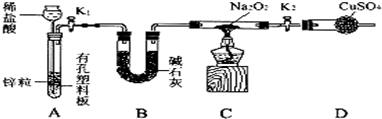
(1)O3将I-氧化成I2的过程由3步反应组成: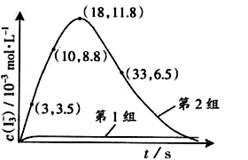 (3) 为探究Fe2+ 对O3氧化I-反应的影响(反应体如图13),某研究小组测定两组实验中I3-浓度和体系pH,结果见图14和下表。
(3) 为探究Fe2+ 对O3氧化I-反应的影响(反应体如图13),某研究小组测定两组实验中I3-浓度和体系pH,结果见图14和下表。