网址:http://m.1010jiajiao.com/timu3_id_46099[举报]
(本小题满分7分)某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了O元素的非金属性比S强的实验研究。回答下列问题:
(1)图中D装置名称是 。
(2) N、C、Si的非金属性由强到弱的顺序是: ;
从以下所给物质中选出甲同学设计的实验所用到物质:
试剂A为_________;试剂C为_________(填序号)。
①稀HNO3溶液②稀盐酸③碳酸钙④Na2SiO3溶液⑤SiO2
(3) 乙同学设计的实验所用到试剂A为________;试剂B为________;试剂C为________。
(本小题满分7分)某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了O元素的非金属性比S强的实验研究。回答下列问题:

(1)图中D装置名称是 。
(2) N、C、Si的非金属性由强到弱的顺序是: ;
从以下所给物质中选出甲同学设计的实验所用到物质:
试剂A为_________;试剂C为_________(填序号)。
①稀HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
(3) 乙同学设计的实验所用到试剂A为________;试剂B为________;试剂C为________。
查看习题详情和答案>>

Ⅰ.检验气密性后关闭弹簧夹I打开弹簧夹Ⅱ,点燃酒精灯,铜丝红热后打开分液漏斗的活塞,A中气体进入B中时不断通入空气,反应一段时间后熄灭酒精灯.
Ⅱ.(1)能证明有氨气产生的现象是


(2)C中铜丝在熄灭酒灯后仍保持红热说明其中反应为
| ||
| △ |
| ||
| △ |
| ||
| △ |
| ||
| △ |
(3)D中产生红棕色气体和白烟,产生白烟的化学方程式为:
(4)F中也产生大量白烟,写出该反应中反应物的物质的量之比n(NH3):n(Cl2)
(5)用化学方程式及相应理论说明A中能产生大量NH3气体的原因
(6)装置中A稍有不足,应该怎样改进
(7)C中铜丝可以与H2O2和H2SO4的混合溶液发生化学反应,已知:
Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)H=64.39KJ?mol-1
2H2O2(l)═2H2O(l)+O2(g)H=-196.46KJ?mol-1
H2(g)+
| 1 |
| 2 |
写出在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式
(1)利用炭粉可以将氮氧化物还原.
已知:N2(g)+O2(g)═2NO(g)△H=+180.6kJ?mol-1
C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1
反应:C(s)+2NO(g)═CO2(g)+N2(g)△H=
(2)TiO2在紫外线照射下会使空气中的某些分子产生活性基团OH,OH能将NO、NO2氧化,如图甲所示,OH与NO2的反应为NO2+OH═HNO3.写出OH与NO反应的化学方程式:
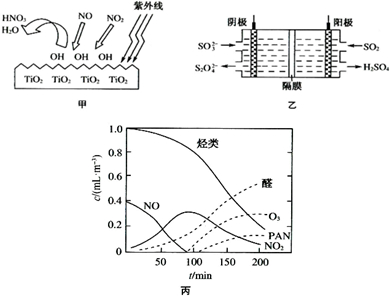
(3)图乙所示的装置能吸收和转化NO2、NO和SO2.
①阳极区的电极反应式为
②阴极排出的溶液中含S2
| O | 2- 4 |
| O | 2- 3 |
| O | 2- 4 |
| O | 2- 4 |
| O | 2- 3 |
③已知阴极生成的吸收液每吸收标准状况下7.84L的气体,阳极区新生成质量分数为49%的硫酸100g,则被吸收气体中NO2和NO的物质的量之比为
(4)O3、醛类、PAN(过氧硝酸乙酰)等污染物气体和颗粒物所形成的烟雾称为光化学烟雾.某研究性学习小组为模拟光化学烟雾的形成,用紫外线照射装在密闭容器内的被污染空气样品,所得物质的浓度随时间的变化如图丙所示.请你根据光化学烟雾的形成原理,对减少光化学烟雾的发生提出一个合理建议:
硫及其化合物有广泛的应用,对SO2性质的研究是高中化学教学的一项重要内容。
I.对比研究是一种重要的研究方法。若将硫的单质及部分化合物按如下表所示分成3 组,则第2组中物质M的化学式是 。
|
第1组 |
第2组 |
第3组 |
|
S (单质) |
SO2、H2SO3、M、NaHSO3 |
SO3、H2SO4、Na2SO4、 NaHSO4 |
Ⅱ.某校化学学习小组用下图所示的实验装置研究SO2气体还原Fe3+、Br2的反应。

(1)下列实验方案可以用于在实验室制取所需SO2的是 。
A.Na2SO3溶液与HNO3 B.Na2SO3固体浓硫酸
C.固体硫在纯氧中燃烧 D.铜与热的浓硫酸
(2)装置C的作用是除去多余的SO2,防止污染空气。已知在用氢氧化钠溶液吸收SO2的 过程中,往往得到Na2SO3和NaHSO3的混合溶液,常温下,溶液pH随n(SO32—):n(HSO3—)变化关系如下表
|
n(SO32—):n(HSO3—) |
91:9 |
1:1 |
9:91 |
|
pH |
8.2 |
7.2 |
6.2 |
当吸收液中n(SO32—):n(HSO3—) =10:1时,溶液中离子浓度关系正确的是 。
A.c(Na+)+ c(H+)= 2c(SO32—)+ c(HSO3—)+ c(OH—)
B.c(Na+)>c(HSO3—)>c(SO32—)>c(OH—)>c(H+)
C.c(Na+)>c(SO32—)>c(HSO3—)>c(OH—)>c(H+)
(3)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中反应后的溶液分成三份,并设计了如下探究实验,请你评价并参与他们的探究过程(限选试剂:KMnO4溶液、KSCN溶液、BaCl2溶液、稀硫酸、稀盐酸、稀硝 酸、Ba(NO3)2溶液、新制的氯水)
|
序号 |
实验方案 |
实验现象 |
结论 |
|
方案① |
往第一份试液中加入KMnO4溶液溶液 |
紫红色褪去 |
SO2与Fe3+反应生成了Fe2+ |
|
方案② |
往第二份试液中加入 |
|
SO2与Fe3+反应生成了Fe2+ |
|
方案③ |
往第二份试液中加入 |
|
SO2与Fe3+反应生成了SO42— |
上述方案①得出的结论是否合理 ,原因 。
如果他们设计的方案②与方案③均合理并且得到相应结论,请你将上面表格补充完整。
(4)装置B中能表明Br—的还原性弱于SO2的现象是 。
查看习题详情和答案>>