摘要:11.已知: H2(g)+ 1/2O2(g)=H2O(l) ΔH = -285.8 kJ·mol-1 CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) ΔH = -890.3 kJ·mol-1 现有H2和CH4的混合气体112 L.使其完全燃烧生成CO2(g)和H2O(l).共放出热量3242.5 kJ.则原混合气体中H2合CH4的物质的量之比是 A.1∶1 B.1∶3 C.1∶4 D.2∶3
网址:http://m.1010jiajiao.com/timu3_id_420521[举报]
已知:H2(g)+1/2O2(g)==H2O(l) ΔH=-285.8 kJ·mol-1 CH4(g)+2O2(g)==CO2(g)+2H2O(l) ΔH=-890kJ·mol-1 现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比为
[ ]
A.1∶1
B.2∶3
C.1∶4
D.1∶3
查看习题详情和答案>>
B.2∶3
C.1∶4
D.1∶3
(1)已知:H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
H2(g)=H2(l) ΔH=-0.92 kJ·mol-1
O2(g)=O2(l) ΔH=-6.84 kJ·mol-1
H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
请写出液氢和液氧反应生成气态水的热化学方程式:__________________________
电解质溶液为KOH溶液的氢氧燃料电池,其负极的电极反应式为____________________________________。
(2)如图表示373 K时,反应A(g)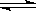 2B(g)在前110 s内的反应进程。
2B(g)在前110 s内的反应进程。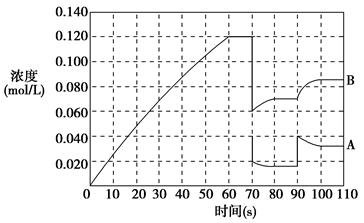
①此反应的平衡常数表达式K=________。
②373 K时反应进行到70 s时,改变的条件可能是________,反应进行到90 s时,改变的条件可能是________。
| A.加入催化剂 | B.扩大容器体积 | C.升高温度 | D.增大A的浓度 |
(1)已知:H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
H2(g)=H2(l) ΔH=-0.92 kJ·mol-1
O2(g)=O2(l) ΔH=-6.84 kJ·mol-1
H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
请写出液氢和液氧反应生成气态水的热化学方程式:__________________________
电解质溶液为KOH溶液的氢氧燃料电池,其负极的电极反应式为____________________________________。
(2)如图表示373 K时,反应A(g) 2B(g)在前110 s内的反应进程。
2B(g)在前110 s内的反应进程。

①此反应的平衡常数表达式K=________。
②373 K时反应进行到70 s时,改变的条件可能是________,反应进行到90 s时,改变的条件可能是________。
③请在图中画出反应物A在0~70 s时的浓度变化曲线。
H2(g)=H2(l) ΔH=-0.92 kJ·mol-1
O2(g)=O2(l) ΔH=-6.84 kJ·mol-1
H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
请写出液氢和液氧反应生成气态水的热化学方程式:__________________________
电解质溶液为KOH溶液的氢氧燃料电池,其负极的电极反应式为____________________________________。
(2)如图表示373 K时,反应A(g)
 2B(g)在前110 s内的反应进程。
2B(g)在前110 s内的反应进程。
①此反应的平衡常数表达式K=________。
②373 K时反应进行到70 s时,改变的条件可能是________,反应进行到90 s时,改变的条件可能是________。
| A.加入催化剂 | B.扩大容器体积 | C.升高温度 | D.增大A的浓度 |
|
已知:H2(g)+O2(g)=H2O(l);ΔH=-285.8 kJ·mol-1 CH4(g)+2O2(g)=CO2(g)+2H2O(l);ΔH=-890 kJ·mol-1 现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695 kJ,则原混合气体中H2与CH4的物质的量之比是 | |
| [ ] | |
A. |
1∶1 |
B. |
2∶3 |
C. |
1∶4 |
D. |
1∶3 |