摘要:15.在一个2.0L密闭容器中.把2.0mol气体X和2.0mol气体Y相混合.在一定条件下发生了下列可逆反应:3X xQ 当反应达平衡时.生成0.8molR.并测得Q的浓度为0.4mol/L.下列叙述中正确的是 A.x的值为3 B.Y的平衡浓度为0.2mol/L C.X的转化率为60% D.X的平衡浓度为0.6mol/L
网址:http://m.1010jiajiao.com/timu3_id_408155[举报]
低碳经济是以低能耗、低污染、低排放为基础的经济模式,低碳循环正成为科学家研究的主要课题.
Ⅰ.最近有科学家提出构想:把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇.该构想技术流程如下:
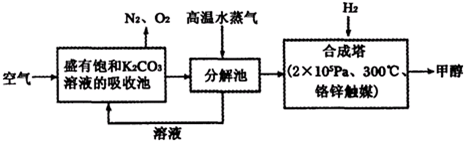
(1)向分解池中通入高温水蒸气的作用是 .
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
③H2O(g)=H2O(1)△H=-44.0kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 .
Ⅱ.一氧化碳与氢气也可以合成甲醇,反应为CO(g)+2H2(g)?CH3OH(g)△H<0.
(1)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应达到平衡,测得c(H2)=2.2mol?L-1,则CO的转化率为 .
(2)T1℃时,此反应的平衡常数为K(T1)=50.此温度下,在一个2L的密闭容器中加入一定量CO和H2,反应到某时刻测得各组分的浓度如下:
①比较此时正、逆反应速率的大小:v正 v逆值(填“>”、“<”或“=”).
②若其他条件不变时,只改变反应的某一个条件,下列说法正确的是 .
A.若达到新平衡时c(CO)=0.3mol/L,平衡一定逆向移动
B.若将容器体积缩小到原来的一半,达到新平衡时,0.2mol/L<c(CO)<0.4mol/L
C.若向容器中同时加入0.4mol CO和0.8mol CH3OH(g),平衡不移动
D.若升高温度,平衡常数将增大
Ⅲ.CO2和SO2的处理是许多科学家都在着力研究的重点.有学者想以如图所示装置用燃料电池原理将CO2、SO2转化为重要的化工原料.
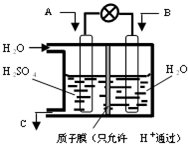
(1)若A为CO2,B为H2,C为CH3OH,电池总反应式为CO2+3H2=CH3OH+H2O,则正极反应式为 .
(2)若A为SO2,B为O2,C为H2SO4,则负极反应式为 .
查看习题详情和答案>>
Ⅰ.最近有科学家提出构想:把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇.该构想技术流程如下:

(1)向分解池中通入高温水蒸气的作用是
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
③H2O(g)=H2O(1)△H=-44.0kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
Ⅱ.一氧化碳与氢气也可以合成甲醇,反应为CO(g)+2H2(g)?CH3OH(g)△H<0.
(1)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应达到平衡,测得c(H2)=2.2mol?L-1,则CO的转化率为
(2)T1℃时,此反应的平衡常数为K(T1)=50.此温度下,在一个2L的密闭容器中加入一定量CO和H2,反应到某时刻测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度/(mol?L-1) | 0.2 | 0.2 | 0.4 |
②若其他条件不变时,只改变反应的某一个条件,下列说法正确的是
A.若达到新平衡时c(CO)=0.3mol/L,平衡一定逆向移动
B.若将容器体积缩小到原来的一半,达到新平衡时,0.2mol/L<c(CO)<0.4mol/L
C.若向容器中同时加入0.4mol CO和0.8mol CH3OH(g),平衡不移动
D.若升高温度,平衡常数将增大
Ⅲ.CO2和SO2的处理是许多科学家都在着力研究的重点.有学者想以如图所示装置用燃料电池原理将CO2、SO2转化为重要的化工原料.

(1)若A为CO2,B为H2,C为CH3OH,电池总反应式为CO2+3H2=CH3OH+H2O,则正极反应式为
(2)若A为SO2,B为O2,C为H2SO4,则负极反应式为
 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:(1)该反应的化学方程式为
3X+Y  2Z
2Z
 2Z
2Z3X+Y  2Z
2Z
; 2Z
2Z(2)从开始至2min,Z的平均反应速率为
0.05mol/(L?min)
0.05mol/(L?min)
;Y的平均反应速率为0.025mol/(L?min)
0.025mol/(L?min)
. 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线,如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线,如图所示.根据图中数据,试填写下列空白:(1)该反应的化学方程式为
Y+3X  2Z
2Z
 2Z
2ZY+3X  2Z
2Z
 2Z
2Z(2)反应开始至2min,气体Z的平均反应速率为
0.05mol/(L.min)
0.05mol/(L.min)
(3)若X、Y、Z均为气体,反应达平衡时,此时容器内的压强与起始压强之比为
9:10
9:10
.(2009?海口模拟)在一个2L的密闭容器中,加入3mol A 和1mol B,发生下述反应:
3A(g)+B(g)?2C(g)+3D(s),5min达到平衡时,C的浓度为0.6mol/L.
(1)达到平衡时,A的转化率为
(2)维持容器的温度不变,若缩小容器的体积,则平衡将
(3)维持容器的体积和温度不变,向密闭容器中加入氦气,达到新平衡时B、C的浓度之比c(B)/c(C)将
(4)若增加A的浓度,B的转化率
查看习题详情和答案>>
3A(g)+B(g)?2C(g)+3D(s),5min达到平衡时,C的浓度为0.6mol/L.
(1)达到平衡时,A的转化率为
60%
60%
.此温度下的平衡常数K=8.33(L/mol)2
8.33(L/mol)2
.(2)维持容器的温度不变,若缩小容器的体积,则平衡将
正反应方向移动
正反应方向移动
. (填“正反应方向移动”、“逆反应方向移动”或“不移动”)(3)维持容器的体积和温度不变,向密闭容器中加入氦气,达到新平衡时B、C的浓度之比c(B)/c(C)将
不变
不变
.(填“增大”、“减小”或“不变”)(4)若增加A的浓度,B的转化率
增大
增大
;若将C分离出来,化学平衡常数不变
不变
.(填“增大”、“减小”、“不变”)在一个1L的密闭容器中,加入2mol A和1mol B,发生下列反应:2A(g)+B(g)?3C(g)+D(s),达到平衡时,C的浓度为1.2mol?L-1.
(1)维持容器的温度不变,若缩小容器的体积,则平衡
(2)维持容器的体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍是1.2mol?L-1的是
A.4mol A+2mol B B.3mol C+1mol D C.2mol A+1mol B+1mol D
(3)若维持容器的体积和温度不变,反应从逆反应开始,按不同配比作为起始物质,达到平衡时,C的浓度仍是1.2mol?L-1,则C的起始物质的量应满足的条件是
查看习题详情和答案>>
(1)维持容器的温度不变,若缩小容器的体积,则平衡
不
不
移动(填“向正反应方向”、“向逆反应方向”或“不”).(2)维持容器的体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍是1.2mol?L-1的是
BC
BC
.A.4mol A+2mol B B.3mol C+1mol D C.2mol A+1mol B+1mol D
(3)若维持容器的体积和温度不变,反应从逆反应开始,按不同配比作为起始物质,达到平衡时,C的浓度仍是1.2mol?L-1,则C的起始物质的量应满足的条件是
1.2mol<nc≤3mol
1.2mol<nc≤3mol
.