摘要:A.B.C属于周期表前4周期的元素.它们的原子序数依次增大.A.B属于同一周期.A.C是生活中常见的金属元素.C的原子序数是A的2倍.B的单质常温下为黄色粉末. (1)C在周期表中位于 周期 族. (2)在加热条件下B单质与C单质反应的化学方程式是 . (3)A的氧化物是某矿物的主要成分.由该矿物提取A元素的第一步是用NaOH溶液处理矿物.使A元素变为可溶性盐.该反应的离子方程式是 . (4)B与C形成的化合物CB2.在有水存在的条件下用氧气氧化该化合物.得到强酸性溶液.低温下 从该强酸性溶液中还可结晶出浅绿色的C的低价盐.该氧化还原反应的化学方程式是 .
网址:http://m.1010jiajiao.com/timu3_id_396770[举报]
A、B、C属于周期表前4周期的元素,它们的原子序数依次增大。A、B属于同一周期,A、C是生活中常见的金属元素。C的原子序数是A的2倍,B的单质常温下为黄色粉末。
(1)C在周期表中位于___________周期____________族。
(2)在加热条件下B单质与C单质反应的化学方程式是_____________。
(3)A的氧化物是某矿物的主要成分,由该矿物提取A元素的第一步是用NaOH溶液处理矿物,使A元素变为可溶性盐,该反应的离子方程式是_____________。
(4)B与C形成的化合物CB2,在有水存在的条件下用氧气氧化该化合物,得到强酸性溶液,低温下从该强酸性溶液中还可结晶出浅绿色的C的低价盐,该氧化还原反应的化学方程式是_______________。
查看习题详情和答案>>
(1)C在周期表中位于___________周期____________族。
(2)在加热条件下B单质与C单质反应的化学方程式是_____________。
(3)A的氧化物是某矿物的主要成分,由该矿物提取A元素的第一步是用NaOH溶液处理矿物,使A元素变为可溶性盐,该反应的离子方程式是_____________。
(4)B与C形成的化合物CB2,在有水存在的条件下用氧气氧化该化合物,得到强酸性溶液,低温下从该强酸性溶液中还可结晶出浅绿色的C的低价盐,该氧化还原反应的化学方程式是_______________。
A、B、C、D、E、F均为周期表中前四周期元素,其原子序数依次增大,其中A、B、C为短周期非金属元素.A是形成化合物种类最多的元素;B原子基态电子排布中只有一个未成对电子;C是同周期元素中原子半径最小的元素.D的基态原子在前四周期元素的基态原子中单电子数最多;E 与D相邻,E的某种氧化物X与C的氢化物的浓溶液加热时反应常用于实验室制取气态单质C;F与D的最外层电子数相等.回答下列问题(相关回答均用元素符号表示):
(1)D的基态原子的核外电子排布式是 .
(2)B的氢化物的沸点比C氢化物的沸点 (填“高”或“低”),原因是 .
(3)A的电负性 C的电负性(填“大于”或“小于”),A形成的氢化物A2H4中A的杂化类型是 .
(4)X在制取C单质中的作用是 ,C的某种含氧酸盐常用于实验室中制取氧气,此酸根离子中化学键的键角 109°28′(填“>”、“=”或“<”).
(5)已知F与C的某种化合物的晶胞结构如图所示,则该化合物的化学式是 ,若F与C原子最近的距离为a cm,则该晶体的密度为 g?cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数的数值为NA ).
查看习题详情和答案>>
(1)D的基态原子的核外电子排布式是
(2)B的氢化物的沸点比C氢化物的沸点
(3)A的电负性
(4)X在制取C单质中的作用是

(5)已知F与C的某种化合物的晶胞结构如图所示,则该化合物的化学式是
A、B、C、D、E五种元素都是前36号元素,原子序数依次增大,其相关信息如下表:
(1)写出上述一种元素与氢元素形成的X2Y2型非极性分子的结构式:
(2)写出E元素的元素符号: ,其价电子排布图为:
(3)A与D形成化合物的化学式为 ,是 分子(填“极性”或“非极性”)
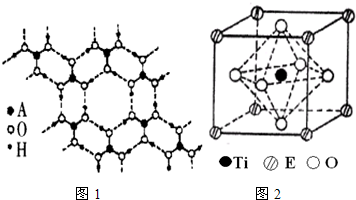
(4)A的最高价氧化物的水化物(H3AO3)是一种白色片层结构的晶体,层内的H3AO3分子间有序排列如
图1所示.在H3AO3晶体中层内分子之间的作用力是 ,该晶体属于 晶体.
(5)在ETiO3晶胞中(结构如图2所示),1个Ti原子和1个E原子周围距离最近的O原子数目分别为 个、 个.
(6)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3-.N3-的空间构型为 ,叠氮化物能与E3+形成配合物,则[E(N3)(NH3)5]SO4中配体是 ,E的配位数是 .
查看习题详情和答案>>
| 元素 | 相关信息 |
| A | A的第一电离能低于同周期左右相邻元素 |
| B | B原子中成对电子数等于未成对电子数的2倍 |
| C | C原子p轨道和s轨道中的电子数相等,与非金属的原子结合时形成共价键 |
| D | D与A、B、C均不同周期,其一个单质分子中只有一个σ键 |
| E | E的原子序数比所处周期中未成对电子数最多的元素大3 |
(2)写出E元素的元素符号:
(3)A与D形成化合物的化学式为

(4)A的最高价氧化物的水化物(H3AO3)是一种白色片层结构的晶体,层内的H3AO3分子间有序排列如
图1所示.在H3AO3晶体中层内分子之间的作用力是
(5)在ETiO3晶胞中(结构如图2所示),1个Ti原子和1个E原子周围距离最近的O原子数目分别为
(6)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3-.N3-的空间构型为
A、B、C、D、E、F周表前四周期中的常见元素,其相关信息如下表:
(1)F位于元素周期表中位置 ,其基态原子核外价电子排布式为 ;
(2)B的电负性比M的 (填“大”或“小”);B2H4分子中σ键与π键与个数之比为 ;
(3)写出E的单质与D的最高价氧化物的水化物溶液反应的化学方程式: ;
(4)已知每5.4gE可与最低价F的氧化物反应,放出346.2kJ的热量.则请写出该反应的热化学方程式: .
查看习题详情和答案>>
| 元素 | 相关信息 |
| A | A是周期表中原子半径最小的元素 |
| B | B元素的原子价电子排布为ns1np4 |
| C | C的基态原子L层电子数是K层电子数的3倍 |
| D | D是第三周期中第一电离能最小的元素 |
| E | E是地壳中含量最多的金属元素 |
| F | 有多种化合价,其某种高价阳离子的价电子具有较稳定的半充满结构 |
(2)B的电负性比M的
(3)写出E的单质与D的最高价氧化物的水化物溶液反应的化学方程式:
(4)已知每5.4gE可与最低价F的氧化物反应,放出346.2kJ的热量.则请写出该反应的热化学方程式:
 A、B、C是由元素周期表中前18号元素中的3种元素形成的单质,甲、乙是常见的化合物.它们之间存在如图所示关系.
A、B、C是由元素周期表中前18号元素中的3种元素形成的单质,甲、乙是常见的化合物.它们之间存在如图所示关系.