摘要:21.对于2SO2(g)+O2(g) 2SO3(g) △H<0反应来说: (1)若将2mol SO2气体和1mol O2气体在2L容器中混合并在一定条件下发生反应.经2min建立平衡.此时测得SO3浓度为0.8mol·L-1.则 ①平衡时.SO2的转化率为 ②从开始至2min用氧气表示的平均速率为v(O2)= ③该条件时反应的平衡常数K= .在体积不变的条件下.改变下列条件重新达到平衡时能使平衡常数K增大的有 A.升高温度 B.降低温度 C.增大压强 D.减小压强 E.加入催化剂 G.移出氧气 (2)一定温度下.若将8mol SO2气体和4mol O2气体混合置于体积可变.压强恒定的密闭容器中.经t1时间达到平衡.测得混合气体的总物质的量为10mol. 试回答下列问题: ①若在t1时充入一定量的氦气.SO3的物质的量将 . 简要说明原因 . ②若在t1时保持温度和压强不变.使SO2.O2.SO3三种气体均增加1mol.则平衡(填“向左移动 .“向右移动 或“不移动 ) . ③若其它条件不变.在t1时再在容器中加入4mol SO2.2mol O2.4mol SO3气体.在下图中做出O→t1→t2点这段时间内SO2的物质的量变化曲线.
网址:http://m.1010jiajiao.com/timu3_id_389977[举报]
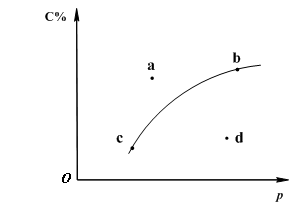
对于可逆反应2A(?)+B(g)![]() 2C(g);下图是其它条件一定时反应中C的百分含量与压强的关系曲线。回答下列问题:
2C(g);下图是其它条件一定时反应中C的百分含量与压强的关系曲线。回答下列问题:
(1)物质A的状态是 (填“气体”、“液体”或“固体”);
(2)图-1中a、b、c、d四点中表示未达到平衡状态且v正<v逆 的点是 ;
(3)在a、b、c三种条件下达平衡时,v(a)、v(b)、v(c)按由大到小排序___________;
 |
|
(4)对于2SO2(g)+O2(g)![]() 2SO3(g);ΔH=-198 kJ/mol。在实际生产过程中,原料气中SO2为7%(体积分数)、O2为11%,常压下进行,控制温度在450℃左右。
2SO3(g);ΔH=-198 kJ/mol。在实际生产过程中,原料气中SO2为7%(体积分数)、O2为11%,常压下进行,控制温度在450℃左右。
请问原料气中SO2与O2的体积比不是2∶1,而要7∶11(大约2∶3)的原因是
;如果在恒容容器中,仅把另外82%的其他气体“抽出来”,是否会减小SO2的转化率 (填“会”或“不会”)。
查看习题详情和答案>>化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种,且均符合勒夏特列原理.请回答下列问题:
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g)?4C(g)△H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)=4mol/L.试确定B的起始浓度c(B)的取值范围是
①增加C的物质的量②加压 ③升温④使用催化剂
(2)反应C(s)+CO2(g)?2CO(g)平衡常数K的表达式为
;
已知C(s)+H20(g)?CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)?C0(g)+H20(g)的平衡常数为K2,则K与K1、K2二者的关系为
(3)已知某温度下,反应2SO2+02?2S03的平衡常数K=19.在该温度下的体积固定的密闭容器中,c0(SO2)=1mol?L-1c0(O2)=1mol?L-1,当反应在该温度下SO2转化率为80%时,该反应
(4)对于可逆反应:aA(g)+bB(g)?cC(g)+dD(g)△H=xkJ?mol-1;若a+b>c+d,增大压强平衡向
查看习题详情和答案>>
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g)?4C(g)△H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)=4mol/L.试确定B的起始浓度c(B)的取值范围是
3mol/L<c(B)<9mol/L
3mol/L<c(B)<9mol/L
;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是①③
①③
.①增加C的物质的量②加压 ③升温④使用催化剂
(2)反应C(s)+CO2(g)?2CO(g)平衡常数K的表达式为
| c2(CO) |
| c(CO2) |
| c2(CO) |
| c(CO2) |
已知C(s)+H20(g)?CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)?C0(g)+H20(g)的平衡常数为K2,则K与K1、K2二者的关系为
K=K1×K2
K=K1×K2
.(3)已知某温度下,反应2SO2+02?2S03的平衡常数K=19.在该温度下的体积固定的密闭容器中,c0(SO2)=1mol?L-1c0(O2)=1mol?L-1,当反应在该温度下SO2转化率为80%时,该反应
否
否
(填“是”或“否”)达到化学平衡状态,若未达到,向逆反应
逆反应
(填“正反应”或“逆反应”)方向进行.(4)对于可逆反应:aA(g)+bB(g)?cC(g)+dD(g)△H=xkJ?mol-1;若a+b>c+d,增大压强平衡向
正反应
正反应
(填“正反应”或“逆反应”)方向移动;若升高温度,平衡向逆反应方向移动,则x<
<
0(填“>”或“<”).对于2SO2(g)+O2(g)?2SO3(g)△H<0 反应来说:
(1)若将2mol SO2气体和1mol O2气体在2L容器中混合并在一定条件下发生反应,经2min建立平衡,此时测得SO3浓度为0.8mol?L-1,则从开始至2min用氧气表示的平均速率v(O2)=
(2)在体积不变的条件下,改变下列条件重新达到平衡时能使平衡常数K增大的有
A.升高温度B.降低温度C.增大压强 D.移出生成的SO3
(3)一定温度下,若将8mol SO2气体和4mol O2气体混合置于体积恒定的密闭容器中,能说明该反应已达到平衡状态的是
A.SO2的转化率和O2的转化率相等 B.容器内压强保持不变
C.v(SO2)逆=2v(O2)正 D.容器内密度保持不变
(4)一定温度下,将8mol SO2和4mol O2气体混合置于体积不变的密闭容器中,经t1时间达到平衡,测得混合气体总物质的量为10mol.若此时向容器中充入一定量的氦气,SO3(g)的物质的量将
查看习题详情和答案>>
(1)若将2mol SO2气体和1mol O2气体在2L容器中混合并在一定条件下发生反应,经2min建立平衡,此时测得SO3浓度为0.8mol?L-1,则从开始至2min用氧气表示的平均速率v(O2)=
0.2mol?L-1?min-1
0.2mol?L-1?min-1
;该条件时反应的平衡常数K=160
160
.(2)在体积不变的条件下,改变下列条件重新达到平衡时能使平衡常数K增大的有
B
B
(填字母).A.升高温度B.降低温度C.增大压强 D.移出生成的SO3
(3)一定温度下,若将8mol SO2气体和4mol O2气体混合置于体积恒定的密闭容器中,能说明该反应已达到平衡状态的是
BC
BC
.A.SO2的转化率和O2的转化率相等 B.容器内压强保持不变
C.v(SO2)逆=2v(O2)正 D.容器内密度保持不变
(4)一定温度下,将8mol SO2和4mol O2气体混合置于体积不变的密闭容器中,经t1时间达到平衡,测得混合气体总物质的量为10mol.若此时向容器中充入一定量的氦气,SO3(g)的物质的量将
不变
不变
(填“增大”、“减小”或“不变”);若使SO2、O2、SO3三种气体均增加1mol,则平衡向右移动
向右移动
(填“向左移动”、“向右移动”或“不移动”).某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.
(1)体系中发生反应的化学方程式是
(2)列式计算该反应在0~3min时间内产物Z的平均反应速率:
(3)该反应达到平衡时反应物X的转化率α等于
(4)对于上述反应在维持其他条件不变的情况下只改变一种实验条件(温度、压强、催化剂)得到Z随时间变化的曲线1、2、3(如图所示)则曲线1、2、3所对应的实验条件改变分别是:1
查看习题详情和答案>>
| tmin | Xmol | Ymol | Zmol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |
X+2Y 2Z
2Z
 2Z
2ZX+2Y 2Z
2Z
; 2Z
2Z(2)列式计算该反应在0~3min时间内产物Z的平均反应速率:
0.083mol/(L?min)
0.083mol/(L?min)
;(3)该反应达到平衡时反应物X的转化率α等于
45%
45%
;
(4)对于上述反应在维持其他条件不变的情况下只改变一种实验条件(温度、压强、催化剂)得到Z随时间变化的曲线1、2、3(如图所示)则曲线1、2、3所对应的实验条件改变分别是:1
升高温度
升高温度
,2加入催化剂
加入催化剂
,3增大压强
增大压强
.该反应的△H<
<
0(填“>”、“<”或“=”),判断理由是:曲线1表示升高温度Z平衡时物质的量减小,平衡逆向移动,
因此正反应为放热反应则有△H<0
因此正反应为放热反应则有△H<0
曲线1表示升高温度Z平衡时物质的量减小,平衡逆向移动,
因此正反应为放热反应则有△H<0
.因此正反应为放热反应则有△H<0
 2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的SO3的反应速率的变化填入下表空格内(填“增大”“减小”或“不变”)。
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的SO3的反应速率的变化填入下表空格内(填“增大”“减小”或“不变”)。