摘要:26.表中为一些短周期元素及相应氢化物沸点的数据: 元 素 性 质 元 素 编 号 ① ② ③ ④ ⑤ ⑥ 氢化物的沸点(℃) -60.7 -33.4 100 -87.7 19.54 -84.9 最 高 化 合 价 +6 +5 +5 +7 最 低 化 合 价 -2 -3 -2 -3 -1 -1 A.B.Y均为上表中的元素.X是一种历史悠久.应用广泛的金属元素. ① X与Y可形成化合物XY.XY2, 二者可用接触法制强酸甲, ② A与B可形成化合物AB.AB2.二者均可用于制备强酸乙. 请回答: (1)元素 ③ 氢化物的分子式是 . (2)下列有关强酸甲.乙说法正确的是 . a. 二者的浓溶液在常温时均可用铁制或铝制的容器贮运 b. 二者的浓溶液在敞口容器中放置.质量都会变化 c. 工业生产强酸甲.乙时.都要用水吸收相应的氧化物 d. 二者的稀溶液均是强氧化剂 (3)工业生产强酸甲时可用浓氨水处理尾气.并获得某种铵盐. 化学方程式为 . (4)写出工业生产强酸乙时获得AB的化学方程式: . (5)工业生产强酸乙时可用纯碱溶液处理尾气.该反应如下: AB + AB2 + Na2CO3 = 2 + CO2 ① 在方框内填某盐的化学式 ② 每产生44.8 LCO2.被吸收尾气的质量是 g. (6) 表中属于第三周期的元素是 (用表中元素编号填写).
网址:http://m.1010jiajiao.com/timu3_id_380492[举报]
表中为一些短周期元素及相应氢化物沸点的数据:
| ||||||||||||||||||||||||||||||||||
查看习题详情和答案>>
表中为一些短周期元素及相应氢化物沸点的数据:
元 素 性 质 | 元 素 编 号 | |||||
① | ② | ③ | ④ | ⑤ | ⑥ | |
氢化物的沸点(℃) | -60.7 | -33.4 | 100 | -87.7 | 19.54 | -84.9 |
最 高 化 合 价 | +6 | +5 | +5 | +7 | ||
最 低 化 合 价 | -2 | -3 | -2 | -3 | -1 | -1 |
A、B、Y均为上表中的元素。X是一种历史悠久,应用广泛的金属元素。
① X与Y可形成化合物XY、XY2, 二者可用接触法制强酸甲;
② A与B可形成化合物AB、AB2,二者均可用于制备强酸乙。
请回答:
(1)元素 ③ 氢化物的分子式是 __________。
(2)下列有关强酸甲、乙说法正确的是 ________。
a. 二者的浓溶液在常温时均可用铁制或铝制的容器贮运
b. 二者的浓溶液在敞口容器中放置,质量都会变化
c. 工业生产强酸甲、乙时,都要用水吸收相应的氧化物
d. 二者的稀溶液均是强氧化剂
(3)工业生产强酸甲时可用浓氨水处理尾气,并获得某种铵盐。
化学方程式为__________________________________。
(4)写出工业生产强酸乙时获得AB的化学方程式: 。
(5)工业生产强酸乙时可用纯碱溶液处理尾气,该反应如下:
AB + AB2 + Na2CO3 = 2 ![]() + CO2
+ CO2
① 在方框内填某盐的化学式
② 每产生44.8 L(标准状况)CO2,被吸收尾气的质量是 ______g。
(6) 表中属于第三周期的元素是_______________(用表中元素编号填写)。
查看习题详情和答案>>
表中为一些短周期元素及相应氢化物沸点的数据:
A、B、Y均为上表中的元素.X是一种历史悠久,应用广泛的金属元素.X与Y可形成化合物XY、XY2,二者可用接触法制强酸甲;A与B可形成化合物AB、AB2,二者均可用于制备强酸乙.下列有关强酸甲、乙的说法正确的是( )
A.二者的浓溶液在常温时均可用X的单质制成容器储运
B.工业生产强酸乙的第一步是将②的氢化物在纯氧中燃烧氧化生成AB
C.工业生产强酸甲、乙时,都要用水吸收相应的氧化物
D.①②③的氢化物均能被强酸甲的浓溶液吸收
查看习题详情和答案>>
| 元素性质 | 元素编号 | |||||
| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 氢化物的沸点(℃) | -60.7 | -33.4 | 100 | -87.7 | 19.54 | -84.9 |
| 最高化合价 | +6 | +5 | +5 | +7 | ||
| 最低化合价 | -2 | -3 | -2 | -3 | -1 | -1 |
A.二者的浓溶液在常温时均可用X的单质制成容器储运
B.工业生产强酸乙的第一步是将②的氢化物在纯氧中燃烧氧化生成AB
C.工业生产强酸甲、乙时,都要用水吸收相应的氧化物
D.①②③的氢化物均能被强酸甲的浓溶液吸收
查看习题详情和答案>>
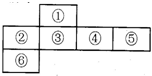 短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;如图是元素周期表的一部分,编号为③的元素最外层与最内层电子数相等
短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;如图是元素周期表的一部分,编号为③的元素最外层与最内层电子数相等(1)编号为⑤的元素的符号为
Si
Si
,其在周期表中位于第三周期第ⅣA族
第三周期第ⅣA族
.(2)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式:
Be+2OH-═BeO22-+H2↑
Be+2OH-═BeO22-+H2↑
.(3)己知AlCl3的熔点为190℃(2.5×105Pa),沸点为182.7℃,试推测:
①BeCl2是
共价
共价
化合物(填“离子”或“共价”),②Be(OH)2的碱性比LiOH弱
弱
.(4)根据Mg在空气中的燃烧情况,Li在空气中燃烧生成的产物为
Li2O
Li2O
(用化学式表示).