题目内容
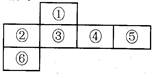
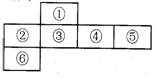
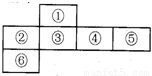
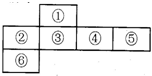 短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;如图是元素周期表的一部分,编号为③的元素最外层与最内层电子数相等
短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;如图是元素周期表的一部分,编号为③的元素最外层与最内层电子数相等(1)编号为⑤的元素的符号为
Si
Si
,其在周期表中位于第三周期第ⅣA族
第三周期第ⅣA族
.(2)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式:
Be+2OH-═BeO22-+H2↑
Be+2OH-═BeO22-+H2↑
.(3)己知AlCl3的熔点为190℃(2.5×105Pa),沸点为182.7℃,试推测:
①BeCl2是
共价
共价
化合物(填“离子”或“共价”),②Be(OH)2的碱性比LiOH弱
弱
.(4)根据Mg在空气中的燃烧情况,Li在空气中燃烧生成的产物为
Li2O
Li2O
(用化学式表示).分析:③的元素最外层与最内层电子数相等,最内层电子为2,则最外层电子为2,应为Mg,结合元素在周期表中的位置可知,①为Be,②为Na,④为Al,⑤为Si,⑥为K,然后结合元素及其单质、化合物的性质来解答.
解答:解:③的元素最外层与最内层电子数相等,最内层电子为2,则最外层电子为2,应为Mg,结合元素在周期表中的位置可知,①为Be,②为Na,④为Al,⑤为Si,⑥为K,
(1)⑤为Si,位于第三周期第ⅣA族,故答案为:Si;第三周期第ⅣA族;
(2)由信息可知铍和铝都能与氢氧化钠溶液反应,则Be与NaOH溶液反应生成Na2BeO2的离子方程式为Be+2OH-═BeO22-+H2↑,
故答案为:Be+2OH-═BeO22-+H2↑;
(3)①由熔沸点较低可知,为共价化合物形成的分子晶体,短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,Be与Al位于对角线位置,性质相似,则BeCl2是共价化合物,故答案为:共价;
②由同周期从左向右金属性减弱可知,Be(OH)2的碱性比LiOH弱,故答案为:弱;
(4)Li在空气中燃烧生成的产物为Li2O,故答案为:Li2O.
(1)⑤为Si,位于第三周期第ⅣA族,故答案为:Si;第三周期第ⅣA族;
(2)由信息可知铍和铝都能与氢氧化钠溶液反应,则Be与NaOH溶液反应生成Na2BeO2的离子方程式为Be+2OH-═BeO22-+H2↑,
故答案为:Be+2OH-═BeO22-+H2↑;
(3)①由熔沸点较低可知,为共价化合物形成的分子晶体,短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,Be与Al位于对角线位置,性质相似,则BeCl2是共价化合物,故答案为:共价;
②由同周期从左向右金属性减弱可知,Be(OH)2的碱性比LiOH弱,故答案为:弱;
(4)Li在空气中燃烧生成的产物为Li2O,故答案为:Li2O.
点评:本题考查位置、结构、性质的应用,③为解答本题的突破口,熟悉元素在周期表中的位置及元素的单质、化合物的性质即可解答,题目难度不大,注意对角线规则的利用.

练习册系列答案
相关题目