摘要:22.下表中表示元素周期表的边界结构.①-⑤分别表示元素周期表中对应位置的元素. ③ ④ ⑤ ① ② (1)短周期元素甲的最外层电子数是两个内层电子数之差.则甲元素的元素符号为 . (2)元素乙的M层电子数只有甲元素的一半.则乙原子半径与甲原子半径比较: > ,甲.乙的最高价氧化物水化物的酸性强弱为: > . (3)元素⑤的单质与元素④的氢化物反应的化学方程式为: .元素③氢化物的电子式为 .元素④在与⑤形成化合物时.元素④化合物中显 价. (4)右图中A.B.C三条曲线分别表示③.④.⑤三种元素所在主族元素的气态氢化物的沸点.其中表示元素④所在主族元素气态氢化物沸点的是曲线 ,同一族中第3.4.5周期元素的气态氢化物沸点依次升高.其原因是 ,A.B.C曲线中第2周期元素的气态氢化物的沸点显著高于第3周期元素气态氢化物沸点的原因是 .
网址:http://m.1010jiajiao.com/timu3_id_377339[举报]
如图是元素周期表的框架图,请根据下面提问回答下列问题:
(1)请在表中用实线补全元素周期表的边界.

(2)请用物质的名称填写.
硬度最大的是单质是
(3)在原子序数为1~18号元素中,请用化学式填写.
与水反应最剧烈的金属单质是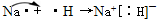
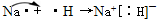 .
.
(4)在原子序数为1~18号元素中,请按要求填写下列空白.
由两种元素组成的淡黄色化合物的电子式为
 ;空气中含量最高的物质的结构式为
;空气中含量最高的物质的结构式为
 ;某元素最高价氧化物的水化物与其气态氢化物反应生成一种盐,该盐的化学式为
;某元素最高价氧化物的水化物与其气态氢化物反应生成一种盐,该盐的化学式为
查看习题详情和答案>>


(2)请用物质的名称填写.
硬度最大的是单质是
金刚石
金刚石
,密度最小的金属是锂
锂
;通常状况呈液态的非金属单质是溴
溴
,地壳中含量最多的金属元素是铝
铝
.(3)在原子序数为1~18号元素中,请用化学式填写.
与水反应最剧烈的金属单质是
Na
Na
;元素的气态氢化物最稳定的是HF
HF
;元素的最高价氧化物所对应的水化物其酸性最强的是HClO4
HClO4
;原子半径最大的金属与原子半径最小的非金属形成的化合物是NaH
NaH
,并用电子式表示其形成过程: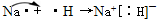
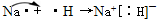
(4)在原子序数为1~18号元素中,请按要求填写下列空白.
由两种元素组成的淡黄色化合物的电子式为


N≡N
N≡N
;常温下为气态,固态常用于人工降雨的氧化物的电子式为

NH4NO3
NH4NO3
,该化合物中的化学键类型是离子键和极性共价键
离子键和极性共价键
.(10分)下表中的实线表示元素周期表的部分边界。①-⑥分别表示元素周期表中对应位置的元素。
(1)请在上表中用实线补全元素周期表边界。
(2)写出①、③两种元素组成的正四面体化合物的电子式 上述元素中,上述元素中能和⑤号元素形成正四面体空间网状结构的化合物的化学式是
(3)上述元素中的一种元素其气态氢化物和该元素的最高价氧化物的水化物能发生化合反应,该反应的化学反应方程式为____________________________________________________
该物质含有的化学键是 。
查看习题详情和答案>>
(10分)下表中的实线表示元素周期表的部分边界。①-⑥分别表示元素周期表中对应位置的元素。
(1 )请在上表中用实线补全元素周期表边界。
)请在上表中用实线补全元素周期表边界。
(2)写出①、③两种元素组成的正四面体化合物的电子式 上述元素中,上述元素中能和⑤号元素形成正四面体空间网状结构的化合物的化学式是
(3)上述元素中的一种元素其气态氢化物和该元素的最高价氧化物的水化物能发生化合反应,该反应的化学反应方程式为____________________________________________________
该物质含有的化学键是 。

