摘要:1]0 C.D
网址:http://m.1010jiajiao.com/timu3_id_357105[举报]
. “1.0 mol/L的Na2SO4溶液”的含义是 ( )
A、1L水中有1mol Na2SO4 B、1L溶液中含有142g Na2SO4
C、SO4 2-的物质的量浓度为2.0 mol/L D、1LNa2SO4溶液中含有Na+1 mol
查看习题详情和答案>>
|
C、CO、CH4、C2H5OH是常用的燃料,它们每1 mol分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量依次为393.5 kJ、283.0 kJ、890.3 kJ、1366.8 kJ.相同质量的这4种燃料,完全燃烧时放出热量最多的是 | |
| [ ] | |
A. |
C |
B. |
CO |
C. |
CH4 |
D. |
C2H5OH |
1 000K时反应C(s)+2H2(g)?CH4(g)的K=8.28×107,当各气体物质的量浓度分别为H2 0.7mol?L-1、CH4 0.2mol?L-1时,上述反应( )
查看习题详情和答案>>

Ⅰ、(1)在某容积为10L的密闭容器中,有可逆反应:
mA(g)+nB(g)?pC(g)+qD(s)△H<0.
如图1为某反应过程中各物质物质的量n(mol)随时间t(min)的变化曲线图.
①在0~15min内的平均反应速率:v(B)=
0.01mol/(L?min)
0.01mol/(L?min)
.②该反应的平衡常数表达式为
| c2(C) |
| c(A)×c3(B) |
| c2(C) |
| c(A)×c3(B) |
③下列哪些物理量不再变化时可以表明该反应已经到达平衡状态
a
a
(填字母,多选、少选均扣分)a.混合气体的压强 b.混合气体的密度
c.混合气体的总体积 d.c(A)与c(B)的比值
(2)若该反应的正反应速率与时间的关系如图2所示.在其他条件不变的情况下,t2时改变的条件可能是
降低温度
降低温度
;Ⅱ、(1)常温下,0.1mol?L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是
BD
BD
(填序号) A.c(H+) B.c(H+)/c(CH3COOH)
C.c(H+)?c(OH-) D.c(OH-)/c(H+)
(2)体积均为100mLpH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图3所示,则Ka(HX)
大于
大于
(填“大于”、“小于”或“等于”)Ka(CH3COOH).(3)23℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中离子浓度大小关系是
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
,c(CH3COO-)/c(CH3COOH)=18
18
. (已知醋酸的电离平衡常数Ka=1.8×10-5)Ⅰ、表中①~⑥为部分短周期元素的化合价及原子半径
Ⅱ、B与C两元素可形成化合物CB2、CB3,二者均可用于制备化合物甲
Ⅲ、A与B两元素可形成化合物AB、AB2,二者均可用于制备化合物乙.
A、B、C均为上表中的元素,甲、乙为中学常见强酸.
请回答下列问题(1)写出B元素位于周期表中的位置
(2)A元素气态氢化物的结构式为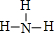
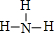 ,写出上述元素形成的最稳定的氢化物的电子式
,写出上述元素形成的最稳定的氢化物的电子式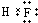
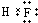 _
_
(3)下列关于物质甲、乙的说法中正确的是
a.二者的浓溶液在常温时均可用铁制容器贮存
b.二者的浓溶液在敞口容器中放置,质量都会变化
c.二者的浓溶液在常温时均与铜反应
d.二者的稀溶液均具有强氧化性
(4)请写出工业上由CB2制备CB3的化学方程式
写出工业生产强酸乙的过程中制备化合物AB的化学方程式
查看习题详情和答案>>
| 元素性质 | 元素编号 | |||||
| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 原子半径/nm | 0.102 | 0.110 | 0.074 | 0.075 | 0.071 | 0.099 |
| 最高化合价 | +6 | +5 | +5 | +7 | ||
| 最低化合价 | -2 | -3 | -2 | -3 | -1 | -1 |
Ⅲ、A与B两元素可形成化合物AB、AB2,二者均可用于制备化合物乙.
A、B、C均为上表中的元素,甲、乙为中学常见强酸.
请回答下列问题(1)写出B元素位于周期表中的位置
第二周期第ⅥA族
第二周期第ⅥA族
(2)A元素气态氢化物的结构式为
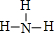
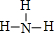
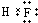
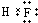
(3)下列关于物质甲、乙的说法中正确的是
ab
ab
(填字母)a.二者的浓溶液在常温时均可用铁制容器贮存
b.二者的浓溶液在敞口容器中放置,质量都会变化
c.二者的浓溶液在常温时均与铜反应
d.二者的稀溶液均具有强氧化性
(4)请写出工业上由CB2制备CB3的化学方程式
2SO2+O2
2SO3
| ||
| △ |
2SO2+O2
2SO3
.
| ||
| △ |
写出工业生产强酸乙的过程中制备化合物AB的化学方程式
4NH3+5O2
4NO+6H2O
| ||
| 高温高压 |
4NH3+5O2
4NO+6H2O
.
| ||
| 高温高压 |