摘要:Be+2OH-=BeO2-+H22+2OH-=BeO22-+2H2O(3)共价..Li3N
网址:http://m.1010jiajiao.com/timu3_id_344271[举报]
下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
试回答下列问题:
(1)表中属于d区的元素有

(2)写出元素L的基态原子的电子排布式
(3)某元素的特征电子排布式为(n+1)sn(n+1)pn-1,在上周期中,与该元素为对角线关系的元素形成的单质与氢氧化钠溶液反应的离子方程式
(4)比较M的氢化物与同族第二周期元素所形成的氢化物稳定性由高到低的顺序为
查看习题详情和答案>>
| A | |||||||||||||||||
| B | C | D | E | ||||||||||||||
| F | G | H | I | ||||||||||||||
| J | K | L | M | ||||||||||||||
(1)表中属于d区的元素有
J K L
J K L
(填所选字母).用电子式表示G和I形成的化合物的形成过程:

(2)写出元素L的基态原子的电子排布式
1S22S22P63S23P6 3d104s1
1S22S22P63S23P6 3d104s1
.(3)某元素的特征电子排布式为(n+1)sn(n+1)pn-1,在上周期中,与该元素为对角线关系的元素形成的单质与氢氧化钠溶液反应的离子方程式
Be+2OH-=BeO22-+H2↑
Be+2OH-=BeO22-+H2↑
(4)比较M的氢化物与同族第二周期元素所形成的氢化物稳定性由高到低的顺序为
NH3>AsH3
NH3>AsH3
(用化学式表示),并说明理由同主族从上到下原子半径依次增大,氢化物的稳定性同主族从上到下非金属性减弱,氢化物稳定性减弱
同主族从上到下原子半径依次增大,氢化物的稳定性同主族从上到下非金属性减弱,氢化物稳定性减弱
.根据周期表对角线规则,金属铍与铝的单质及其化合物性质相似,又已知氯化铝的熔、沸点较低,易升化.回答下列问题:
(1)写出铍与氢氧化钠反应的离子方程式
(2)氢氧化铍与氢氧化镁可用
(3)锂和镁据对角线规则,性质也相似.锂在空气中燃烧主要产物的电子式是
 ,同时还有少量的
,同时还有少量的
查看习题详情和答案>>
(1)写出铍与氢氧化钠反应的离子方程式
Be+2OH-═BeO22-+H2↑
Be+2OH-═BeO22-+H2↑
.(2)氢氧化铍与氢氧化镁可用
NaOH溶液
NaOH溶液
鉴别,其离子方程式是Be(OH)2+2OH-═BeO22-+2H2O
Be(OH)2+2OH-═BeO22-+2H2O
.氯化铍属于共价
共价
(填“离子”或“共价”)化合物.(3)锂和镁据对角线规则,性质也相似.锂在空气中燃烧主要产物的电子式是


Li3N
Li3N
生成.铍和铝、锂和镁等在元素周期表中具有特殊的“对角线关系”,单质及化合物的性质十分相似.请按要求回答下列各问:
(1)写出Be与NaOH溶液反应的离子方程式(生成Na2BeO2):
查看习题详情和答案>>
(1)写出Be与NaOH溶液反应的离子方程式(生成Na2BeO2):
Be+2OH-═BeO22-+H2↑
Be+2OH-═BeO22-+H2↑
;(2)Be(OH)2与Mg(OH)2可用试剂NaOH溶液
NaOH溶液
鉴别,其离子方程式为:Be(OH)2+2OH-═BeO22-+2H2O
Be(OH)2+2OH-═BeO22-+2H2O
.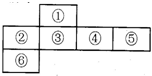 短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;如图是元素周期表的一部分,编号为③的元素最外层与最内层电子数相等
短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;如图是元素周期表的一部分,编号为③的元素最外层与最内层电子数相等(1)编号为⑤的元素的符号为
Si
Si
,其在周期表中位于第三周期第ⅣA族
第三周期第ⅣA族
.(2)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式:
Be+2OH-═BeO22-+H2↑
Be+2OH-═BeO22-+H2↑
.(3)己知AlCl3的熔点为190℃(2.5×105Pa),沸点为182.7℃,试推测:
①BeCl2是
共价
共价
化合物(填“离子”或“共价”),②Be(OH)2的碱性比LiOH弱
弱
.(4)根据Mg在空气中的燃烧情况,Li在空气中燃烧生成的产物为
Li2O
Li2O
(用化学式表示).下表中所列的是8种短周期元素原子的半径及主要化合价:
(1)C元素在周期表中的位置为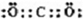
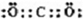 ,G元素最低价氢化物的空间构型为
,G元素最低价氢化物的空间构型为
(2)B、D、E所代表元素的离子半径从大到小的顺序为
(3)C与E形成的化合物属于
(4)周期表中有些元素存在“对角线相似”现象(一种元素的性质常同它右下方相邻的另一种元素具有类似性),请写出A的单质与强碱溶液反应的离子方程式:
(5)有人认为:H-E键的键能大于H-L键的键能,所以H2E的沸点高于H2L的沸点.你是否赞同这种观点
查看习题详情和答案>>
| 元素代号 | A | B | C | D | E | G | L | I |
| 原子半径/nm | 0.111 | 0.064 | 0.117 | 0.16 | 0.066 | 0.070 | 0.104 | 0.077 |
| 主要化合价 | +2 | -1 | +4,-4 | +2 | -2 | +5.-3 | +6,-2 | +4,-4 |
第三周期ⅣA族
第三周期ⅣA族
;IE2的电子式为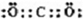
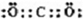
三角锥型
三角锥型
.(2)B、D、E所代表元素的离子半径从大到小的顺序为
O2->F->Mg2+
O2->F->Mg2+
(填离子符号).G、C最高价氧化物对应水化物的酸性强弱关系为(写化学式)HNO3>H2SiO3
HNO3>H2SiO3
.(3)C与E形成的化合物属于
原子
原子
晶体.(4)周期表中有些元素存在“对角线相似”现象(一种元素的性质常同它右下方相邻的另一种元素具有类似性),请写出A的单质与强碱溶液反应的离子方程式:
Be+2OH-═BeO22-+H2↑
Be+2OH-═BeO22-+H2↑
.(5)有人认为:H-E键的键能大于H-L键的键能,所以H2E的沸点高于H2L的沸点.你是否赞同这种观点
不赞同
不赞同
(填“赞同”或“不赞同”),理由:H2O与H2S所成晶体为分子晶体,H2O的熔沸点高于H2S的熔沸点与键能无关
H2O与H2S所成晶体为分子晶体,H2O的熔沸点高于H2S的熔沸点与键能无关
.