摘要: []>[ Fe3+ ]>[ Fe2+ ]>[ H+ ]>[ OH- ]
网址:http://m.1010jiajiao.com/timu3_id_343926[举报]
(1)与OH-电子数和质子数均相同的单核微粒的离子结构示意图为 ;
(2)要证明某溶液不含Fe3+但可能含有Fe2+,最佳的实验操作顺序是 (填选项);
①加入少量氯水②加入足量KMnO4溶液③加入少量NH4SCN溶液
A.①③B.③②C.③①D.①②③
(3)25℃时,2.3g酒精在血液中被氧气完全氧化放出66.8kJ热量,该反应的热化学方程式为 ;
(4)汽车安全气囊中含MYn和红棕色金属氧化物.M、Y为短周期元素,其最外层电子数之和等于氧原子的最外层电子数,且可发生如图的转化.
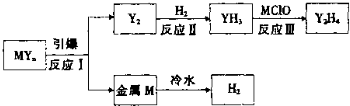
①在2L密闭容器中,起始投入2mol Y2和3.5mol H2发生反应Ⅱ,测得平衡时的数据如表.若该反应△H<0,则T1 T2(填“>”、“<”或“=”);在温度T2下,若经过10min反应达到平衡,则平均速率v(YH3)= ,平衡常数为 ;(保留两位有效数字)
②反应Ⅲ的化学方程式为 ;
③红棕色金属氧化物是为消除反应Ⅰ生成的金属M,该反应的化学方程式为 .
查看习题详情和答案>>
(2)要证明某溶液不含Fe3+但可能含有Fe2+,最佳的实验操作顺序是
①加入少量氯水②加入足量KMnO4溶液③加入少量NH4SCN溶液
A.①③B.③②C.③①D.①②③
(3)25℃时,2.3g酒精在血液中被氧气完全氧化放出66.8kJ热量,该反应的热化学方程式为
(4)汽车安全气囊中含MYn和红棕色金属氧化物.M、Y为短周期元素,其最外层电子数之和等于氧原子的最外层电子数,且可发生如图的转化.

①在2L密闭容器中,起始投入2mol Y2和3.5mol H2发生反应Ⅱ,测得平衡时的数据如表.若该反应△H<0,则T1
| 温度 | 平衡时YH3的物质的量(mol) |
| T1 | 1.2 |
| T2 | 1.0 |
③红棕色金属氧化物是为消除反应Ⅰ生成的金属M,该反应的化学方程式为
下列排列顺序正确的是
①沸点:H2S>H2O
②氧化性:Cu2+>Fe3+>H+>Fe2+
③原子半径:Na>Mg>O
④还原性:F->Cl->S2-
⑤结合H+的能力:OH->CH3COO->Cl-
- A.①③④
- B.②③
- C.③⑤
- D.②④⑤
|
下列排列顺序正确的是 ①沸点:H2S>H2O ②氧化性:Cu2+>Fe3+>H+>Fe2+ ③原子半径:Na>Mg>O ④还原性:F->Cl->S2- ⑤结合H+的能力:OH->CH3COO->Cl- | |
| [ ] | |
A. |
①③④ |
B. |
②③ |
C. |
③⑤ |
D. |
②④⑤ |