摘要:4.将agCu投入一定浓度的硝酸溶液中.反应中消耗HNO3为bg.若a:b=8:21.则反应中起酸作用的HNO3质量为 ( ) A.b/2g B.2bg C.3a/4g D.3b/4g 将32.64g铜与140mL一定浓度的硝酸反应.铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L.请回答: ⑴NO的体积为5.8L.NO2的体积为5.4L. ⑵待产生的气体全部释放后.向溶液中加入VmLamol/L的NaOH溶液.恰好使溶液中的Cu2+全部转化成沉淀.则原硝酸溶液的浓度为(aV•10-3+0.5)/0.14mol/L. ⑶欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3.至少需要30%的双氧水57.8g. (4)Fe与稀HNO3反应的分析与计算
网址:http://m.1010jiajiao.com/timu3_id_342863[举报]
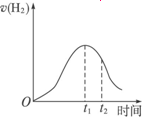
下图所示为将Zn投入一定浓度一定体积的H2SO4溶液中,解释图象的成因(纵坐标为H2的生成速率)。

(1)0—t1速率变化的原因是______________________________。
(2)t1—t2速率变化的原因是______________________________。
查看习题详情和答案>>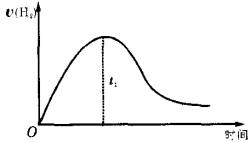
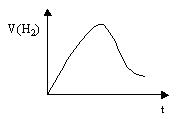 将Zn投入一定浓度一定体积的盐酸中,H2的生成速率与时间的关系如图所示,试解释图中曲线变化的原因(纵坐标为H2的生成速率,横坐标为时间)。
将Zn投入一定浓度一定体积的盐酸中,H2的生成速率与时间的关系如图所示,试解释图中曲线变化的原因(纵坐标为H2的生成速率,横坐标为时间)。