摘要: 比较氧化剂的氧化性或还原剂的还原性的强弱,
网址:http://m.1010jiajiao.com/timu3_id_342403[举报]
高铁酸钾(K2FeO4)是集氧化、吸附、絮凝于一体的新型多功能水处理剂,其生产工艺如下:
已知:①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3C12=5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+2KC1O+10KOH=2K2FeO4+6KNO3+2KCl+5H2O
回答下列问题:(1)该工艺应在 (填“温度较高”或“温度较低”)的情况下进行,
(2)K2FeO4可作为新型多功能水处理剂的原因 ,
(3)在“反应液I”中加KOH固体的目的是① ,②为下一步反应提供反应物,
(4)从“反应液II”中分离出K2FeO4后,副产品是 (写化学式),
(5)高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压高铁电池的总反应3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH
①写出该电池充电时阳极的电极反应式 ,
②下列叙述正确的是 (填字母)
A.Zn电极在放电时作负极,发生氧化反应
B.该电池放电时,K+向负极移动
C.放电时正极有1mol K2FeO4被还原,则转移3mol电子
③用该电池电解200mL 1mol?L-1 的AgNO3溶液(用惰性电极),当阴极质量增加2.16g时,被电解溶液的pH为 (溶液体积变化忽略不计).
查看习题详情和答案>>

已知:①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3C12=5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+2KC1O+10KOH=2K2FeO4+6KNO3+2KCl+5H2O
回答下列问题:(1)该工艺应在
(2)K2FeO4可作为新型多功能水处理剂的原因
(3)在“反应液I”中加KOH固体的目的是①
(4)从“反应液II”中分离出K2FeO4后,副产品是
(5)高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压高铁电池的总反应3Zn+2K2FeO4+8H2O
| 放电 | 充电 |
①写出该电池充电时阳极的电极反应式
②下列叙述正确的是
A.Zn电极在放电时作负极,发生氧化反应
B.该电池放电时,K+向负极移动
C.放电时正极有1mol K2FeO4被还原,则转移3mol电子
③用该电池电解200mL 1mol?L-1 的AgNO3溶液(用惰性电极),当阴极质量增加2.16g时,被电解溶液的pH为
(14分)氮的化合物是中学化学的重要物质,与人类生活密切相关。
(1)金属与不同密度的硝酸溶液反应所得的还原产物比较复杂,如图所示: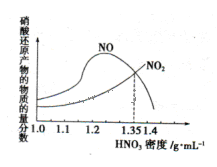
请写出铁与密度为1.35 g.m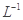 的硝酸反应的化学方程式:______________________.
的硝酸反应的化学方程式:______________________.
(2)亚硝酸钠是一种致癌物质,它在中性或碱性条件下是稳定的,酸化后能氧化碘化钾生成棕色溶液和NO,则该反应中氧化剂与还原剂的物质的量之比为____。
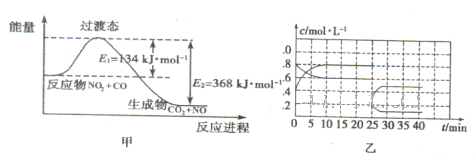
(3)如图甲为NO2和C0反应生成CO2和NO过程的能量变化示意图,请写出该反应的热化学方程式:__________________________________________________________.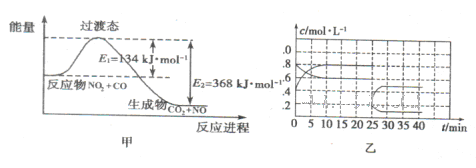
(4)已知NO2和N2O4可以相互转化:2NO2(g)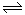 N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。
N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。
①前10 min内用NO2表示的平均反应速率v(NO2)= ;上述反应的平衡常数K=__________。
②反应进行至25 min时,曲线发生变化的原因是________________________.
③若要使上述反应的平衡常数K增大,采取的措施是_________________。
| A.加入催化剂 | B.缩小容器体积 | C.降低温度 | D.再加入一定量的NO2 |
(14分)氮的化合物是中学化学的重要物质,与人类生活密切相关。
(1)金属与不同密度的硝酸溶液反应所得的还原产物比较复杂,如图所示:

请写出铁与密度为1.35 g.m 的硝酸反应的化学方程式:______________________.
的硝酸反应的化学方程式:______________________.
(2)亚硝酸钠是一种致癌物质,它在中性或碱性条件下是稳定的,酸化后能氧化碘化钾生成棕色溶液和NO,则该反应中氧化剂与还原剂的物质的量之比为____。
(3)如图甲为NO2和C0反应生成CO2和NO过程的能量变化示意图,请写出该反应的热化学方程式:__________________________________________________________.
(4)已知NO2和N2O4可以相互转化:2NO2(g) N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。
N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。
①前10 min内用NO2表示的平均反应速率v(NO2)= ;上述反应的平衡常数K=__________。
②反应进行至25 min时,曲线发生变化的原因是________________________.
③若要使上述反应的平衡常数K增大,采取的措施是_________________。
(1)金属与不同密度的硝酸溶液反应所得的还原产物比较复杂,如图所示:

请写出铁与密度为1.35 g.m
 的硝酸反应的化学方程式:______________________.
的硝酸反应的化学方程式:______________________.(2)亚硝酸钠是一种致癌物质,它在中性或碱性条件下是稳定的,酸化后能氧化碘化钾生成棕色溶液和NO,则该反应中氧化剂与还原剂的物质的量之比为____。
(3)如图甲为NO2和C0反应生成CO2和NO过程的能量变化示意图,请写出该反应的热化学方程式:__________________________________________________________.

(4)已知NO2和N2O4可以相互转化:2NO2(g)
 N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。
N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。①前10 min内用NO2表示的平均反应速率v(NO2)= ;上述反应的平衡常数K=__________。
②反应进行至25 min时,曲线发生变化的原因是________________________.
③若要使上述反应的平衡常数K增大,采取的措施是_________________。
| A.加入催化剂 | B.缩小容器体积 | C.降低温度 | D.再加入一定量的NO2 |
材料1:N2O5是一种新型硝化剂,其性质和制备受到人们的关注.一定温度下,在密闭容器中N2O5可发生下列反应:
①2N2O5(g)?4NO2(g)+O2(g);△H>0
②2NO2(g)?2NO(g)+O2(g);△H>0

若达平衡时,c(NO2)=0.4mol?L-1,c(O2)=1.3mol?L-1.
(1)反应②中NO2的转化率为
(2)将密闭容器内的氮氧化物用水吸收完全转化为硝酸,是否还需要通入氧气?
(3)如图1装置可用于制备N2O5,则N2O5在电解池的
材料2:选择性催化还原法(SCR)脱除NOx具有较高的效率,是目前工业中应用最广泛的工艺.在一定条件下可用SnO2/Al2O3等多种催化剂实现丙烯选择性还原NOx,
③18NO(g)+2C3H6(g)?9N2(g)+6CO2(g)+6H2O(g);△H1
④18NO2(g)+4C3H6(g)?9N2(g)+12CO2(g)+12H2O(g);△H2
探究丙烯还原NOx有关问题:
(4)在容积相同的两组均为多个密闭容器内(装有等量的某种催化剂),分别充入同量的NOx及C3H6,在不同温度下,同时发生可逆反应③或④,并分别在t秒时测定其中NOx转化率,绘得如如图2所示,下列说法不正确的是
A.反应③的△Hl<0;反应④的△H2<0
B.反应③中,当反应消耗2molNO的同时生成了1molN2,说明该反应已达平衡
C.该催化剂在450℃活性最大
D.对于反应③,其他条件不变时,增大压强,NO转化率增大
E.相同条件下,NO2的转化率要比NO的大.
查看习题详情和答案>>
①2N2O5(g)?4NO2(g)+O2(g);△H>0
②2NO2(g)?2NO(g)+O2(g);△H>0

若达平衡时,c(NO2)=0.4mol?L-1,c(O2)=1.3mol?L-1.
(1)反应②中NO2的转化率为
80%
80%
,N2O5(g)的起始浓度应不低于1
1
mol?L-1.(2)将密闭容器内的氮氧化物用水吸收完全转化为硝酸,是否还需要通入氧气?
需要
需要
(填“需要”或“不需要”).(3)如图1装置可用于制备N2O5,则N2O5在电解池的
阳极
阳极
(填“阳极”或“阴极”)区生成,其电极反应式为N2O4+2HNO3-2e-=2N2O5+2H+
N2O4+2HNO3-2e-=2N2O5+2H+
.材料2:选择性催化还原法(SCR)脱除NOx具有较高的效率,是目前工业中应用最广泛的工艺.在一定条件下可用SnO2/Al2O3等多种催化剂实现丙烯选择性还原NOx,
③18NO(g)+2C3H6(g)?9N2(g)+6CO2(g)+6H2O(g);△H1
④18NO2(g)+4C3H6(g)?9N2(g)+12CO2(g)+12H2O(g);△H2
探究丙烯还原NOx有关问题:
(4)在容积相同的两组均为多个密闭容器内(装有等量的某种催化剂),分别充入同量的NOx及C3H6,在不同温度下,同时发生可逆反应③或④,并分别在t秒时测定其中NOx转化率,绘得如如图2所示,下列说法不正确的是
BDE
BDE
.(填序号)A.反应③的△Hl<0;反应④的△H2<0
B.反应③中,当反应消耗2molNO的同时生成了1molN2,说明该反应已达平衡
C.该催化剂在450℃活性最大
D.对于反应③,其他条件不变时,增大压强,NO转化率增大
E.相同条件下,NO2的转化率要比NO的大.
高锰酸钾是一种典型的强氧化剂,无论在实验室还是在化工生产中都有重要的应用.如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).

(1)制备氯气选用的药品为:高锰酸钾和浓盐酸,相应的离子方程式为: .
(2)装置B的作用是 ,监测实验进行时C中可能发生堵塞,请写出发生堵塞时B中的现象 .
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、Ⅱ、Ⅲ依次放入 .(选a或b或c)
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性.当向D中缓缓通入足量氯气时,可以看到无色溶液逐渐变为红棕色,说明氯的非金属性大于溴.打开活塞,将D中的少量溶液加入E中,振荡E.观察到的现象是 .该现象 (填“能”或“不能”)说明溴的非金属性强于碘,原因是 .
查看习题详情和答案>>

(1)制备氯气选用的药品为:高锰酸钾和浓盐酸,相应的离子方程式为:
(2)装置B的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、Ⅱ、Ⅲ依次放入
| a | b | c | |
| I | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |