题目内容
(14分)氮的化合物是中学化学的重要物质,与人类生活密切相关。
(1)金属与不同密度的硝酸溶液反应所得的还原产物比较复杂,如图所示:

请写出铁与密度为1.35 g.m 的硝酸反应的化学方程式:______________________.
的硝酸反应的化学方程式:______________________.
(2)亚硝酸钠是一种致癌物质,它在中性或碱性条件下是稳定的,酸化后能氧化碘化钾生成棕色溶液和NO,则该反应中氧化剂与还原剂的物质的量之比为____。
(3)如图甲为NO2和C0反应生成CO2和NO过程的能量变化示意图,请写出该反应的热化学方程式:__________________________________________________________.
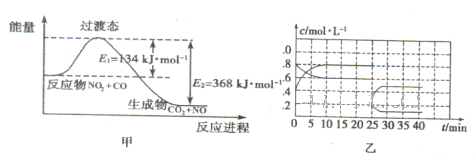
(4)已知NO2和N2O4可以相互转化:2NO2(g) N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。
N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。
①前10 min内用NO2表示的平均反应速率v(NO2)= ;上述反应的平衡常数K=__________。
②反应进行至25 min时,曲线发生变化的原因是________________________.
③若要使上述反应的平衡常数K增大,采取的措施是_________________。
(1)金属与不同密度的硝酸溶液反应所得的还原产物比较复杂,如图所示:

请写出铁与密度为1.35 g.m
 的硝酸反应的化学方程式:______________________.
的硝酸反应的化学方程式:______________________.(2)亚硝酸钠是一种致癌物质,它在中性或碱性条件下是稳定的,酸化后能氧化碘化钾生成棕色溶液和NO,则该反应中氧化剂与还原剂的物质的量之比为____。
(3)如图甲为NO2和C0反应生成CO2和NO过程的能量变化示意图,请写出该反应的热化学方程式:__________________________________________________________.

(4)已知NO2和N2O4可以相互转化:2NO2(g)
 N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。
N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。①前10 min内用NO2表示的平均反应速率v(NO2)= ;上述反应的平衡常数K=__________。
②反应进行至25 min时,曲线发生变化的原因是________________________.
③若要使上述反应的平衡常数K增大,采取的措施是_________________。
| A.加入催化剂 | B.缩小容器体积 | C.降低温度 | D.再加入一定量的NO2 |
(14分)
(1)4Fe+18HNO3="4" Fe(NO3)3+3NO2↑+3NO↑+9H2O;(2分)
(2)1:1(2分)
(3)NO2(g)+CO(g)=CO2(g)+NO(g) △H=-234kJ/mol(2分)
(4)①0.04 mol·L-1·min-1;(2分)0.9375;(2分)②增大容器体积;(2分)③C(2分)
(1)4Fe+18HNO3="4" Fe(NO3)3+3NO2↑+3NO↑+9H2O;(2分)
(2)1:1(2分)
(3)NO2(g)+CO(g)=CO2(g)+NO(g) △H=-234kJ/mol(2分)
(4)①0.04 mol·L-1·min-1;(2分)0.9375;(2分)②增大容器体积;(2分)③C(2分)
试题分析:(1)由图可知Fe与密度为1.35 g·mL-1的硝酸反应的气体产物是NO2、NO,且二者的物质的量相等,所以该反应的化学方程式为4Fe+18HNO3="4" Fe(NO3)3+3NO2↑+3NO↑+9H2O;
(2)亚硝酸钠酸化后能氧化碘,其中亚硝酸钠作氧化剂,碘化钾作还原剂,2NO2-~2NO,得2个电子,2I-~I2,失去2个电子,根据得失电子守恒规律,氧化剂与还原剂的物质的量之比为1:1;
(3)由图甲判断NO2和C0反应生成CO2和NO过程为放热反应,△H=E1-E2=-234kJ/mol,所以该反应的热化学方程式为NO2(g)+CO(g)=CO2(g)+NO(g) △H=-234kJ/mol;
(4)①根据乙图可知,浓度增大的曲线表示NO2,前10 min内NO2的浓度由0.4mol·L-1增大到0.8 mol·L-1,浓度的改变量是0.4 mol·L-1,所以前10 min内用NO2表示的平均反应速率
v(NO2)="0.4" mol·L-1/10min="0.04" mol·L-1·min-1;平衡时NO2和N2O4的浓度分别为0.8mol/L、0.6mol/L,所以K=0.6mol/L/0.82mol/L=0.9375;
②由图分析,NO2和N2O4的浓度都瞬间减小,若是温度的改变则其中一种物质的浓度肯定比原平衡时的浓度大,与图不符;若减小体积,则2种物质的浓度都要增大,所以只能是增大容器的体积,2种物质的浓度都减小;此题中不能答减小压强,因为压强的改变有多种途径,对物质浓度的影响也不一样;
③K是温度常数,只随温度变化,K=c(N2O4)/c2(NO2),所以要使K增大则需减小NO2的浓度增大N2O4的浓度,平衡正向移动,所以采取的措施只能是降低温度,答案选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

 CO2(g)+H2(g)(ΔH>0),若温度越高,则v(CO)越大
CO2(g)+H2(g)(ΔH>0),若温度越高,则v(CO)越大
 向_________极移动。
向_________极移动。 。一定温度下,向2 L容积不变的密闭容器中充入4 mol
。一定温度下,向2 L容积不变的密闭容器中充入4 mol  和6 mo1 H2O(g)发生反应,10 min时,反应达到平衡状态,测得CH4(g)和H2(g)的物质的量随时间变化的曲线如图所示。
和6 mo1 H2O(g)发生反应,10 min时,反应达到平衡状态,测得CH4(g)和H2(g)的物质的量随时间变化的曲线如图所示。
 (CO)表示的化学反应速率为_________。
(CO)表示的化学反应速率为_________。
 Ni(CO)4(g)
Ni(CO)4(g)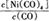 减小,则?H 0(填“>”或“<”)。
减小,则?H 0(填“>”或“<”)。
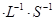 。
。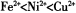 )
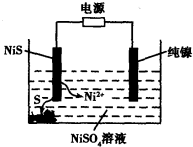
)


 。
。 4NO+6H2O,若在反应开始后5s~10s之间的反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列判断正确的关系是( )。
4NO+6H2O,若在反应开始后5s~10s之间的反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列判断正确的关系是( )。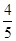 v(NH3)=v(O2)
v(NH3)=v(O2) 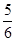 v(O2)=v(H2O)
v(O2)=v(H2O)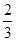 v(NH3)=v(H2O)
v(NH3)=v(H2O) 2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
2SO3(g) ΔH=-196.6 kJ·mol-1),请回答下列问题:
 2H2↑+O2↑
2H2↑+O2↑ 2H2+O2
2H2+O2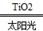 2H2↑+O2↑
2H2↑+O2↑