摘要:2.常见与铁或铜及其化合物的颜色相同或相近的物质 红 : Fe2O3 Fe(OH)3 Fe(SCN)3 Cu2O Cu NO2 Br2(g) 黄 : Fe3+ 的溶液 Na2O2 S AgI AgBr Ag3PO4 Cl2 绿 : Fe2+ 的溶液 FeSO4·7 H2O Cu2(OH)2CO3 紫 : ( Fe3+ 与苯酚作用的溶液) KMnO4 I2 黑 : Fe3O4 FeO FeS MnO2 CuO Cu2S CuS 白 : Fe(OH)2 Fe3 Mg(OH)2 BaCO3 BaSO4 AgCl 蓝 : Cu2+ 的溶液 CuSO4·5H2O
网址:http://m.1010jiajiao.com/timu3_id_341665[举报]
铁、铜及其化合物应用广泛,如FeCl3可用作印刷电路铜板腐蚀剂和外伤止血剂等;CuCl2可用作消毒剂、媒染剂、催化剂;硫酸铁可用作电化浸出黄铜矿精矿工艺。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式 ;
(2)催化剂的应用已有多年的历史,在现代化学工业中的应用十分普遍。下列物质中可以用做催化剂加速双氧水分解的是 ;
①FeCl3 ②CuCl2 ③MnO2 ④CuSO4
(3)黄铜矿精矿工艺在阳极浸出的反应比较复杂,其中有一步主要的化学反应为:CuFeS2+4Fe3+=Cu2++5Fe2++2S。(CuFeS2中S为![]() 2价)当有1mol CuFeS2参加反应时,转移的电子有 mol。
2价)当有1mol CuFeS2参加反应时,转移的电子有 mol。
(4)已知A由氧化铜和氧化亚铜混合而成。X为一种常见的酸,能使蔗糖粉末变黑。A与X反应的转化关系如下图所示,其中反应条件及部分产物均已略去。

①X的化学式为 ;
②写出B转化为D的化学方程式 ;
③X使蔗糖变黑这一现象,体现了X的 性;
④若混合物A中Cu的质量分数为85%,则混合物中氧化铜和氧化亚铜的物质的量之比为
查看习题详情和答案>>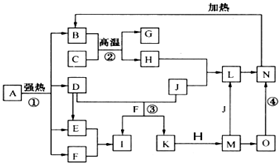 仔细阅读图,已知B、D、E、F、G是氧化物,其中D是形成酸雨的主要污染物,F、K是氢化物,且F在常温下为液态;C、H是日常生活中最为常见的金属单质,J是气态非金属单质,O是白色沉淀,且B、H、L、M、N、O中含有同种元素(图中部分反应物或产物已略去)请按要求回答:
仔细阅读图,已知B、D、E、F、G是氧化物,其中D是形成酸雨的主要污染物,F、K是氢化物,且F在常温下为液态;C、H是日常生活中最为常见的金属单质,J是气态非金属单质,O是白色沉淀,且B、H、L、M、N、O中含有同种元素(图中部分反应物或产物已略去)请按要求回答:(1)反应①既是分解反应,又是氧化还原反应,产物B、D、E、F的物质的量之比1:1:1:14.A强热分解的化学反应方程式为
2FeSO4?7H2O
Fe2O3+SO2↑+SO3↑+14H2O
| ||
. |
2FeSO4?7H2O
Fe2O3+SO2↑+SO3↑+14H2O
.
| ||
. |
(2)写出反应②在工业生产上的一种用途:
焊接钢轨
焊接钢轨
.(3)反应③的离子方程式为
Cl2+SO2+2H2O═4H++SO42-+2Cl-
Cl2+SO2+2H2O═4H++SO42-+2Cl-
;反应④的化学方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3
4Fe(OH)2+O2+2H2O═4Fe(OH)3
.(4)常以C或H制成容器盛装和运输I的浓溶液,其原理是
冷的浓硫酸与铁或铝制容器接触时,在表面生成一层致密的氧化膜,阻止金属继续与酸反应而使金属“钝化”,所以可用铁或铝制容器储运浓硫酸
冷的浓硫酸与铁或铝制容器接触时,在表面生成一层致密的氧化膜,阻止金属继续与酸反应而使金属“钝化”,所以可用铁或铝制容器储运浓硫酸
.铁、铜及其化合物在生活、生产中有广泛应用.请回答下列问题:
(1)黄铁矿(FeS2,其中S为-1价)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为3FeS2+8O2
6SO2+Fe3O4,氧化产物为
(2)与明矾相似,硫酸铁也可用作净水剂.某自来水厂用氯气和绿矾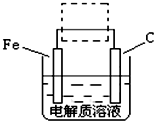 (FeSO4?7H2O)一起净水,其原理为
(FeSO4?7H2O)一起净水,其原理为
(3)①钢铁的电化腐蚀简单示意图如右,将该图稍作修改 即可成为钢铁电化学防护的简单示意图,请在右图虚线框内作出修改,并用箭头标出电子流动方向.
②写出修改前的钢铁吸氧腐蚀石墨电极的电极反应式
(4)高铁酸钾(K2FeO4)可用作净水剂,也可用于制造高铁电池.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为
3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
该电池放电时正极反应式为
用该电池电解100mL 1mol?L-1的AgNO3溶液,当电路中通过0.1mol 电子时,被电解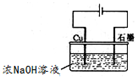 溶液的pH为
溶液的pH为
(5)氧化亚铜是一种半导体材料,常用作制造整流器的材料,还可以用于光照条件下水分解的催化剂和农作物的杀菌剂.
用右图装置可制得氧化亚铜,试写出阳极的电极反应式
查看习题详情和答案>>
(1)黄铁矿(FeS2,其中S为-1价)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为3FeS2+8O2
| ||
SO2、Fe3O4
SO2、Fe3O4
,若有3mol FeS2参加反应,转移电子的物质的量为32mol
32mol
.(2)与明矾相似,硫酸铁也可用作净水剂.某自来水厂用氯气和绿矾
 (FeSO4?7H2O)一起净水,其原理为
(FeSO4?7H2O)一起净水,其原理为Cl2+2Fe2+=2Fe3++2Cl-
Fe3++3H2O?Fe(OH)3(胶体)+3H+
Fe3++3H2O?Fe(OH)3(胶体)+3H+
Cl2+2Fe2+=2Fe3++2Cl-
Fe3++3H2O?Fe(OH)3(胶体)+3H+
(用离子方程式表示).Fe3++3H2O?Fe(OH)3(胶体)+3H+
(3)①钢铁的电化腐蚀简单示意图如右,将该图稍作修改 即可成为钢铁电化学防护的简单示意图,请在右图虚线框内作出修改,并用箭头标出电子流动方向.
②写出修改前的钢铁吸氧腐蚀石墨电极的电极反应式
O2+2H2O+4e-=4OH-,
O2+2H2O+4e-=4OH-,
.(4)高铁酸钾(K2FeO4)可用作净水剂,也可用于制造高铁电池.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为
3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH该电池放电时正极反应式为
2FeO42-+8H2O+6e-=2Fe(OH)3+10OH-
2FeO42-+8H2O+6e-=2Fe(OH)3+10OH-
.用该电池电解100mL 1mol?L-1的AgNO3溶液,当电路中通过0.1mol 电子时,被电解
 溶液的pH为
溶液的pH为0
0
(溶液体积变化忽略不计).(5)氧化亚铜是一种半导体材料,常用作制造整流器的材料,还可以用于光照条件下水分解的催化剂和农作物的杀菌剂.
用右图装置可制得氧化亚铜,试写出阳极的电极反应式
2Cu-2e-+2OH-=Cu2O+H2O
2Cu-2e-+2OH-=Cu2O+H2O
. 某同学欲探究浓硫酸、稀硫酸、浓硝酸、稀硝酸分别与铁、铜反应的实验中的有关问题.
某同学欲探究浓硫酸、稀硫酸、浓硝酸、稀硝酸分别与铁、铜反应的实验中的有关问题.(1)在常温下,分别向盛有等量铁片的四支试管中加入等体积的①浓硫酸 ②稀硫酸 ③浓硝酸 ④稀硝酸,能观察到发生明显反应的是
(2)分别向盛有等量铜片的四支试管中加入等体积的①浓硫酸 ②稀硫酸 ③浓硝酸 ④稀硝酸,能观察到随即发生剧烈反应的是
a.通入X气体后先产生白色沉淀后溶解
b.通入X气体后溶液中无明显现象
c.通入Y气体后有沉淀产生
d.通入Y气体后沉淀溶解
e.通入Y气体后溶液中无明显现象
(3)若将(2)的Ba(OH)2换为氢硫酸,则通入X气体后的现象为