摘要:4.★下列转化需加入氧化剂才能实现的是 A CI2→CIO- B NH3→NO C I2→I- D NO2→HNO3 点燃 5.★★下列各种表示形式正确的是 △ A 碳燃烧生成二氧化碳 C + O2 = CO2 B结晶硫酸铜风化 CuSO4·5H2O = CuSO4 + 5H2O C 过氧化钠与二氧化碳反应 2Na2O2 + 2CO2 = 2Na2CO3 + O2↑ D 碳酸钠溶液水解 Na2CO3 + H2O = NaHCO3 + NaOH
网址:http://m.1010jiajiao.com/timu3_id_341248[举报]
[选修2-化学与技术]
三氧化二镍(Ni2O3)是一种重要的电子元件材料和蓄电池材料.工业上利用含镍废料(镍、铁、钙、镁合金为主)制取草酸镍(NiC2O4?2H2O),再高温煅烧草酸镍制取三氧化二镍.已知草酸的钙、镁、镍盐均难溶于水.根据工艺流程示意图回答问题.

(1)操作1为 ;
(2)生产过程中多次进行过滤,实验室进行过滤操作中需用到玻璃棒,下列实验操作中,玻璃棒的作用完全相同的是 (填选项字母);
①配制0.1mol/L的H2SO4溶液
②测定Na2CO3溶液的pH
③用KI淀粉试纸检验溶液中氧化性离子
④加热食盐溶液制备NaCl晶体
⑤配制20%的KNO3溶液
A.①⑤B.②③C.④⑤D.①④
(3)加入H2O2发生的主要反应的离子方程式为 ;加入Na2CO3溶液调pH至4.0?4.5,其目的为 ;加入NH4F后除掉的杂质是 ;
(4)草酸镍(NiC2O4?2H2O)在热空气中干燥脱水后在高温下煅烧三小时,制得Ni2O3,同时获得混合气体.草酸镍受热分解的化学方程式为 ;
(5)工业上还可用电解法制取Ni2O3.用NaOH溶液调节NiCl2溶液的pH至7.5,加入适量Na2SO4后采用惰性电极电解.电解过程中产生的Cl2有80%在弱碱性条件下生成ClO-,再把二价镍氧化为三价镍.ClO-氧化Ni(OH)2生成Ni2O3的离子方程式为 .a mol二价镍全部转化为三价镍时,外电路中通过电子的物质的量为 ;
(6)电解法制取Ni2O3的实际过程中,有时获得一种结晶水合物,巳知含1mol Ni的该物质中含有0.5mol结晶水.取该化合物20.2g进行充分加热,获得Ni2O3固体和0.2mol水,则该结晶水合物的化学式为 .
查看习题详情和答案>>
三氧化二镍(Ni2O3)是一种重要的电子元件材料和蓄电池材料.工业上利用含镍废料(镍、铁、钙、镁合金为主)制取草酸镍(NiC2O4?2H2O),再高温煅烧草酸镍制取三氧化二镍.已知草酸的钙、镁、镍盐均难溶于水.根据工艺流程示意图回答问题.

(1)操作1为
(2)生产过程中多次进行过滤,实验室进行过滤操作中需用到玻璃棒,下列实验操作中,玻璃棒的作用完全相同的是
①配制0.1mol/L的H2SO4溶液
②测定Na2CO3溶液的pH
③用KI淀粉试纸检验溶液中氧化性离子
④加热食盐溶液制备NaCl晶体
⑤配制20%的KNO3溶液
A.①⑤B.②③C.④⑤D.①④
(3)加入H2O2发生的主要反应的离子方程式为
(4)草酸镍(NiC2O4?2H2O)在热空气中干燥脱水后在高温下煅烧三小时,制得Ni2O3,同时获得混合气体.草酸镍受热分解的化学方程式为
(5)工业上还可用电解法制取Ni2O3.用NaOH溶液调节NiCl2溶液的pH至7.5,加入适量Na2SO4后采用惰性电极电解.电解过程中产生的Cl2有80%在弱碱性条件下生成ClO-,再把二价镍氧化为三价镍.ClO-氧化Ni(OH)2生成Ni2O3的离子方程式为
(6)电解法制取Ni2O3的实际过程中,有时获得一种结晶水合物,巳知含1mol Ni的该物质中含有0.5mol结晶水.取该化合物20.2g进行充分加热,获得Ni2O3固体和0.2mol水,则该结晶水合物的化学式为
 (1)食品和药品关系人的生存和健康.
(1)食品和药品关系人的生存和健康.①市场上销售的食盐品种很多.下列食盐中,所添加的元素不属于人体必需微量元素的是
A
A
(填字母).A.加钙盐 B.加碘盐 C.加锌盐
②碳酸镁可治疗胃酸过多的原理是
MgCO3+2H+=Mg2++CO2↑+H2O
MgCO3+2H+=Mg2++CO2↑+H2O
(用离子方程表示).③阿司匹林具有
解热镇痛
解热镇痛
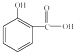
作用.长期大量服用阿司匹林,其水解产物水杨酸可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解.写出水杨酸与小苏打反应的化学方程式:

(2)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活.
①在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其各成分金属的熔点
低
低
(选填“高”或“低”).②炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑.铁锅的腐蚀主要是由
电化学腐蚀
电化学腐蚀
(填“化学腐蚀”或“电化学腐蚀”)造成的,铁锅锈蚀的负极电极反应式为Fe-2e-═Fe2+
Fe-2e-═Fe2+
.③玻璃是一种常用的硅酸盐材料.制备普通玻璃的原料有CaCO3、
Na2CO3
Na2CO3
(填化学式)和SiO2.(3)防治环境污染,改善生态环境已成为全球的共识.
①pH<5.6的雨水称为酸雨,主要是由人为排放的硫氧化物和
氮氧化物
氮氧化物
等酸性气体转化而成的.向煤中加入石灰石作为脱硫剂,可以减少煤燃烧时产生的SO2.发生反应的化学方程式为2CaCO3+O2+2SO2
2CaSO4+2CO2
| ||
2CaCO3+O2+2SO2
2CaSO4+2CO2
.
| ||
②城市餐饮业会产生大量污染环境的“地沟油”.综合利用“地沟油”的一种方法是将“地沟油”中的油脂水解以获取甘油和
高级脂肪酸
高级脂肪酸
.生活中会产生大量废弃塑料,将废弃塑料进行裂解
裂解
处理,可以获得乙烯、丙烯等化工原料.③含铬元素的废水必须治理达标.某兴趣小组探究含铬(Cr2O72ˉ)废水的处理方法,经查阅资料,拟采用(NH4)2Fe(SO4)2将Cr2O72ˉ还原为Cr3+,再用氨水将Cr3+转变成难溶的Cr(OH)3.该方案运用了污水处理方法中的氧化还原法和
沉淀法
沉淀法
.指导老师指出该方案处理后的废水中因含有大量NH4+
NH4+
(填离子符号),能导致水体富营养化.(2011?南开区二模)Ⅰ.高炉炼铁过程中发生的主要反应为:
Fe2O3(s)+CO(g)?
Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
请回答以下问题:
(1)该反应的平衡常数表达式K=
,△H=
(2)在体积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡,该时间范围内反应的平均反应速度v(CO2)=
Ⅱ.在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质.
(1)某厂废水中含KCN,其浓度为650mg/L.现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2═KOCN+2KCl+H2O,则被氧化的元素是
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:
(3)若处理上述废水20L,使KCN完全转化为无毒物质,至少需液氯
查看习题详情和答案>>
| 1 |
| 3 |
| 2 |
| 3 |
已知该反应在不同温度下的平衡常数如下:
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
(1)该反应的平衡常数表达式K=
| c(CO2) |
| c(CO) |
| c(CO2) |
| c(CO) |
<
<
0(填“>”、“<”或“=”).(2)在体积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡,该时间范围内反应的平均反应速度v(CO2)=
0.006mol/(L?min)
0.006mol/(L?min)
,CO的平衡转化率为60%
60%
.Ⅱ.在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质.
(1)某厂废水中含KCN,其浓度为650mg/L.现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2═KOCN+2KCl+H2O,则被氧化的元素是
C
C
.(2)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:
2
2
KOCN+4
4
KOH+3
3
Cl2═2
2
CO2+1
1
N2+6
6
KCl+2
2
H2O(3)若处理上述废水20L,使KCN完全转化为无毒物质,至少需液氯
35.5
35.5
g.
A.《化学与生活》
(1)南京“青奥会”已进入倒计时,体育场馆和城市交通建设日臻完善.
①体育场馆建设需大量建筑材料.下列材料不属于硅酸盐材料的是 (填字母).
a.石灰石 b.水泥 c.玻璃
②轨道交通建设需大量金属材料.下列金属材料最易发生腐蚀的是 (填字母).
a.铝合金 b.钢铁 c.纯铜
③“塑胶”跑道是由聚氨酯橡胶等材料建成.聚氨酯橡胶属于 (填字母).
a.金属材料 b.无机非金属材料 c.有机高分子材料
(2)“青奥会”期间,要保障运动员的营养与健康.
①及时补充体能是运动员取得优秀成绩的基本保证.六大基本营养素中能在人体内氧化供能的有糖类、 和 .
②水果和蔬菜富含VC.已知VC的结构为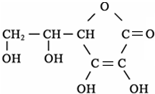 ,其分子式为
,其分子式为
;在氯化铁溶液中加入VC溶液后,溶液由黄色转变为浅绿色,说明VC具有较强的 性.
③服用违禁药物不仅妨碍体育竞技的公平、公正,也有害运动员的身心健康.在阿斯匹林、青霉素、麻黄素、小苏打等常用药物中,参赛选手不可服用的是 .
(3)“绿水蓝天”工程为运动员提供优良环境,向世界展示古都南京的美好形象.
①PM2.5指悬浮于大气中的直径≤2.5μm(微米)的颗粒物,大量PM2.5会造成灰霾天气,危害人体健康.燃煤气化有助于控制PM2.5的含量,写出焦炭与水蒸气反应的化学方程式 .
②汽车尾气中含有污染大气的NO和CO.给汽车排气管加装“催化转化器”,可使CO和NO反应生成无毒无污染的气体,反应的化学方程式为 .装有“催化转化器”的汽车必须使用无铅汽油,其原因是 .
③含铬元素的废水必须治理达标.某兴趣小组探究含铬(Cr2O72ˉ)废水的处理方法,经查阅资料,拟采用(NH4)2Fe(SO4)2将Cr2O72ˉ还原为Cr3+,再用氨水将Cr3+转变成难溶的Cr(OH)3.该方案运用了污水处理方法中的氧化还原法和 .指导老师指出该方案处理后的废水中因含有大量 (填离子符号),能导致水体富营养化.
查看习题详情和答案>>
(1)南京“青奥会”已进入倒计时,体育场馆和城市交通建设日臻完善.
①体育场馆建设需大量建筑材料.下列材料不属于硅酸盐材料的是
a.石灰石 b.水泥 c.玻璃
②轨道交通建设需大量金属材料.下列金属材料最易发生腐蚀的是
a.铝合金 b.钢铁 c.纯铜
③“塑胶”跑道是由聚氨酯橡胶等材料建成.聚氨酯橡胶属于
a.金属材料 b.无机非金属材料 c.有机高分子材料
(2)“青奥会”期间,要保障运动员的营养与健康.
①及时补充体能是运动员取得优秀成绩的基本保证.六大基本营养素中能在人体内氧化供能的有糖类、
②水果和蔬菜富含VC.已知VC的结构为
 ,其分子式为
,其分子式为③服用违禁药物不仅妨碍体育竞技的公平、公正,也有害运动员的身心健康.在阿斯匹林、青霉素、麻黄素、小苏打等常用药物中,参赛选手不可服用的是
(3)“绿水蓝天”工程为运动员提供优良环境,向世界展示古都南京的美好形象.
①PM2.5指悬浮于大气中的直径≤2.5μm(微米)的颗粒物,大量PM2.5会造成灰霾天气,危害人体健康.燃煤气化有助于控制PM2.5的含量,写出焦炭与水蒸气反应的化学方程式
②汽车尾气中含有污染大气的NO和CO.给汽车排气管加装“催化转化器”,可使CO和NO反应生成无毒无污染的气体,反应的化学方程式为
③含铬元素的废水必须治理达标.某兴趣小组探究含铬(Cr2O72ˉ)废水的处理方法,经查阅资料,拟采用(NH4)2Fe(SO4)2将Cr2O72ˉ还原为Cr3+,再用氨水将Cr3+转变成难溶的Cr(OH)3.该方案运用了污水处理方法中的氧化还原法和
