摘要:阳离子检验 离子 使用试剂 必须进行的操作 化学反应方程式 现象 H+ 石芯试液 将石芯试液滴入被测试液 溶液变红 K+ 用铂丝或光亮的铁丝蘸取试液.在无色灯焰上灼烧 焰色反应 隔蓝色的钴玻璃观察.火焰呈紫色 Mg2+ NaOH溶液NH4Cl溶液 取试液加入NaOH溶液即有白色沉淀.加过量的NaOH溶液沉淀不溶(与Al3+区别).但加NH4Cl 溶液沉淀溶解 2OH―+Mg2+ =Mg(OH)2 有白色沉淀生成.加NH4Cl 沉淀溶解 Al3+ NaOH溶液HCl溶液 在试液中逐滴加入NaOH 溶液.在产生的沉淀中HCl 或过量NaOH溶液.沉淀均溶解 Al3++3OH―=Al(OH)3 Al(OH)3+3H+=Al3++3H2O Al(OH)3+OH-=AlO2―+2H2O 有白色絮状沉淀生成.溶于HCl溶液或过量NaOH.不溶于水. Fe2+ ①NaOH溶液 ②KSCN溶液 ①在试液中加入少量NaOH溶液②在试液中加入少量KSCN溶液.振荡观察.然后加入少量新配的氯水 ①Fe2++2OH―=Fe(OH)2 4Fe(OH)2+O2+2H2O=4Fe(OH)3 ②2Fe2++Cl2=2Fe3++2Cl― Fe3++SCN-=[Fe(SCN)]2+ ①先生成白色沉淀.很快变为灰绿色.最后变为红褐色②KSCN溶液不变色.加氯水后变红色. Ag+ 稀HCl .HNO3 . 氨水 在试液中先加少量稀盐酸.再加硝酸.再加氨水 Ag++Cl―=AgCl AgCl+2NH3·H2O = [Ag(NH3)2 ]+ +2H2O + Cl― 生成白色沉淀.不溶于稀硝酸.但溶于氨水. NH4+ NaOH溶液.红色的石芯试纸 在烧杯中加少量试液.加NaOH溶液.表面皿内贴一条湿润的红色石芯试纸.反盖在烧杯上.微热 NH4++OH― = NH3↑ + H2O 有刺激性气体放出.使湿润的红色石芯试纸变蓝.
网址:http://m.1010jiajiao.com/timu3_id_340969[举报]
钼是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强合金的强度、硬度、可焊性及韧性,还可增强其耐高温强度及耐腐蚀性能.如图1所示是化工生产中制备金属钼的实验流程图:
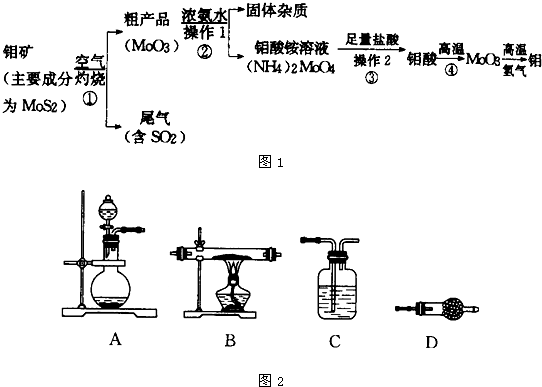
(1)钼酸铵溶液中的阳离子检验方法: .
(2)写出反应①的化学方程式. .
(3)反应①的尾气可以NH3?H2O溶液吸收合成肥料,写出反应的离子方程式 .
(4)操作1中使用的主要玻璃仪器有 .
(5)某同学利用如图2所示装置来制备氢气,利用氢气还原三氧化钼,根据要求回答问题.
①请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是 .
②在烧瓶A中加入少量的硫酸铜目的是 .
②两次使用D装置,其中所盛的药品依次是 、 .
查看习题详情和答案>>

(1)钼酸铵溶液中的阳离子检验方法:
(2)写出反应①的化学方程式.
(3)反应①的尾气可以NH3?H2O溶液吸收合成肥料,写出反应的离子方程式
(4)操作1中使用的主要玻璃仪器有
(5)某同学利用如图2所示装置来制备氢气,利用氢气还原三氧化钼,根据要求回答问题.
①请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是
②在烧瓶A中加入少量的硫酸铜目的是
②两次使用D装置,其中所盛的药品依次是
A、B、C、D、E是中学化学中五种常见元素,有关信息如下:
请回答下列问题:
(1)A的氢化物分子的电子式是
 ,其水溶液能使酚酞变红的原因用电离方程式解释为:
,其水溶液能使酚酞变红的原因用电离方程式解释为:
(2)A、D的氢化物相互反应,产生白色固体,对该固体中阳离子存在检验的操作方法是:
(3)B、C组成的某种化合物和B的某种氢化物反应可生成B的单质,则B、C组成的该化合物所含有的化学键为
(4)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(5)E制品通常在潮湿空气中发生电化学腐蚀,该过程的正极反应式为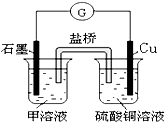
(6)若在D与E组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图所示,其反应中正极出现的现象是
查看习题详情和答案>>
| 元素 | 有关信息 |
| A | 最高价氧化物对应的水化物与其氢化物反应生成离子化合物 |
| B | 地壳中含量最多的元素 |
| C | 单质须保存在煤油中 |
| D | 单质与NaOH溶液反应可用于生产漂白液 |
| E | 单质是生活中用量最大的金属,其制品在潮湿空气中易被腐蚀或损坏 |
(1)A的氢化物分子的电子式是


NH3?H2O  NH4++OH-
NH4++OH-
 NH4++OH-
NH4++OH-NH3?H2O  NH4++OH-
NH4++OH-
. NH4++OH-
NH4++OH-(2)A、D的氢化物相互反应,产生白色固体,对该固体中阳离子存在检验的操作方法是:
取该白色固体少许于试管中,加入适量浓NaOH溶液并加热,用湿润的红色石蕊试纸接近试管口检验放出的气体,若试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生)
取该白色固体少许于试管中,加入适量浓NaOH溶液并加热,用湿润的红色石蕊试纸接近试管口检验放出的气体,若试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生)
,证明存在该阳离子.(3)B、C组成的某种化合物和B的某种氢化物反应可生成B的单质,则B、C组成的该化合物所含有的化学键为
离子键和共价键
离子键和共价键
.(4)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:
①③
①③
.①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(5)E制品通常在潮湿空气中发生电化学腐蚀,该过程的正极反应式为
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.
(6)若在D与E组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图所示,其反应中正极出现的现象是
黄色溶液慢慢变为浅绿色
黄色溶液慢慢变为浅绿色
,负极的反应式为:Cu-2e-=Cu2+
Cu-2e-=Cu2+
.
工业上常用铬铁矿(有效成份为FeO?Cr2O3,主要杂质为SiO2、Al2O3)为原料生产重铬酸钾(K2Cr2O7),实验室模拟工业法用铬铁矿制重铬酸钾的主要工艺流程如图所示,涉及的主要反应是:6FeO?Cr2O3+24NaOH+7KClO3
12Na2CrO4+3Fe2O3+7KCl+12H2O,试回答下列问题:

(1)⑤中溶液金属阳离子的检验方法是 .
(2)步骤③被沉淀的离子为(填离子符号) .
(3)在反应器①中,二氧化硅与纯碱反应的化学方程式为: .
(4)烟道气中的CO2可与H2合成甲醇.CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式: .
(5)2011年云南曲靖的铬污染事件,说明含铬废渣(废水)的随意排放对人类生存环境有极大的危害.电解法是处理铬污染的一种方法,金属铁作阳极、石墨作阴极电解含Cr2O72-的酸性废水,一段时间后产生Fe(OH)3和Cr(OH)3沉淀.
①写出电解法处理废水的总反应的离子方程式 .
②已知Cr(OH)3的Ksp=6.3×10-31,若地表水铬含量最高限值是0.1mg/L,要使溶液中c(Cr3+)降到符合地表水限值,须调节溶液的c(OH-)≥ mol/L(只写计算表达式).
查看习题详情和答案>>
| ||

(1)⑤中溶液金属阳离子的检验方法是
(2)步骤③被沉淀的离子为(填离子符号)
(3)在反应器①中,二氧化硅与纯碱反应的化学方程式为:
(4)烟道气中的CO2可与H2合成甲醇.CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式:
(5)2011年云南曲靖的铬污染事件,说明含铬废渣(废水)的随意排放对人类生存环境有极大的危害.电解法是处理铬污染的一种方法,金属铁作阳极、石墨作阴极电解含Cr2O72-的酸性废水,一段时间后产生Fe(OH)3和Cr(OH)3沉淀.
①写出电解法处理废水的总反应的离子方程式
②已知Cr(OH)3的Ksp=6.3×10-31,若地表水铬含量最高限值是0.1mg/L,要使溶液中c(Cr3+)降到符合地表水限值,须调节溶液的c(OH-)≥
(2011?枣庄模拟)由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样进行下列实验(部分产物略去):
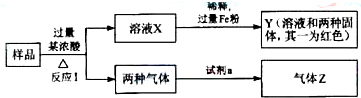
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成.取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是
(2)如何检验Y中的金属阳离子
(3)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式是
②若Z为两种气体的混合物,试剂a为适量的水,则Z中两种气体的化学式是
(4)向Y中通入过量的Cl2,并不断搅拌,充分反应后,溶液中的阳离子是
(5)取Y中的溶液,调节pH约为7,加入淀粉KI和H2O2,溶液呈蓝色并有红褐色沉淀生成.当消耗2molI-时,共转移3mol电子,该反应的离子方程式
查看习题详情和答案>>

(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成.取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是
Al
Al
.(填化学式)(2)如何检验Y中的金属阳离子
取少量Y中的溶液加入适量KSCN溶液,无明显现象,再滴入适量氯水,溶液呈血红色,则说明溶液中含有Fe2+
取少量Y中的溶液加入适量KSCN溶液,无明显现象,再滴入适量氯水,溶液呈血红色,则说明溶液中含有Fe2+
.(3)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式是
C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O
C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O
.②若Z为两种气体的混合物,试剂a为适量的水,则Z中两种气体的化学式是
NO、CO2
NO、CO2
.(4)向Y中通入过量的Cl2,并不断搅拌,充分反应后,溶液中的阳离子是
Cu2+、Fe3+、H+
Cu2+、Fe3+、H+
_.(填写离子符号)(5)取Y中的溶液,调节pH约为7,加入淀粉KI和H2O2,溶液呈蓝色并有红褐色沉淀生成.当消耗2molI-时,共转移3mol电子,该反应的离子方程式
2Fe2++4I-+3H2O2=2Fe(OH)3↓+2I2
2Fe2++4I-+3H2O2=2Fe(OH)3↓+2I2
.