摘要: 用惰性电极电解分别含有①Ag+, ②Cu2+, ③Zn2+, ④Pb2+四种阳离子的水溶液, 若析出 相同质量的金属, 则耗电量由大到小的顺序是 ④①③② ②③④①
网址:http://m.1010jiajiao.com/timu3_id_340676[举报]
X、Y、Z、Q、T五种元素位于前四周期,且原子序数依次增大.X、Y的单质在常温常压下呈气态,X形成的单质分子中无孤电子对,Y的基态原子中能级上有两个未成对电子.Z原子的半径在同周期主族元素中最大.Q的氧化物是形成酸雨的一种主要物质.T2+所含有的电子数等于Z原子与Q原子的电子数之和.
(1)Q元素位于元素周期表第 周期 族,T2+的电子排布式为 .
(2)Y元素和Q元素分别形成的组成相似的氢化物中,沸点最高的是 .(写出化学式)原因是 .用惰性电极电解X、Y、Z三种元素形成的化合物水溶液,其阳极的电极反应式为 .
(3)Z与Q形成的化合物的水溶液呈 (填“酸性”、“中性”、“碱性”)原因是 (用离子方程式表示)
(4)已知在25℃、101325Pa时:
2T(s)+Q(s)=T2Q(s)△H=-79.5KJ/mol
Q(s)+Y2(g)=QY2(g)△H=-296.6KJ/mol
根据上述反应,请写出T2Q与Y2反应生成T与QY2的热化学方程式 .
查看习题详情和答案>>
(1)Q元素位于元素周期表第
(2)Y元素和Q元素分别形成的组成相似的氢化物中,沸点最高的是
(3)Z与Q形成的化合物的水溶液呈
(4)已知在25℃、101325Pa时:
2T(s)+Q(s)=T2Q(s)△H=-79.5KJ/mol
Q(s)+Y2(g)=QY2(g)△H=-296.6KJ/mol
根据上述反应,请写出T2Q与Y2反应生成T与QY2的热化学方程式
(1)把a、b、c、d 四块金属片浸入稀H2SO4中,分别用导线两两相连可以组成原电池.a、b相连时,导线上电子由 a→b;c、d相连时,电流由 d→c; a、c相连时 c极上产生大量气泡; b、d相连时,d极发生氧化反应.这4种金属的活动性由强到弱的顺序是
(2)王同学想在钥匙上镀上一层铜,设计电解实验时,钥匙应和电源的 极相连.
(3)碳作阳极,铜作阴极电解MgCl2溶液的离子方程式: 碳作阴极,铜作阳极电解硫酸钠溶液的化学方程式:
(4)用惰性电极电解饱和食盐水,当电源供给0.2mol电子时,停止通电.若此时溶液体积为2L,则所得电解液的pH是 .(不考虑气体的溶解)
(5)将含有0.4mol Cu(NO3)2和0.4mol KCl的溶液1L,用铂电极电解一段时间后,在一个极析出0.3mol红色物质,则另一个极上放出气体(标准状况下)为 L.
查看习题详情和答案>>
(2)王同学想在钥匙上镀上一层铜,设计电解实验时,钥匙应和电源的
(3)碳作阳极,铜作阴极电解MgCl2溶液的离子方程式:
(4)用惰性电极电解饱和食盐水,当电源供给0.2mol电子时,停止通电.若此时溶液体积为2L,则所得电解液的pH是
(5)将含有0.4mol Cu(NO3)2和0.4mol KCl的溶液1L,用铂电极电解一段时间后,在一个极析出0.3mol红色物质,则另一个极上放出气体(标准状况下)为
A、B、C、D四种金属,当A、B和稀硫酸组成原电池时,电流流动方向为B-→A;将A、C分别投入等浓度的盐酸中,C比A反应剧烈;用惰性电极电解含有相同浓度的B2+、D2+的溶液时,D先在电极上析出.则A、B、C、D金属活泼性由强到弱的顺序为( )
| A、A>B>D>C | B、A>B>C>D | C、C>D>A>B | D、C>A>B>D |
下表是元素周期表的一部分,表中所列的字母分别代表一种元素.
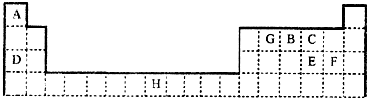
请回答下列问题:
(1)元素H位于元素周期表的 区,其原子结构示意图为 .
(2)在A、B、C、D、E、F、G送7种元素中,基态原子中未成对电子数与其所在周期数相同的元素有 种.
(3)元素D与E形成的化合物D2E的水溶液的pH≠7,原因是 (用离子方程式表示).在工业上用惰性电极电解DF的饱和溶液时,阴极的电极反应式为 .
(4)王水(浓消酸和浓盐酸以体积比1:3混合而成)可溶解不能与硝酸反应的金属如Au、Pt等,其原因是王水中不仅含有HNO3、还有反应生成的化合物BCF等,若BCF分子的所有原子都达到8电子结构,则BCF的电子式为 (用对应的元素符号表示).
(5)已知化合物H(GC)5,常温下呈液态,熔点为-20.5℃、沸点为103℃,易溶于非极性溶剂.据此可判断该化合物晶体为 .
查看习题详情和答案>>

请回答下列问题:
(1)元素H位于元素周期表的
(2)在A、B、C、D、E、F、G送7种元素中,基态原子中未成对电子数与其所在周期数相同的元素有
(3)元素D与E形成的化合物D2E的水溶液的pH≠7,原因是
(4)王水(浓消酸和浓盐酸以体积比1:3混合而成)可溶解不能与硝酸反应的金属如Au、Pt等,其原因是王水中不仅含有HNO3、还有反应生成的化合物BCF等,若BCF分子的所有原子都达到8电子结构,则BCF的电子式为
(5)已知化合物H(GC)5,常温下呈液态,熔点为-20.5℃、沸点为103℃,易溶于非极性溶剂.据此可判断该化合物晶体为