摘要:36.解答: (1)采取逆向思维 前提:在25℃时.碱的PH>7. 理由:假设当a=3,则b=6.与题意b>7矛盾. 结论:所以a不可能等于3. (2) (2)否.若a=5.[H+]a=10-5mol·L-1.则b=10.[OH-]b = 10-4mol·L‑1 .,不符合题意.故a≠5 (3) 所以<0.而a=0.5b即3a<14.a< 又pH=b=3a>7.a> 所以<a< 37C.38BC.39C.40BD.41AD. 42 >b (3)配制pH=l的HA溶液难以实现 不妥之处在于加入的锌粒难以做到表面积相同 (4)配制NaA溶液.测其pH值>7即证明HA是弱电解质 43AD.44B.
网址:http://m.1010jiajiao.com/timu3_id_339151[举报]
可以证明可逆反应N2+3H2?2NH3已达到平衡状态的是( )
①一个N≡N键断裂的同时,有6个N-H键断裂
②其它条件不变时,混合气体平均式量不再改变
③保持其它条件不变时,体系压强不再改变
④NH3%、N2%、H2%都不再改变
⑤恒温恒容时,密度保持不变
⑥正反应速率υ(H2)=0.6mol?L?min-1,逆反应速率υ(NH3)=0.4mol?L?min-1.
①一个N≡N键断裂的同时,有6个N-H键断裂
②其它条件不变时,混合气体平均式量不再改变
③保持其它条件不变时,体系压强不再改变
④NH3%、N2%、H2%都不再改变
⑤恒温恒容时,密度保持不变
⑥正反应速率υ(H2)=0.6mol?L?min-1,逆反应速率υ(NH3)=0.4mol?L?min-1.
| A、①③④⑤ | B、①②③④⑥ | C、①③⑤⑥ | D、全部 |
归纳法是髙中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结:(均在常温下)
①pH=1的强酸溶液,加水稀释后,溶液中离子浓度都降低.
②pH=2的盐酸和pH=l的盐酸,c(H+)之比为2:1
③pH相等的三种溶液:a.CH3COONa b NaHCO3 c.NaOH,其溶质物质的量浓度由小到大顺序为:c、b、a
④反应2A(s)+B (g)=2C (g)+D (g)不能自发进行,则该反应△H一定大于0
⑤已知醋酸电离平衡常数为Ka:醋酸根水解常数为Kb;水的离子积为Kw:则三者关系为:Ka?Kb=Kw
⑥反应A(g)═2B(g)△H,若正反应的活化能为Ea kJ?mol-1,逆反应的活化能 为Eb kJ?mol-1,
则△H=(Ea-EB)kJ,mol-1上述归纳正确的是( )
①pH=1的强酸溶液,加水稀释后,溶液中离子浓度都降低.
②pH=2的盐酸和pH=l的盐酸,c(H+)之比为2:1
③pH相等的三种溶液:a.CH3COONa b NaHCO3 c.NaOH,其溶质物质的量浓度由小到大顺序为:c、b、a
④反应2A(s)+B (g)=2C (g)+D (g)不能自发进行,则该反应△H一定大于0
⑤已知醋酸电离平衡常数为Ka:醋酸根水解常数为Kb;水的离子积为Kw:则三者关系为:Ka?Kb=Kw
⑥反应A(g)═2B(g)△H,若正反应的活化能为Ea kJ?mol-1,逆反应的活化能 为Eb kJ?mol-1,
则△H=(Ea-EB)kJ,mol-1上述归纳正确的是( )
| A、全部 | B、③④⑤⑥ | C、②④⑤⑥ | D、①②④⑤ |
双酚A(BPA) 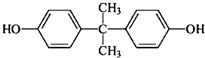 是一种重要的有机化工原料.双酚A的合成一般是在质子酸的催化下,由苯酚和丙酮缩合而成的.某中学研究性学习小组在查阅了有关文献后,拟按下列流程合成双酚A(实验中所用丙酮过量).
是一种重要的有机化工原料.双酚A的合成一般是在质子酸的催化下,由苯酚和丙酮缩合而成的.某中学研究性学习小组在查阅了有关文献后,拟按下列流程合成双酚A(实验中所用丙酮过量).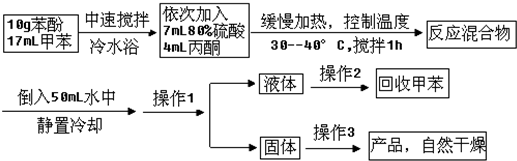
(1)控制温度在30-40℃的条件下反应,你建议的加热方式是 ;
(2)为了加快分离的速度,操作1采取的最佳方法是 ;操作2最后得到甲苯的具体操作是 ;操作3粗产品用冷水洗涤时,如何确定已经洗涤干净 ;
(3)若最后所得产品为6.06g,则双酚A的产率为 ;
(4)离子液体是绿色合成的最有效途径,具有非挥发性、较高选择性等优点,比如以(CH2CH3)3NHCl-AlCl3离子液体为催化剂,常温下合成效率可达85%.而上述常规合成,从催化剂及溶剂角度考虑会造成什么问题,请例举两条 .
查看习题详情和答案>>
 是一种重要的有机化工原料.双酚A的合成一般是在质子酸的催化下,由苯酚和丙酮缩合而成的.某中学研究性学习小组在查阅了有关文献后,拟按下列流程合成双酚A(实验中所用丙酮过量).
是一种重要的有机化工原料.双酚A的合成一般是在质子酸的催化下,由苯酚和丙酮缩合而成的.某中学研究性学习小组在查阅了有关文献后,拟按下列流程合成双酚A(实验中所用丙酮过量).
(1)控制温度在30-40℃的条件下反应,你建议的加热方式是
(2)为了加快分离的速度,操作1采取的最佳方法是
(3)若最后所得产品为6.06g,则双酚A的产率为
(4)离子液体是绿色合成的最有效途径,具有非挥发性、较高选择性等优点,比如以(CH2CH3)3NHCl-AlCl3离子液体为催化剂,常温下合成效率可达85%.而上述常规合成,从催化剂及溶剂角度考虑会造成什么问题,请例举两条