摘要:62.在0.100mol/L Na(NH4)2PO4溶液中.正确的关系式为 A [Na+]+[NH4+]+[NH3]=[H3PO4]+[H2PO4-]+[HPO42-]+[PO43-] B [H+]+[Na+]+[NH4+]=[OH-]+[H2PO4-]+[HPO42-]+[PO43-] C [H+]+3[H3PO4]+2[H2PO4-]+[HPO42-]=[OH-]+[NH3] D [H3PO4]+[H2PO4-]+2[HPO42-]+3[PO43-]=0.100mol/L
网址:http://m.1010jiajiao.com/timu3_id_339132[举报]
 在温度为373K时,将0.100mol无色的N2O4气体放入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4?2NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
在温度为373K时,将0.100mol无色的N2O4气体放入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4?2NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)(1)计算在20至40秒时间内,NO2的平均生成速率为
0.002
0.002
mol?L-1?S-1.(2)该反应的化学平衡常数表达式为
K=
| c2(NO2) |
| c(N2O4) |
K=
.| c2(NO2) |
| c(N2O4) |
氨气是一种重要的基础化工原料,用途广泛.
在微电子工业中,氨水可作刻蚀剂H2O2 的清除剂,产物不污染环境.该反应的化学方程式为2NH3+3H2O2═
工业中常用以下反应合成氨:N2+3H2?2NH3△H<0.某实验室在三个不同条件的密闭容器中,分别加入浓度均为c(N2)=0.100mol/L,c(H2)=0.300mol/L进行反应时,N2的浓度随时间的变化如下图①、②、③曲线所示.
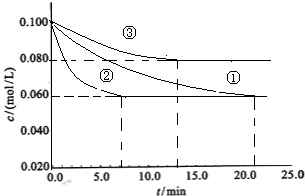
(1)该反应平衡常数的数学表达式
;实验②平衡时H2的转化率为
(2)据图所示,②、③两装置中各有一个条件与①不同.请指出,并说明判断的理由.
②条件:
③条件:
查看习题详情和答案>>
在微电子工业中,氨水可作刻蚀剂H2O2 的清除剂,产物不污染环境.该反应的化学方程式为2NH3+3H2O2═
N2
N2
+6H2O工业中常用以下反应合成氨:N2+3H2?2NH3△H<0.某实验室在三个不同条件的密闭容器中,分别加入浓度均为c(N2)=0.100mol/L,c(H2)=0.300mol/L进行反应时,N2的浓度随时间的变化如下图①、②、③曲线所示.

(1)该反应平衡常数的数学表达式
| c2(NH3)平衡 |
| c(N2)平衡c3(H2)平衡 |
| c2(NH3)平衡 |
| c(N2)平衡c3(H2)平衡 |
40%
40%
(2)据图所示,②、③两装置中各有一个条件与①不同.请指出,并说明判断的理由.
②条件:
加了催化剂
加了催化剂
理由:因为加入催化剂能缩短达到平衡的时间,但化学平衡不移动所以①②两装置达到平衡时N2的浓度相同.
因为加入催化剂能缩短达到平衡的时间,但化学平衡不移动所以①②两装置达到平衡时N2的浓度相同.
③条件:
温度升高
温度升高
理由:该反应为放热反应,温度升高,达到平衡的时间缩短,但平衡向逆反应方向移动,③中到达平衡时N2的浓度高于①
该反应为放热反应,温度升高,达到平衡的时间缩短,但平衡向逆反应方向移动,③中到达平衡时N2的浓度高于①
.(1)室温下,在pH=12的某种溶液中,由水电离的c(OH-)为 .
(2)等体积的下列溶液中,阳离子的总物质的量最大的是 .
①0.2mol?L-1的CuSO4溶液
②0.1mol?L-1的Na2CO3
③0.2mol?L-1的KCl
④0.1mol?L-1的Na2SO4
(3)浓度为0.100mol?L-1的下列各物质的溶液中,c(NH4+)由大到小的顺序是 (填序号).
①NH4Cl ②NH4HSO4 ③NH3?H2O ④CH3COONH4
(4)某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A═H++HA-,HA-?H++A2-.
①则Na2A溶液显 (填“酸性”“中性”或“碱性”),理由是 (用离子方程式表示).
②若有0.1mol?L-1 Na2A的溶液,其中各种离子浓度由大到小的顺序是: (填序号).
A.c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+)
B.c(Na+)>c(OH-)>c(HA-)>c(A2-)>c(H+)
C.c(Na+)>c(H+)>c(A2-)>c(OH-)>c(HA-)
D.c(A2-)>c(Na+)>c(OH-)>c(H+)>c(HA-)
查看习题详情和答案>>
(2)等体积的下列溶液中,阳离子的总物质的量最大的是
①0.2mol?L-1的CuSO4溶液
②0.1mol?L-1的Na2CO3
③0.2mol?L-1的KCl
④0.1mol?L-1的Na2SO4
(3)浓度为0.100mol?L-1的下列各物质的溶液中,c(NH4+)由大到小的顺序是
①NH4Cl ②NH4HSO4 ③NH3?H2O ④CH3COONH4
(4)某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A═H++HA-,HA-?H++A2-.
①则Na2A溶液显
②若有0.1mol?L-1 Na2A的溶液,其中各种离子浓度由大到小的顺序是:
A.c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+)
B.c(Na+)>c(OH-)>c(HA-)>c(A2-)>c(H+)
C.c(Na+)>c(H+)>c(A2-)>c(OH-)>c(HA-)
D.c(A2-)>c(Na+)>c(OH-)>c(H+)>c(HA-)
 在温度为373K时,将0.100mol无色的N2O4气体放入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4
在温度为373K时,将0.100mol无色的N2O4气体放入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4  2NO2的平衡.下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
2NO2的平衡.下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)(1)计算在20至40秒时间内,NO2的平均生成速率为
0.002
0.002
mol?L-1?S-1.(2)该反应的化学平衡常数表达式为K=
| C2(NO2) |
| C(N2O4) |
| C2(NO2) |
| C(N2O4) |
(3)下表是不同温度下测定得到的该反应的化学平衡常数.
| T/K | 323 | 373 |
| K值 | 0.022 | 0.36 |
吸热
吸热
反应(选填“吸热”或“放热”).