摘要:(B)下表是元素周期表的一部分.表中所列字母分别代表某一化学元素. a b d f c g i h e (1)表中属于主族金属元素的是 . (2)表中有两种元素可以组成两种不同的固体化合物.写出这两种化合物的化学式 . (3)第七周期为未完成周期.若将来的发现可把这一周期的所有元素都排满.则下列推论中可能错误的是 . A. 本周期的最后一种元素的单质在特殊情况下能转变成化合物 B. 除两种元素外.本周期的其它元素全部是放射性元素 C. 本周期第IIIA族元素的氢氧化物与Al(OH)3具有相似的化学性质 D. 本周期第VIIA族元素的原子序数为117.它是一种金属元素 (4)以下是上表中短周期非金属元素的原子半径.将相应的元素代号字母填入空格中: 元素代号 原子半径 32 64 99 70
网址:http://m.1010jiajiao.com/timu3_id_338950[举报]
下表是元素周期表的一部分,表中所列字母分别代表短周期中的一种元素.
(1)A单质的电子式是
 ;B元素在周期表中的位置是
;B元素在周期表中的位置是
(2)D单质与C的最高价氧化物对应水化物反应的离子方程式是
(3)B、C两元素分别形成的离子的半径关系:B
(4)A的气态氢化物与D的气态氢化物反应的产物是
(5)下列事实不能说明D的非金属性比A的非金属性强的是
a.D的氢化物比A的氢化物稳定
b.D的最高正化合价大于A的最高正化合价
c.D的最高价含氧酸比A的最高价含氧酸的酸性强.
查看习题详情和答案>>

(1)A单质的电子式是


第二周期第ⅥA族
第二周期第ⅥA族
.(2)D单质与C的最高价氧化物对应水化物反应的离子方程式是
Cl2+2OH-═Cl-+ClO-+H2O
Cl2+2OH-═Cl-+ClO-+H2O
.(3)B、C两元素分别形成的离子的半径关系:B
<
<
C(填“>”“=”或“<”).(4)A的气态氢化物与D的气态氢化物反应的产物是
NH4Cl
NH4Cl
,该产物中含有的化学键类型是离子键、共价键
离子键、共价键
.(5)下列事实不能说明D的非金属性比A的非金属性强的是
ac
ac
.a.D的氢化物比A的氢化物稳定
b.D的最高正化合价大于A的最高正化合价
c.D的最高价含氧酸比A的最高价含氧酸的酸性强.
下表是元素周期表的一部分,表中所列字母分别代表短周期中的一种元素:

(1)B元素在周期表中的位置是第
(2)E单质与C的最高价氧化物对应水化物反应的离子方程式是
(3)比较C、D、E的最高价氧化物对应水化物的碱性由强到弱的顺序为
(4)比较B、E、F原子半径由大到小的顺序为
查看习题详情和答案>>

(1)B元素在周期表中的位置是第
二
二
周期、第ⅥA
ⅥA
族.(2)E单质与C的最高价氧化物对应水化物反应的离子方程式是
2Al+2OH-+2H2O═2AlO2-+3H2↑
2Al+2OH-+2H2O═2AlO2-+3H2↑
.(3)比较C、D、E的最高价氧化物对应水化物的碱性由强到弱的顺序为
NaOH>Mg(OH)2>Al(OH)3
NaOH>Mg(OH)2>Al(OH)3
.(4)比较B、E、F原子半径由大到小的顺序为
Al>S>O
Al>S>O
. 下表是元素周期表的一部分,表中所列字母分别代表某一化学元素.
下表是元素周期表的一部分,表中所列字母分别代表某一化学元素.| a | b | ||||||||||||||||
| c | d | ||||||||||||||||
| e | f | g | h | i | |||||||||||||
| j | |||||||||||||||||
[Ar]3d74s2
[Ar]3d74s2
.(2)c、d原子半径大小c
>
>
d,第一电离能大小关系是c>
>
d,电负性大小关系是c<
<
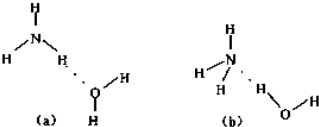
d.(以上填“>”或“<”)(3)已知NH3?H2O的电离方程式为NH3?H2O?NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是
(b)
(b)
(填序号,见图).(4)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去.核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
①原子核对核外电子的吸引力②形成稳定结构的倾向
下表是一些主族元素的气态原子失去核外不同电子所需的能量(kJ?mol-):
| 锂 | X | Y | |
| 失去第一个电子 | 519 | 502 | 580 |
| 失去第二个电子 | 7296 | 4570 | 1820 |
| 失去第三个电子 | 11799 | 6920 | 2750 |
| 失去第四个电子 | 9550 | 11600 |
Mg
Mg
、Al
Al
(填写元素符号).下表是元素周期表的一部分,表中所列字母分别代表某一化学元素.
(1)i是铁元素,其原子的最外层电子数为2,请写出铁元素的原子结构示意图
 .
.
(2)由以上元素形成的金属单质中,熔点最低的是
(3)NH3?H2O的电离方程式为NH3?H2O NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是
NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是
 (4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是
(4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是
(5)利用稀有气体化合物,人们实现了许多制备实验上的突破.如用XeO3在碱性条件下与NaBrO3反应生成NaBrO4,同时放出Xe.写出上述反应方程式:
(6)a与g形成的化合物是
查看习题详情和答案>>
| a | b | ||||||||||||||||
| c | d | ||||||||||||||||
| e | f | g | h | ||||||||||||||
| i | |||||||||||||||||
| j | |||||||||||||||||


(2)由以上元素形成的金属单质中,熔点最低的是
Na
Na
.(填元素符号)(3)NH3?H2O的电离方程式为NH3?H2O
 NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是
NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是(b)
(b)
(填序号). (4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是
(4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是j
j
(填写字母).(5)利用稀有气体化合物,人们实现了许多制备实验上的突破.如用XeO3在碱性条件下与NaBrO3反应生成NaBrO4,同时放出Xe.写出上述反应方程式:
XeO3+3NaBrO3═3NaBrO4+Xe↑
XeO3+3NaBrO3═3NaBrO4+Xe↑
.(6)a与g形成的化合物是
共价
共价
(填“离子”或“共价”)化合物.