摘要:26.两性氢氧化物 Be(OH)2+2H+=Be2++2H2O, Be(OH)2+2OH-=BeO22-+2H2O
网址:http://m.1010jiajiao.com/timu3_id_338917[举报]
A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如图所示(部分反应中的H2O已略去).
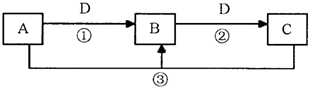
请填空:
(1)若D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式可能是
(2)若A是一种碱性气体,常用作制冷剂,B和D为空气的主要成分,则反应②的化学方程式为
(3)若D的氯碱工业的主要产品,B有两性,则反应②的离子方程式是
(4)若D为酸或酸性气体,则A、C可以是
(5)若C是一种温室气体,D是空气的主要成分之一,1mol黑色固体A完全燃烧放出393.5kJ热量,1molB气体完全燃烧放出283.0kJ热量,则A→B反应的热化学方程式为
查看习题详情和答案>>

请填空:
(1)若D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式可能是
FeCl3
FeCl3
(只写一种).用有关离子方程式解释 B溶液显酸性的原因是:氯化铁水解而使其溶液呈酸性
氯化铁水解而使其溶液呈酸性
. (2)若A是一种碱性气体,常用作制冷剂,B和D为空气的主要成分,则反应②的化学方程式为
N2+O2
2NO
| ||
N2+O2
2NO
.
| ||
(3)若D的氯碱工业的主要产品,B有两性,则反应②的离子方程式是
Al(OH)3+OH-═AlO2-+2H2O
Al(OH)3+OH-═AlO2-+2H2O
.(4)若D为酸或酸性气体,则A、C可以是
NaOH、NaHCO3或Fe、Fe(NO3)3
NaOH、NaHCO3或Fe、Fe(NO3)3
(请按顺序写出任意一组符合要求的物质的化学式)(5)若C是一种温室气体,D是空气的主要成分之一,1mol黑色固体A完全燃烧放出393.5kJ热量,1molB气体完全燃烧放出283.0kJ热量,则A→B反应的热化学方程式为
2C(s)+O2(g)═2CO(g)△H=-221kJ?mol-1
2C(s)+O2(g)═2CO(g)△H=-221kJ?mol-1
. (1)下列5种有机化合物:水杨酸(
(1)下列5种有机化合物:水杨酸( )、苯酚(
)、苯酚( )、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH).
)、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH).①其中能与Na2CO3溶液反应,但不能与FeCl3溶液发生显色反应的是
乙酸(CH3COOH)
乙酸(CH3COOH)
.②其中能与FeCl3溶液发生显色反应,但不能与NaHCO3溶液反应的是
苯酚( )
)
 )
)苯酚( )
)
. )
)③写出乙醛与银氨溶液发生银镜反应的化学方程式
CH3CHO+2Ag(NH3)2OH
2Ag+3NH3+H2O+CH3COONH4
| △ |
CH3CHO+2Ag(NH3)2OH
2Ag+3NH3+H2O+CH3COONH4
.| △ |
④写出水杨酸与金属钠反应的化学方程式


(2)①蛋白质是维持生命的重要物质,它是由氨基酸通过
肽键
肽键
连接而成的一类高分子化合物;氨基酸因分子中含有氨基和羧基,而具有两
两
性.②2008年,三鹿婴幼儿奶粉由于人为添加三聚氰胺,导致长期食用该奶粉的部分婴幼儿出现肾结石病.三聚氰胺的结构简式
 .请你预测三聚氰胺在核磁共振氢谱图(1H核磁共振谱图)中会出现
.请你预测三聚氰胺在核磁共振氢谱图(1H核磁共振谱图)中会出现1
1
个峰;三聚氰胺中氮元素的质量分数为66.7%
66.7%
(结果用百分数表示,并保留一位小数),添加三聚氰胺会使食品中蛋白质的含量虚高.(2010?济南一模)下列为元素周期表的一部分,表中阿拉伯数字(1、2…)是原周期表中行或列的序号.请参照元素A~I在表中的位置,回答下列问题.
(1)B、C两元素中非金属性较强的是
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1:1和1:2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素构成离子个数比为1:1和1:2的两种离子化合物Z和M.写出Z与Y反应的化学方程式:
(4)I元素在周期表里的位置在第
实验室中采用如图所示装置模拟工业上同时制取元素A和I的单质过程:
①写出电极C1上发生反应的电极反应式
②当电极上产生112mL(标准状况)元素I单质气体时(假设气体完全逸出,溶液体积不变),烧杯中溶液的pH=
查看习题详情和答案>>
| 纵行 | 1 | 18 | ||||||
| 横行 | ||||||||
| 1 | A | 2 | 13 | 14 | 15 | 16 | 17 | |
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | ||||
氮
氮
(写出元素名称),请设计一个简单的实验证明这一结论取碳酸钠或碳酸氢钠溶液置于试管中,向其中滴加稀硝酸,观察是否有无色无味的气体产生,HNO3+NaHCO3═NaNO3+H2O+CO2↑
或2HNO3+Na2CO3═2NaNO3+H2O+CO2↑
或2HNO3+Na2CO3═2NaNO3+H2O+CO2↑
取碳酸钠或碳酸氢钠溶液置于试管中,向其中滴加稀硝酸,观察是否有无色无味的气体产生,HNO3+NaHCO3═NaNO3+H2O+CO2↑
或2HNO3+Na2CO3═2NaNO3+H2O+CO2↑
.或2HNO3+Na2CO3═2NaNO3+H2O+CO2↑
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式
Al2O3+2OH-═2AlO2-+H2O
Al2O3+2OH-═2AlO2-+H2O
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1:1和1:2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素构成离子个数比为1:1和1:2的两种离子化合物Z和M.写出Z与Y反应的化学方程式:
2Na2O2+2H2O═4NaOH+O2↑
2Na2O2+2H2O═4NaOH+O2↑
.(4)I元素在周期表里的位置在第
三
三
周期、第VIIA
VIIA
族.
实验室中采用如图所示装置模拟工业上同时制取元素A和I的单质过程:
①写出电极C1上发生反应的电极反应式
2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
.②当电极上产生112mL(标准状况)元素I单质气体时(假设气体完全逸出,溶液体积不变),烧杯中溶液的pH=
13
13
.(KW=1.00×10-14)下表是元素周期表的一部分,回答下列问题:
(1)写出①、②两种元素的符号
(2)写出⑦、⑩两种元素的名称
(3)在这些元素中,
(4)这些元素的最高价氧化物的对应水化物中
(5)从③到⑨的元素中,
(6)比较④和⑤的化学性质
查看习题详情和答案>>
| I A | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
Be
Be
、O
O
(2)写出⑦、⑩两种元素的名称
硅
硅
、氩
氩
(3)在这些元素中,
Na
Na
(用元素符号填写,下同)是最活泼的金属元素;F
F
是最活泼的非金属元素;Ar
Ar
是最不活泼的元素.(4)这些元素的最高价氧化物的对应水化物中
HClO4
HClO4
(用化学式填写)酸性最强;NaOH
NaOH
(用化学式填写)碱性最强;能形成两性氢氧化物的元素是Al
Al
(用元素符号填写)(5)从③到⑨的元素中,
F
F
(用元素符号填写)原子半径最小.(6)比较④和⑤的化学性质
Na
Na
(用元素符号填写)更活泼,可用水
水
试剂验证.在周期表中,同一主族元素化学性质相似.目前也发现有些元素的化学性质和它在周期表中左上方或右下方的另一主族元素性质相似,这称为对角线规则.据此请回答:
(1)锂在空气中燃烧主要产物的电子式是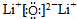
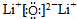 ,同时生成微量的
,同时生成微量的
(2)铍的最高价氧化物对应的水化物的化学式是
(3)若已知反应Be2C+4H2O═2Be(OH)2+CH4↑,则Al4C3遇强碱溶液反应的离子方程式为
(4)科学家证实,BeCl2属共价化合物,设计一个简单实验证明,其方法是
 .
.
查看习题详情和答案>>
(1)锂在空气中燃烧主要产物的电子式是
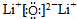
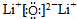
Li3N
Li3N
;(2)铍的最高价氧化物对应的水化物的化学式是
Be(OH)2
Be(OH)2
,它属两性化合物,证明这一结论的有关离子方程Be(OH)2+2H+═Be2++2H2O
Be(OH)2+2H+═Be2++2H2O
,Be(OH)2+2OH-═BeO22-+2H2O
Be(OH)2+2OH-═BeO22-+2H2O
;(3)若已知反应Be2C+4H2O═2Be(OH)2+CH4↑,则Al4C3遇强碱溶液反应的离子方程式为
Al4C3+4OH-+4H2O═4AlO2-+3CH4↑
Al4C3+4OH-+4H2O═4AlO2-+3CH4↑
;(4)科学家证实,BeCl2属共价化合物,设计一个简单实验证明,其方法是
将BeCl2加热至熔融状态,不能导电,证明BeCl2是共价化合物
将BeCl2加热至熔融状态,不能导电,证明BeCl2是共价化合物
,用电子式表示BeCl2的形成过程:
