网址:http://m.1010jiajiao.com/timu3_id_338742[举报]
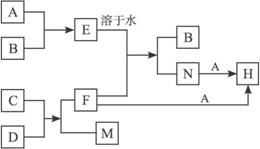
(1)写出有关反应的离子方程式:
E的水溶液+F:_______________________________________________________。
A+N:_______________________________________________________________。
M对应的氢氧化物与氢氧化钠溶液反应:_________________________________。
C+D:(写出化学方程式)______________________________________________。
(2)在足量的稀N溶液中,加入少量A的水溶液,振荡后溶液变为黄绿色。甲同学认为这不是发生化学反应所致,是A水溶液的颜色,乙同学认为这是发生化学反应所致,使溶液变黄绿色的物质是生成物和A水溶液的混合颜色。
①请你判断哪位同学的推断是正确的?_____________(填“甲”或“乙”)。
②请你设计一个实验探究你的判断(要求写出化学实验必要的操作步骤,所用化学试剂及实验现象,以及得出的化学实验结论)。
查看习题详情和答案>>A、B、C、F是中学化学常见的单质,在相同条件下,气体A的密度大于气体B的密度,D为红棕色固体。其有关转化如下:

(1)①写出A与N反应的离子方程式 。
②写出C与D反应的化学方程式 。
(2)怎样检验N溶液中的阳离子,简述实验步骤 。
(3)将H的水溶液加热蒸干并灼烧,得到的固体为 (写化学式),其有关反应的化学方程式为 。
查看习题详情和答案>>(1)D元素的名称为
(2)C、D、F的简单离子中,半径最小的是
(3)BA4的空间构型为
(4)由这六种元素形成的单质和化合物中,可以相互反应生成H2的化学方程式为
(5)下列关于甲和乙的说法中,错误的是
①乙分子中含有非极性键,一定是非极性分子
②甲的沸点较高与分子间形成氢键有关
③甲中中心原子采取sp2杂化
④乙在一定条件下可以分解生成甲
⑤甲分子中极性键的极性向量和为零.
| 3 |
| 4 |
(1)写出元素A和B形成的直线型非极性分子的电子式:


(2)已知:泡沫灭火器的工作原理是含有A、B、C、D四种元素形成的化合物X和含有C、E、F三种元素形成的Y的水溶液间的反应,写出该反应的离子方程式:
(3)工业上制备单质E,是通过电解C和E形成的化合物;写出阴极上的电极反应式:
(4)1mol由E、F两种元素组成的化合物跟由A、C、D三种元素组成的化合物的溶液恰好完全反应,则消耗后者化合物的物质的量为
(5)含有溶质为DAB2C4的水溶液显酸性的原因是
(6)若G是周期表中第四周期第Ⅷ族的金属元素,其最高价氧化物与单质E反应的化学方程式是
| ||
| ||
 A、B、C、D是短周期元素形成的四种气体单质.E、F均为气体,且F为红棕色.有关的转化关系如图所示(反应条件均已略去).
A、B、C、D是短周期元素形成的四种气体单质.E、F均为气体,且F为红棕色.有关的转化关系如图所示(反应条件均已略去).请回答下列问题:
(1)D的化学式为
(2)反应③的离子方程式为
(3)Y和E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为
(4)0.1mol?L-1的X溶液和0.1mol?L-1的Y溶液等体积混合,溶液呈
(5)常温下0.1mol?L-1的Y溶液中c(H+)/c(OH-)=1×10-8,下列叙述正确的是
A.该溶液的pH=11
B.该溶液中的溶质电离出的阳离子浓度0.1mol?L-1
C.该溶液中水电离出的c(H+)与c(OH-)乘积为1×10-22
D.pH=3的盐酸溶液V1 L与该0.1mol?L-1的Y溶液V2 L混合,若混合溶液pH=7,则:V1>V2
E.将以上溶液加水稀释100倍后,pH为9.