网址:http://m.1010jiajiao.com/timu3_id_337083[举报]
某实验小组的同学探究氢氧化铜的制法.实验记录为:

Ⅰ.猜想:同学们猜想3、4号试管中沉淀为Cu(OH)2,1、2号试管中沉淀有Cu2(OH)2SO4.
试写出生成Cu2(OH)2SO4的离子方程式________.
Ⅱ.探究:为验证1、2号试管中沉淀有SO42-,它们做了如下实验:
①操作1名称________,需要的玻璃仪器有________,
②在加稀盐酸之前应如何操作才能保证最后白色沉淀中的SO42-全部来自绿色固体________.
Ⅲ.结论:为了更好的制得氢氧化铜,下列说法合理的是________(填序号,多项选择)
A、反应应控制在常温下进行
B、反应物中氢氧化钠与硫酸铜的量应相等
C、反应物中n(NaOH)/n(CuSO4)应大于2/1
Ⅰ、有关资料
铜的化合物颜色性质如下:
| 物质 | 颜色、性质 | 物质 | 颜色、性质 |
| 氢氧化铜Cu(OH)2 | 蓝色固体不溶于水 | 硫酸铜(CuSO4) | 溶液呈蓝色 |
| 氧化亚铜(CuO) | 红色固体不溶于水 | 氯化铜(CuCl2) | 溶液呈绿色,稀溶液呈蓝色 |
| 氯化亚铜(CuCl) | 白色固体不溶于水 | 碱式氯化铜 | 绿色固体不溶于水 |
(1)提出假设:
①红色物质一定有铜,还可能有Cu2O;
②白色物质为铜的化合物,其化学式可能为CuCl.
(2)实验验证:
取电解CuCl2溶液后的阴极碳棒,洗涤、干燥,连接下列装置进行实验,验证阴极产物
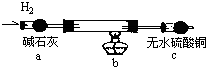
实验结束后,碳棒上的白色物质变为红色,无水硫酸铜不变色.
①碳棒上的红色物质是否有Cu2O
②在c装置后将气体通入
③写出装置b中发生反应的化学方程式:
(3)问题讨论:
①电解CuCl2溶液后的阴极上发生的反应为:Cu2++2e-=Cu和
②用石墨电极电解饱和硫酸铜溶液,观察阴极碳棒表面出现的现象红色物质附着,无白色物质,加入
Ⅰ.测定过氧化氢的含量
(1)取10.00mL密度为ρg/mL的过氧化氢溶液稀释至250mL,移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.用高锰酸钾标准溶液滴定被测试样,写出滴定过程中发生反应的离子方程式:
(2)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为
Ⅱ.探究过氧化氢的性质
(1)H2O2与铜的有关探究实验:
①将铜丝置于用硫酸酸化的H2O2溶液中,铜被迅速氧化,溶液变蓝;同时产生大量气体,经检测该气体能使余烬木条复燃,反应的离子方程式为:
②将铜丝置于H2O2溶液中,没有气泡产生,加热溶液时,观察到铜丝表面产生大量气体,且气体能使余烬木条复燃,在该变化中铜丝所起的作用是
(2)将氯气用导管通入较浓的NaOH和H2O2的混和液中,在导管口与混和液的接触处有闪烁的红光出现,这是因为通气后混和液中产生的ClO-被H2O2还原,发生激烈反应,产生能量较高的氧分子,它立即转变为普通氧分子,将多余的能量以红光放出,ClO-与H2O2反应的离子方程式是
(16分)
为探究如何尽可能多的使NO2被水吸收,某活动小组设计并完成了以下实验。
(1)活动小组同学利用铜与浓硝酸反应制取NO2、过氧化氢溶液与MnO2制取O2。
①根据反应原理他们选用了相同的装置 (填“图l”或“图2”)分别制取N22和O2。
②写出铜与浓硝酸反应的离子方程式 。
③过氧化氢溶液与MnO2制取O2时MnO2的作用是 。
④收集NO2的方法是 。
(2)活动小组的同学做了如下准备工作:用气囊收集好纯净的O2,收集了一试管NO2,
用干燥的烧瓶收集了一定比例的NO2和O2的混合气体。
①为了尽可能多的使NO2被水吸收,并达到较好的实验效果,利用图3吸收气体时,用气囊通入O2与直接利用制气装置制取并通人O2相比,其优点是 。
②利用图4吸收气体时,其操作和现象为 。
③NO2、H2O反应的产物为硝酸,反应中NO2和O2物质的量之比a:b= ;若图4中混合气体NO2和O2比例为a:b,当混合气体全部被吸收时所得溶液物质的量浓度为 mol/L(保留两位有效数字)。
查看习题详情和答案>>
(16分)
为探究如何尽可能多的使NO2被水吸收,某活动小组设计并完成了以下实验。
(1)活动小组同学利用铜与浓硝酸反应制取NO2、过氧化氢溶液与MnO2制取O2。
①根据反应原理他们选用了相同的装置 (填“图l”或“图2”)分别制取N22和O2。
②写出铜与浓硝酸反应的离子方程式 。
③过氧化氢溶液与MnO2制取O2时MnO2的作用是 。
④收集NO2的方法是 。
(2)活动小组的同学做了如下准备工作:用气囊收集好纯净的O2,收集了一试管NO2,
用干燥的烧瓶收集了一定比例的NO2和O2的混合气体。
①为了尽可能多的使NO2被水吸收,并达到较好的实验效果,利用图3吸收气体时,用气囊通入O2与直接利用制气装置制取并通人O2相比,其优点是 。
②利用图4吸收气体时,其操作和现象为 。
③NO2、H2O反应的产物为硝酸,反应中NO2和O2物质的量之比a:b= ;若图4中混合气体NO2和O2比例为a:b,当混合气体全部被吸收时所得溶液物质的量浓度为 mol/L(保留两位有效数字)。