题目内容
某实验小组的同学探究氢氧化铜的制法.实验记录为:

Ⅰ.猜想:同学们猜想3、4号试管中沉淀为Cu(OH)2,1、2号试管中沉淀有Cu2(OH)2SO4.
试写出生成Cu2(OH)2SO4的离子方程式________.
Ⅱ.探究:为验证1、2号试管中沉淀有SO42-,它们做了如下实验:
①操作1名称________,需要的玻璃仪器有________,
②在加稀盐酸之前应如何操作才能保证最后白色沉淀中的SO42-全部来自绿色固体________.
Ⅲ.结论:为了更好的制得氢氧化铜,下列说法合理的是________(填序号,多项选择)
A、反应应控制在常温下进行
B、反应物中氢氧化钠与硫酸铜的量应相等
C、反应物中n(NaOH)/n(CuSO4)应大于2/1
答案:
解析:
解析:
|
(1)Ⅰ:2Cu2++SO42-+2OH-=Cu2(OH)2SO4 Ⅱ:①过滤 漏斗、烧杯、玻璃棒 ②用蒸馏水对沉淀进行多次洗涤,取最后的洗涤液加入BaCl2,至不再产生白色沉淀 Ⅲ:AC |

练习册系列答案
相关题目

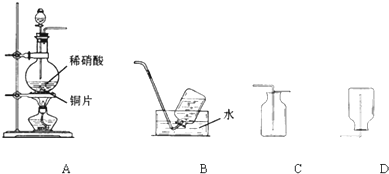
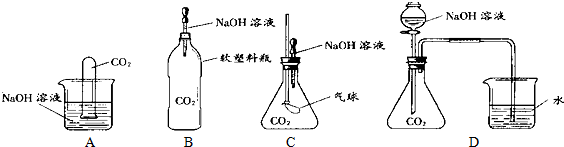
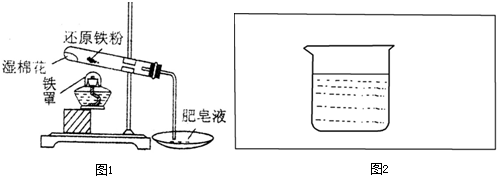
 ”表示),设计一套原电池装置,并验证有电流产生,请帮他在图2方框内补充全装置简图(要求标注正、负极及其材料和电解质溶液名称).
”表示),设计一套原电池装置,并验证有电流产生,请帮他在图2方框内补充全装置简图(要求标注正、负极及其材料和电解质溶液名称).