摘要:一定温度下CuSO4在水中的溶解度为25g.该温度下将32g CuSO4白色粉末投入mg水中形成饱和溶液.并有CuSO4·5H2O晶体析出.则m的取值为( ) A.18g≤m≤128g B. 18g<m<128g C. 36g<m<180g D. 36g≤m≤180g
网址:http://m.1010jiajiao.com/timu3_id_336386[举报]
下列实验事实与结论均正确的是( )
查看习题详情和答案>>
| A | 将0.1mol/LNaOH溶液滴到饱和FeCl3溶液中 | 可用于制备Fe(OH)3胶体 |
| B | H2O2的分解实验中,分别加入数滴的FeCl3、CuSO4溶液 | 探究不同催化剂对反应速率的影响 |
| C | 将盛满NO2的烧瓶分别浸泡在热水、冷水中,热水中看到的颜色更浅 | 说明由NO2生成N2O4是放热反应 |
| D | 一定温度下,一定浓度的草酸与KMnO4反应,颜色褪去,开始较慢后逐渐加快 | 说明反应生成的Mn2+有催化作用 |
(2010?诸城市模拟)研究化学反应对人类社会的发展进步有重要意义.
(1)已知:N2(g)+3H2(g)2NH3(g)△H1=-92.4kJ/mol
2H2(g)+O2(g)=2H2O(g)△H2=-523.6kJ/mol
H2O(g)=H2O(l)△H3=-44.0kJ/mol
根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应生成氨气,试写出此反应的热化学方程式
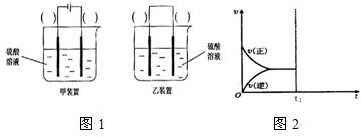
(2)现有反应:Cu+H2SO4═CuSO4+H2,欲通过如图1所示装置实现上述反应,请选择合适的装置在括
号内标出电极材料(填“Cu”或“C”),并且写出C电极上的电极反应式
(3)长期使用的锅炉需要定期除水垢,否则会降低燃料的利用率.水垢中含有的CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去.则CaSO4 转化为CaCO3的离子方程式为
(4)科学研究发现纳米级Cu2O的可作为太阳光分解水的催化剂.一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气,发生反应:2H2O(g)
2H2(g)+O2(g)△H>0,不同时段产生O2的量见下表:
则:
①该条件下上述反应的化学平衡常数K=
②若达到平衡后在t1时刻保持温度不变,将容器的体积缩小,请在图2中画出正、逆反应速率随时间变化的关系图.
查看习题详情和答案>>

(1)已知:N2(g)+3H2(g)2NH3(g)△H1=-92.4kJ/mol
2H2(g)+O2(g)=2H2O(g)△H2=-523.6kJ/mol
H2O(g)=H2O(l)△H3=-44.0kJ/mol
根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应生成氨气,试写出此反应的热化学方程式
2N2(g)+6H2O(l)=4NH3(g)+3O2(g)△H=-1650kJ/mol
2N2(g)+6H2O(l)=4NH3(g)+3O2(g)△H=-1650kJ/mol
.(2)现有反应:Cu+H2SO4═CuSO4+H2,欲通过如图1所示装置实现上述反应,请选择合适的装置在括
号内标出电极材料(填“Cu”或“C”),并且写出C电极上的电极反应式
2H++2e-→H2↑
2H++2e-→H2↑
.(3)长期使用的锅炉需要定期除水垢,否则会降低燃料的利用率.水垢中含有的CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去.则CaSO4 转化为CaCO3的离子方程式为
CaSO4(s)+CO32-(aq)=CaCO3(s)+SO42-(aq)
CaSO4(s)+CO32-(aq)=CaCO3(s)+SO42-(aq)
.(4)科学研究发现纳米级Cu2O的可作为太阳光分解水的催化剂.一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气,发生反应:2H2O(g)
| 光 |
| Cu2O |
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
①该条件下上述反应的化学平衡常数K=
1.7×10-6mol/L
1.7×10-6mol/L
;②若达到平衡后在t1时刻保持温度不变,将容器的体积缩小,请在图2中画出正、逆反应速率随时间变化的关系图.