摘要:4.早期食盐加碘在食盐中加入的化合物是碘化钾.但在使用过程中发现食盐不久会泛黄.口感变苦.有人做了这样的小实验:将泛黄的食盐放到稀饭中.稀饭变成浅蓝色.则可推断.空气中使KI变质的物质可能是:( ) A.H2O B.CO2 C.O2 D.N2
网址:http://m.1010jiajiao.com/timu3_id_335936[举报]
 (2010?四川)碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.请回答下列问题:
(2010?四川)碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.请回答下列问题:(1)碘是
紫黑色
紫黑色
(填颜色)固体物质,实验室常用升华
升华
方法来分离提纯含有少量杂质的固体碘.(2)电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:
3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区.另将氢氧化钾溶液加入阴极区,电解槽用水冷却.电解时,阳极上发生反应的电极反应式为
2I--2e-=I2
2I--2e-=I2
;阴极上观察到的实验现象是有气泡产生
有气泡产生
.(3)电解过程中,为确定电解是否完成,需检验电解液中是否有I-.请设计一个检验电解液中是否有I-的实验方案,并按要求填写下表.
要求:所需药品只能从下列试剂中选择,实验仪器及相关用品自选.
试剂:淀粉溶液、碘化钾淀粉试纸、过氧化氢溶液、稀硫酸.
| 实验方法 | 实验现象及结论 |
取少量阳极区电解液于试管中,加稀硫酸酸化后加入几滴淀粉溶液,观察是否变蓝. 取少量阳极区电解液于试管中,加稀硫酸酸化后加入几滴淀粉溶液,观察是否变蓝. |
如果不变蓝,说明无I-.(如果变蓝,说明有I-) 如果不变蓝,说明无I-.(如果变蓝,说明有I-) |

步骤②的操作名称是
冷却结晶
冷却结晶
,步骤⑤的操作名称是干燥
干燥
.步骤④洗涤晶体的目的是洗去吸附在碘酸钾晶体上的氢氧化钾等杂质
洗去吸附在碘酸钾晶体上的氢氧化钾等杂质
. 人体缺碘会导致甲状腺肿大,我国实行“食盐加碘”预防碘缺乏
人体缺碘会导致甲状腺肿大,我国实行“食盐加碘”预防碘缺乏症.如图为加碘盐的标签,下列说法正确的是( )
| A、加碘盐中的碘可直接用AgNO3溶液检验 | B、使用加碘盐勿长时间加热,因为KIO3加热易升华 | C、加碘盐中添加KIO3而不是KI,原因是在空气中前者比后者稳定 | D、IO3-+5I-+6H+=3I2+3H2O中,氧化剂和还原剂的物质的量之比为5:1 |
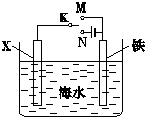 (1)利用如图装置,可以模拟铁的电化学防护.若X为碳棒,为减缓铁的腐蚀,开关K应该置于
(1)利用如图装置,可以模拟铁的电化学防护.若X为碳棒,为减缓铁的腐蚀,开关K应该置于N
N
处.若X为锌,开关K置于M处,该电化学防护法称为牺牲阳极的阴极保护法
牺牲阳极的阴极保护法
.(2)肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料.肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液.该电池放电时,通入肼的一极为
负
负
极,该极的电极反应式是N2H4+4OH--4e-=N2↑+4H2O
N2H4+4OH--4e-=N2↑+4H2O
,电池工作一段时间后,电解质溶液的pH将减小
减小
(填“增大”、“减小”、“不变”).(3)碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,可通过电解制备碘酸钾.(阴、阳两极均用惰性电极,阴极室与阳极室用阳离子交换膜隔开)请回答下列问题:
①电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I2+6KOH═5KI+KIO3+3H2O,将该溶液加入阳极区.另将氢氧化钾溶液加入阴极区,电解槽用水冷却.电解时,阳极上发生反应的电极反应式为
2I--2e-=I2
2I--2e-=I2
.②电解过程中,为确定电解是否完成,需检验电解液中是否有I-.请设计一个检验电解液中是否有I-的实验方案,并按要求填写下表.
要求:所需药品只能从下列试剂中选择,实验仪器及相关用品自选.
试剂:淀粉溶液、碘化钾淀粉试纸、过氧化氢溶液、稀硫酸.
| 实验方法 | 实验现象及结论 |