摘要:此类图象能说明各平衡体系组分在反应过程中的变化情况.如A+B 2AB反应情况如图2.此类图象要注意各物质曲线的折点时刻相同.各物质浓度变化的内在联系及比例符合化学方程式中的系数关系. 例2.在一定温度下.容器内某一反应中M.N的物质的量随反应时间变化的曲线如下图.下列表述中正确的是( ) A.反应的化学方程式为:2 MN B.t2时.正逆反应速率相等.达到平衡 C.t3时.正反应速率大于逆反应速率 D.t1时.N的浓度是M浓度的2倍 练习2.今有反应X.若反应开始经t1s后达到平衡.又经t2 s后.由于反应条件的改变使平衡破坏.到t3 s时又达到平衡.如图所示.试分析从t2到t3的曲线变化的原因是 A增大了X和Y的浓度 B.使用了催化剂 C.增加了反应体积的压强 D.升高了反应的温度
网址:http://m.1010jiajiao.com/timu3_id_334360[举报]
 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO)
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO)CO(g)+2H2(g)?CH3OH(g).
根据题意和所给图象完成下列各题:
(1)反应达到平衡时,平衡常数表达式K=
| c(CH3OH) |
| c(CO)c2(H2) |
| c(CH3OH) |
| c(CO)c2(H2) |
(2)升高温度,K值
减小
减小
(填“增大”“减小”或“不变”).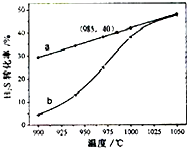 H2S受热分解的反应为:2H2S(g)→2H2(g)+S2(g).在恒温密闭容器中,控制不同温度进行 H2S分解实验.以H2S起始浓度均为cmol?L-1测定H2S的转化率,结果如图.图中a曲线为H2S 的平衡转化率与温度关系,b曲线表示不同温度下反应经过相同时间的转化率.下列叙述错误的是( )
H2S受热分解的反应为:2H2S(g)→2H2(g)+S2(g).在恒温密闭容器中,控制不同温度进行 H2S分解实验.以H2S起始浓度均为cmol?L-1测定H2S的转化率,结果如图.图中a曲线为H2S 的平衡转化率与温度关系,b曲线表示不同温度下反应经过相同时间的转化率.下列叙述错误的是( )A、985℃时,H2S按上述反应分解的平衡常数K=
| ||
| B、H2S的分解为吸热反应 | ||
| C、图象能解释,温度升高,反应速率加快 | ||
| D、如果只将上述条件中的温度改为压强,图象的形式基本不变 |
(2011?黄浦区一模)500℃时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3物质的量变化如图所示,分析图象完成下列填空:
(1)0-10分钟,N2的平均反应速率为
(2)计算500℃时,反应N2+3H2 2NH3的平衡常数K的数值为
2NH3的平衡常数K的数值为
(3)在图中画出25min-40min时间段内N2的物质的量的变化图象.
查看习题详情和答案>>

(1)0-10分钟,N2的平均反应速率为
0.0025
0.0025
mol?L-1?min-1,0-10分钟与10到20分钟两个时间段中,N2的反应速率之比为1:2
1:2
.反应在第10min可能改变的条件是加入催化剂
加入催化剂
,运用图象信息说明该条件不是升温的原因是10min时变化是连续的,三种气体物质的速率增加倍数相同
10min时变化是连续的,三种气体物质的速率增加倍数相同
.(2)计算500℃时,反应N2+3H2
 2NH3的平衡常数K的数值为
2NH3的平衡常数K的数值为426.7
426.7
.保持温度不变,反应进行至25min时,抽去0.1mol氨,此时平衡常数K将不变
不变
(填“增大”或“减小”或“不变”).保持体积不变,达到新平衡后的正反应的化学反应速率比原平衡状态小
小
(填“大”或“小”或“不变”).(3)在图中画出25min-40min时间段内N2的物质的量的变化图象.
对溶液的研究和认识,在生产、生活和科研领域具有重要意义.
(1)现有一种含有弱酸HA和其钠盐NaA的溶液,请回答下列问题:
①组成该溶液的微观粒子有 .
②若向该溶液中加入少量盐酸时,发生反应的离子方程式是 ;
③若向该溶液中逐滴加入KOH溶液时,下列图象能表示Aˉ离子数目变化趋势的是 ;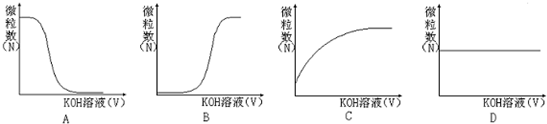
④现将1体积0.04mol?L-1HA溶液和1体积0.02mol?L-1NaOH溶液混合,得到2体积混合溶液.若该混合液显碱性,则其c(A-) 0.01mol?L-1(填“<”、“=”或“>”);若该混合液显酸性,溶液中所有离子的浓度由大到小的顺序是 .
(2)血液里含有的H2CO3和NaHCO3,与上述情况相似,对保持血液pH的稳定起到重要作用.
当c(H+)增大时,血液中消耗H+的离子方程式为 ;
当c(OH-)增大时,血液的pH也能保持基本稳定,试结合离子方程式简要说明 .
查看习题详情和答案>>
(1)现有一种含有弱酸HA和其钠盐NaA的溶液,请回答下列问题:
①组成该溶液的微观粒子有
②若向该溶液中加入少量盐酸时,发生反应的离子方程式是
③若向该溶液中逐滴加入KOH溶液时,下列图象能表示Aˉ离子数目变化趋势的是

④现将1体积0.04mol?L-1HA溶液和1体积0.02mol?L-1NaOH溶液混合,得到2体积混合溶液.若该混合液显碱性,则其c(A-)
(2)血液里含有的H2CO3和NaHCO3,与上述情况相似,对保持血液pH的稳定起到重要作用.
当c(H+)增大时,血液中消耗H+的离子方程式为
当c(OH-)增大时,血液的pH也能保持基本稳定,试结合离子方程式简要说明