摘要:已知:CH4(气)+2O2(气)=CO2(气)+2H2O(液),ΔH=-Q1, 2H2(气)+O2(气)=2H2O(气),ΔH=-Q2, 2H2(气)+O2(气)=2H2O(液),ΔH=-Q3.常温下取体积比4:1的甲烷和 氢气的混合气体11.2L.经完全燃烧后恢复至常 温.则放出的热量为 ( ) A.0.4Q1+ 0.05Q3 B. 0.4 Q1+0.05Q2 C. 0.4 Q1+ 0.1Q3 D. 0.4 Q1+0.2Q2 根据下列叙述回答4-6题 能源可划分为一级能源和二级能源.自然界中以现成形式提供的能 源称为一级能源,需依靠其他能源的能量间接制取的能源称为二级 能源.氢气是一种高效而没有污染的二级能源.它可以由自然界中 大量存在的水来制取:2H2O(液)=2H2(气)+O2(气),ΔH=+517.6kJ/mol
网址:http://m.1010jiajiao.com/timu3_id_332385[举报]
已知:CH4(气)+2O2(气)=CO2(气)+2H2O(液)+Q1;2H2(气)+O2=2H2O(气)+Q2;2H2(气)+O2(气)=2H2O(液)+Q3,常温下取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则放出的热量为( )
A.0.4Q1+0.05Q3
B.0.4Q1+0.05Q2
C.0.4Q1+0.1Q3
D.0.4Q1+0.2Q2
查看习题详情和答案>>
已知:CH4(气)+2O2(气)=CO2(气)+2H2O(液)+Q1;2H2(气)+O2=2H2O(气)+Q2;2H2(气)+O2(气)=2H2O(液)+Q3,常温下取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则放出的热量为( )
A.0.4Q1+0.05Q3
B.0.4Q1+0.05Q2
C.0.4Q1+0.1Q3
D.0.4Q1+0.2Q2
查看习题详情和答案>>
甲醇被称为21世纪的新型燃料,甲烷可制成合成气(CO、H2),再制成甲醇,
代替日益供应紧张的燃油.
(1)已知:①CH4(g)+H2O (g)=CO (g)+3H2(g)△H1=+206.2kJ?mol-1
②CH4(g)+
O2(g)=CO(g)+2H2(g)△H2=-35.4kJ?mol-1
③CH4(g)+2H2O (g)=CO2(g)+4H2(g)△H3=+165.0kJ?mol-1
CH4(g)与CO2(g)反应生成CO(g)和H2(g)的热化学方程式为 .
(2)合成气中的H2可用于生产NH3,在进入合成塔前常用Cu(NH3)2Ac溶液来吸收其中的CO,防止合成塔中的催化剂中毒,其反应是:
Cu(NH3)2Ac+CO+NH3[Cu(NH3)3]Ac?CO△H<0,Cu(NH3)2Ac溶液吸收CO的适宜生产条件应是 ,该反应的△S 0(填“>”、“=”或“<”)
(3)工业上一般采用下列两种反应合成甲醇:
反应A:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1
反应B:CO(g)+2H2(g)?CH3OH(g)△H2<0
①对于反应A,某温度下,将4mol CO2和12mol H2,充入2L的密闭容器中,充分反应达到平衡后,测得c(CO2)=0.5mol?L-1,则该温度下该反应的平衡常数
②对于反应B,若容器容积不变,下列措施可提高CO的转化率是
A.降低温度 B.增加CO的量
C.充入He,使体系总压强增大 D.再充入1mol CO和2mol H2
(4)某种甲醇-空气燃料电池是采用铂作为电极,氢氧化钾作电解质溶液.其工作时负极的电极反应式可表示为
(5)用上述碱性甲醇-空气燃料电池电解硫酸钠溶液(均为铂电极),标准状况下阳极得到VL的气体,计算消耗甲醇的质量为 g.
查看习题详情和答案>>
代替日益供应紧张的燃油.
(1)已知:①CH4(g)+H2O (g)=CO (g)+3H2(g)△H1=+206.2kJ?mol-1
②CH4(g)+
| 1 | 2 |
③CH4(g)+2H2O (g)=CO2(g)+4H2(g)△H3=+165.0kJ?mol-1
CH4(g)与CO2(g)反应生成CO(g)和H2(g)的热化学方程式为
(2)合成气中的H2可用于生产NH3,在进入合成塔前常用Cu(NH3)2Ac溶液来吸收其中的CO,防止合成塔中的催化剂中毒,其反应是:
Cu(NH3)2Ac+CO+NH3[Cu(NH3)3]Ac?CO△H<0,Cu(NH3)2Ac溶液吸收CO的适宜生产条件应是
(3)工业上一般采用下列两种反应合成甲醇:
反应A:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1
反应B:CO(g)+2H2(g)?CH3OH(g)△H2<0
①对于反应A,某温度下,将4mol CO2和12mol H2,充入2L的密闭容器中,充分反应达到平衡后,测得c(CO2)=0.5mol?L-1,则该温度下该反应的平衡常数
②对于反应B,若容器容积不变,下列措施可提高CO的转化率是
A.降低温度 B.增加CO的量
C.充入He,使体系总压强增大 D.再充入1mol CO和2mol H2
(4)某种甲醇-空气燃料电池是采用铂作为电极,氢氧化钾作电解质溶液.其工作时负极的电极反应式可表示为
(5)用上述碱性甲醇-空气燃料电池电解硫酸钠溶液(均为铂电极),标准状况下阳极得到VL的气体,计算消耗甲醇的质量为
 氮及其化合物与人们的生活息息相关.
氮及其化合物与人们的生活息息相关.(1)氮元素在周期表中的位置是
(2)实验室可用铜与稀硝酸反应制取NO,其离子方程式是
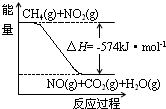
(3)已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ?mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1
根据①和②,标准状况下,4.48L CH4恰好将NO2转化为N2时,△H=
关于①和②,下列说法正确的是
a.由反应①可推知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l)△H<-574kJ?mol-1
b.等物质的量的甲烷分别发生反应①、②,转移电子数相同
c.如图可表示①的反应过程和能量关系
(4)同温同压下,3.5L NH3恰好将3.0L NO和NO2的混合气完全转化为N2,则原混合气中 NO和NO2的体积比是
 合成气(CO和H2)是重要的化工原料,在工业生产中有着广泛的应用.
合成气(CO和H2)是重要的化工原料,在工业生产中有着广泛的应用.(1)工业上用甲烷和水蒸气在高温条件下发生反应制备合成气(CO和H2),4g甲烷完全反应吸收51.5KJ热量,写该反应的热化学方程式
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206KJ/mol
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206KJ/mol
(2)已知:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802kJ?mol-1,由反应(1)制备的合成气10m3(已折成标况),完全燃烧所提供的能量为
1.125×105
1.125×105
kJ(3)工业上常用合成气来冶炼金属,其中CO还原氧化铁来冶炼生铁方程式如下:
3CO(g)+Fe2O3(s)═3CO2(g)+2Fe(s)△H<0
①如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,
AD
AD
.A.容器中Fe2O3的质量不随时间而变化 B.反应物不再转化为生成物
C.n (CO):n (CO2)=1:1 D.容器中气体的压强不随时间而变化
②在一个容积为4L的密闭容器中,1000℃时加入4mol CO(g)和足量Fe2O3(s),反应2分钟后达到平衡,测得此时容器内气体的密度为40g/L,求该时间范围内反应的平均反应速率υ(CO2)=
0.375mol/L?min
0.375mol/L?min
、CO的平衡转化率=75%
75%
、该反应的化学平衡常数K=27
27
.③如果在3分钟时向②的平衡体系中再加入2mol CO(g),其它条件不变,经过2分钟反应又达到平衡.请画出②、③c(CO)、c(CO2) 随时间变化的图象.