题目内容
已知:CH4(气)+2O2(气)=CO2(气)+2H2O(液)+Q1;2H2(气)+O2=2H2O(气)+Q2;2H2(气)+O2(气)=2H2O(液)+Q3,常温下取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则放出的热量为( )A.0.4Q1+0.05Q3
B.0.4Q1+0.05Q2
C.0.4Q1+0.1Q3
D.0.4Q1+0.2Q2
答案:A
提示:
提示:
| 11.2L混合气体中甲烷和氢气的物质的量分别等于0.4mol和0.1mol,放出的热量与反应物的物质的量成正比,0.4mol甲烷完全燃烧放出的热量等于0.4 Q1,氢气完全反应后恢复至常温生成液体水,1mol氢气反应放热0.05 Q3,正确答案是A。
|

练习册系列答案
相关题目
 合成气(CO和H2)是重要的化工原料,在工业生产中有着广泛的应用.
合成气(CO和H2)是重要的化工原料,在工业生产中有着广泛的应用.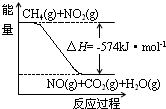 氮及其化合物与人们的生活息息相关.
氮及其化合物与人们的生活息息相关.