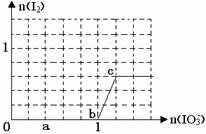
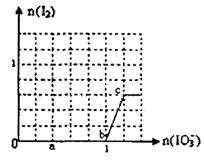
摘要:已知:还原性HSO3->I-.氧化性IO3-> I2 . (1)在NaIO3溶液中滴加少量NaHSO3溶液.发生下列反应.配平反应方程式并标出电子转移的方向和数目. 囗NaIO3+囗NaHSO3 → 囗I2+囗Na2SO4+囗H2SO4+囗H2O (2)在NaIO3溶液中滴加过量NaHSO3溶液.反应完全后.推测反应后溶液中的还原产物为 , (3)在含5molNaHSO3的溶液中逐滴加入NaIO3溶液.加入NaIO3的物质的量和析出I2单质的物质的量的关系曲线如右图所示.写出反应过程中与AB段曲线对应的离子方程式 ,当溶液中I-与I2的物质的量之比为5:3时.加入的NaIO3为 mol.
网址:http://m.1010jiajiao.com/timu3_id_328027[举报]
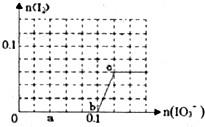 已知:还原性HSO3->I-,氧化性IO3->I2.在含0.3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法不正确的是( )
已知:还原性HSO3->I-,氧化性IO3->I2.在含0.3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法不正确的是( )| A、0~b间的反应可用如下离子方程式表示:3HSO3-+IO3-═3SO42-+I-+3H+ | B、a点时消耗NaHSO3的物质的量为0.12mol | C、当溶液中I-与I2的物质的量之比为5:2时,加入的KIO3为0.18mol | D、b点时的还原产物可能是KI或NaI,b~c间的还原产物是I2 |
(2013?闵行区一模)氧化还原反应在生产、生活中具有广泛的用途,贯穿古今.
(1)下列生产、生活中的事例中没有发生氧化还原反应的是
a.煤的形成 b.原电池工作
c.简单机械织布 d.我国古代烧制陶器
(2)水是人体的重要组成部分,是人体中含量最多的一种物质.“四种基本反应类型与氧化还原反应的关系”可用下图表示.

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:
(3)工业上利用NaIO3和NaHSO3反应来制取单质I2.配平下列化学方程式并标明电子转移的方向和数目:
(4)已知:还原性HSO3->I-,若加入的NaHSO3过量,还可能与上述生成物中的
查看习题详情和答案>>
(1)下列生产、生活中的事例中没有发生氧化还原反应的是
c
c
(选填编号).a.煤的形成 b.原电池工作
c.简单机械织布 d.我国古代烧制陶器
(2)水是人体的重要组成部分,是人体中含量最多的一种物质.“四种基本反应类型与氧化还原反应的关系”可用下图表示.

试写出有水参加的符合反应类型Ⅳ的一个化学方程式:
2F2+2H2O=4HF+O2或2Na+2H2O=2NaOH+H2↑或C+H2O
CO+H2
| ||
2F2+2H2O=4HF+O2或2Na+2H2O=2NaOH+H2↑或C+H2O
CO+H2
.
| ||
(3)工业上利用NaIO3和NaHSO3反应来制取单质I2.配平下列化学方程式并标明电子转移的方向和数目:
4
4
NaIO3+10
10
NaHSO3→2
2
I2+7
7
Na2SO4+3
3
H2SO4+2
2
H2O(4)已知:还原性HSO3->I-,若加入的NaHSO3过量,还可能与上述生成物中的
I2
I2
反应,离子方程式为H2O+I2+HSO3-=2I-+SO42-+3H+
H2O+I2+HSO3-=2I-+SO42-+3H+
.已知:还原性HSO3¯>I¯,氧化性IO3¯> I2 。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。
下列说法正确的是

A.反应过程中的氧化产物均为SO3
B.a点时剩余NaHSO3的物质的量为1.2 mol
C.b点时的还原产物可能是KI或NaI
D.当溶液中I¯与I2的物质的量之比为1:1时,加入的KIO3为9/8mol
查看习题详情和答案>>