摘要:在固定体积的密闭容器中.注入2体积的SO2和1体积的O2.在一定条件下发生反应:2SO2(g)+O2(g)⇌2SO3(g).达平衡后温度不变.压强降低了1/4.SO2的转化率是( ). A.60% B.75% C.80% D.50% 答案:B
网址:http://m.1010jiajiao.com/timu3_id_326814[举报]
 在80℃时,将0.40mol的N204气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4?2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:
在80℃时,将0.40mol的N204气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4?2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:| 时间(s) n(mol) |
0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
0.0020
0.0020
mol?L-1?S-1;(2)计算在80℃时该反应的平衡常数K=
1.8mol?L-1
1.8mol?L-1
(请注明单位).(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色(填“变浅”.“变深”或“不变”)
变浅
变浅
;(4)要增大该反应的K值,可采取的措施有(填序号)
D
D
:A.增大N2O4的起始浓度 B.向混合气体中通入NO2 C.使用高效催化剂 D.升高温度
(5)如图是80℃时容器中N204物质的量的变化曲线,请在该图中补画出该反应在60℃时N204物质的量的变化曲线.
在80℃时,将0.40mo1的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4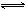 2NO2
△H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2
△H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
|
t/s n/mol |
0 |
20 |
40 |
60 |
80 |
100 |
|
n(N2O4) |
0.40 |
a |
0.20 |
c |
d |
e |
|
n(NO2) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
(1)计算0~20s内用NO2表示的平均反应速率为 mo1•L—1•s—1。
(2)计算在80℃时该反应的平衡常数K= (请注明单位)。
(3)反应进行至100s后将反应混合物的温度升高,混合气体的颜色 (填“变浅”“变深”或“不变”)。
(4)要增大该反应的K值,可采取的措施有 (填序号)。
A.增大N2O4的起始浓度
C.使用高效催化剂
B.向混合气体中通入NO2
D.升高温度
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出(不用计算,定性处理)该反应在60℃时N2O4物质的量的变化曲线。

查看习题详情和答案>>
在80℃时,将0.40mo1的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4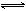 2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
| t/s n/mol | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(2)计算在80℃时该反应的平衡常数K= (请注明单位)。
(3)反应进行至100s后将反应混合物的温度升高,混合气体的颜色 (填“变浅”“变深”或“不变”)。
(4)要增大该反应的K值,可采取的措施有 (填序号)。
A.增大N2O4的起始浓度
C.使用高效催化剂
B.向混合气体中通入NO2
D.升高温度
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出(不用计算,定性处理)该反应在60℃时N2O4物质的量的变化曲线。
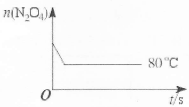 查看习题详情和答案>>
查看习题详情和答案>>
在80℃时,将0.40mol的N24气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4?2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:
(1)计算20s一40s内用N2O4表示的平均反应速率为______mol?L-1?S-1;
(2)计算在80℃时该反应的平衡常数K=______(请注明单位).
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色(填“变浅”.“变深”或“不变”)______;
(4)要增大该反应的K值,可采取的措施有(填序号)______:
A.增大N2O4的起始浓度 B.向混合气体中通入NO2 C.使用高效催化剂 D.升高温度
(5)如图是80℃时容器中N24物质的量的变化曲线,请在该图中补画出该反应在60℃时N24物质的量的变化曲线.
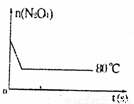 查看习题详情和答案>>
查看习题详情和答案>>
| 时间(s) n(mol) | 20 | 40 | 60 | 80 | 100 | |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(2)计算在80℃时该反应的平衡常数K=______(请注明单位).
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色(填“变浅”.“变深”或“不变”)______;
(4)要增大该反应的K值,可采取的措施有(填序号)______:
A.增大N2O4的起始浓度 B.向混合气体中通入NO2 C.使用高效催化剂 D.升高温度
(5)如图是80℃时容器中N24物质的量的变化曲线,请在该图中补画出该反应在60℃时N24物质的量的变化曲线.
 查看习题详情和答案>>
查看习题详情和答案>>
在80℃时,将0.40mo1的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
(1)计算0~20s内用NO2表示的平均反应速率为 mo1?L—1?s—1。
(2)计算在80℃时该反应的平衡常数K= (请注明单位)。
(3)反应进行至100s后将反应混合物的温度升高,混合气体的颜色 (填“变浅”“变深”或“不变”)。
(4)要增大该反应的K值,可采取的措施有 (填序号)。
A.增大N2O4的起始浓度
C.使用高效催化剂
B.向混合气体中通入NO2
D.升高温度
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出(不用计算,定性处理)该反应在60℃时N2O4物质的量的变化曲线。

 2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:| t/s n/mol | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(2)计算在80℃时该反应的平衡常数K= (请注明单位)。
(3)反应进行至100s后将反应混合物的温度升高,混合气体的颜色 (填“变浅”“变深”或“不变”)。
(4)要增大该反应的K值,可采取的措施有 (填序号)。
A.增大N2O4的起始浓度
C.使用高效催化剂
B.向混合气体中通入NO2
D.升高温度
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出(不用计算,定性处理)该反应在60℃时N2O4物质的量的变化曲线。
