摘要:实验室可用NaNO2和NH4Cl共热方法制取少量N2(同时生成NaCl和H2O).若标准状况下制得5.6L氮气.则被氧化的氮原子是( ). A.3.5g B.7g C.0.25mol D.0.5mol 答案:AC
网址:http://m.1010jiajiao.com/timu3_id_326795[举报]
实验室可用NaNO2+NH4Cl =NaCl+N2↑+2H2O制备N2,下列说法正确的是
A.NaNO2发生氧化反应
B.NH4Cl中的氮元素被还原
C.N2既是氧化产物,又是还原产物
D.每生成1mol N2转移电子的物质的量为6mol
查看习题详情和答案>>
实验室可用NaNO2+NH4Cl =NaCl+N2↑+2H2O制备N2,下列说法正确的是
- A.NaNO2发生氧化反应
- B.NH4Cl中的氮元素被还原
- C.N2既是氧化产物,又是还原产物
- D.每生成1mol N2转移电子的物质的量为6mol
实验室可用NaNO2+NH4Cl NaCl+N2↑+2H2O制备N2,下列说法正确的是
NaCl+N2↑+2H2O制备N2,下列说法正确的是
- A.NaNO2发生氧化反应
- B.NH4Cl中的氮元素被还原
- C.N2既是氧化产物,又是还原产物
- D.每生成1mol N2转移电子的物质的量为6mol
 氯化铵是一种重要的化工原料,应用广泛.
氯化铵是一种重要的化工原料,应用广泛.(1)实验室通常用NH4Cl固体与Ca(OH)2固体混合共热制取氨气.
①写出实验室制取氨气的反应方程式
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
②浓氨水可以用来检验有毒气体氯气的泄漏,反应式为3Cl2+8NH3=N2+6NH4Cl,在该反应中,氧化剂是
Cl2
Cl2
(填化学式),检测时观察到的现象是有大量白烟产生
有大量白烟产生
,21.3g氯气能氧化氨气0.2
0.2
mol.(2)用浓氯化铵溶液处理的舞台幕布难着火,其原因是
B
B
(填字母).①幕布的着火点升高
②幕布的质量增加
③氯化铵分解吸收热量,降低了温度
④氯化铵分解产生的气体隔离了部分空气
A.①②B.③④C.①③D.②④
(3)实验室可用NH4Cl溶液与饱和的NaNO2溶液反应制取纯净的氮气,反应方程式为:NaNO2+NH4Cl
| ||
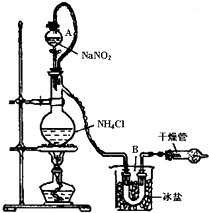
实验装置如图所示,试回答:
①装置中A部分的分液漏斗与蒸馏烧瓶之间连接的导管所起的作用是
c
c
(填写编号).a.防止饱和溶液蒸发
b.保证实验装置不漏气
c.使饱和NaNO2溶液容易滴下
②加热前必须进行的一个操作步骤是
检查气密性
检查气密性
.③收集N2最适宜的方法是
c
c
(填写编号)a.排空气法收集在集气瓶中
b.排水法收集在集气瓶中
c.直接收集在球胆或塑料袋中.