题目内容
实验室可用NaNO2+NH4Cl NaCl+N2↑+2H2O制备N2,下列说法正确的是
NaCl+N2↑+2H2O制备N2,下列说法正确的是
- A.NaNO2发生氧化反应
- B.NH4Cl中的氮元素被还原
- C.N2既是氧化产物,又是还原产物
- D.每生成1mol N2转移电子的物质的量为6mol
C
分析:NaNO2+NH4Cl NaCl+N2↑+2H2O中,N元素的化合价由-3价升高为0,N元素的化合价由+3价降低为0,以此来解答.
NaCl+N2↑+2H2O中,N元素的化合价由-3价升高为0,N元素的化合价由+3价降低为0,以此来解答.
解答:NaNO2+NH4Cl NaCl+N2↑+2H2O中,N元素的化合价由-3价升高为0,N元素的化合价由+3价降低为0,
NaCl+N2↑+2H2O中,N元素的化合价由-3价升高为0,N元素的化合价由+3价降低为0,
A.NaNO2发生还原反应,故A错误;
B.NH4Cl中的氮元素被氧化,故B错误;
C.反应中只有N元素的化合价变化,N2既是氧化产物,又是还原产物,故C正确;
D.生成1molN2转移电子的物质的量为1mol×(3-0)=3mol,故D错误;
故选C.
点评:本题考查氧化还原反应,明确反应中元素的化合价变化是解答的关键,题目较简单.
分析:NaNO2+NH4Cl
 NaCl+N2↑+2H2O中,N元素的化合价由-3价升高为0,N元素的化合价由+3价降低为0,以此来解答.
NaCl+N2↑+2H2O中,N元素的化合价由-3价升高为0,N元素的化合价由+3价降低为0,以此来解答.解答:NaNO2+NH4Cl
 NaCl+N2↑+2H2O中,N元素的化合价由-3价升高为0,N元素的化合价由+3价降低为0,
NaCl+N2↑+2H2O中,N元素的化合价由-3价升高为0,N元素的化合价由+3价降低为0,A.NaNO2发生还原反应,故A错误;
B.NH4Cl中的氮元素被氧化,故B错误;
C.反应中只有N元素的化合价变化,N2既是氧化产物,又是还原产物,故C正确;
D.生成1molN2转移电子的物质的量为1mol×(3-0)=3mol,故D错误;
故选C.
点评:本题考查氧化还原反应,明确反应中元素的化合价变化是解答的关键,题目较简单.

练习册系列答案
相关题目
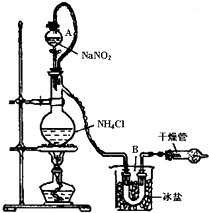 氯化铵是一种重要的化工原料,应用广泛.
氯化铵是一种重要的化工原料,应用广泛.