摘要:T℃时.在一个体积为2L的容器中.A气体与B气体反应生成C气体.反应过程中A.B. C浓度变化如图所示.(1)写出该反应的方程式: (2)计算该温度下该反应的平衡常数: >K.该反应是 热反应. (4)0-4分钟时.A的平均反应速率为: (5)到达平衡时B的转化率为: (6)恒容条件下.下列措施中能使n降低的有 . A.充入氦气 B.使用催化剂 C.再充入2.4molA和1.6molB D.降低温度 2010学年第二学期十校联合体高二期中联考
网址:http://m.1010jiajiao.com/timu3_id_325949[举报]
 T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示.
T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示.(1)写出该反应的方程式:
2A+B  C
C
 C
C2A+B  C
C
 C
C(2)计算该温度下该反应的平衡常数:
0.52
0.52
(3)已知:K(300℃)>K(350℃),该反应是
放
放
热反应.(4)0~4分钟时,A的平均反应速率为:
0.05mol?L-1?min-1
0.05mol?L-1?min-1
(5)到达平衡时B的转化率为:
25%
25%
(6)恒容条件下,下列措施中能使n(A)/n(C)降低的有
CD
CD
.A.充入氦气 B.使用催化剂
C.再充入2.4molA和1.6molB D.降低温度.
T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示.
(1)写出该反应的方程式:______
(2)计算该温度下该反应的平衡常数:______
(3)已知:K(300℃)>K(350℃),该反应是______热反应.
(4)0~4分钟时,A的平均反应速率为:______
(5)到达平衡时B的转化率为:______
(6)恒容条件下,下列措施中能使n(A)/n(C)降低的有______.
A.充入氦气 B.使用催化剂
C.再充入2.4molA和1.6molB D.降低温度.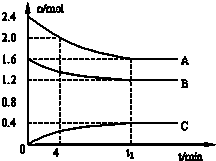
查看习题详情和答案>>
(1)写出该反应的方程式:______
(2)计算该温度下该反应的平衡常数:______
(3)已知:K(300℃)>K(350℃),该反应是______热反应.
(4)0~4分钟时,A的平均反应速率为:______
(5)到达平衡时B的转化率为:______
(6)恒容条件下,下列措施中能使n(A)/n(C)降低的有______.
A.充入氦气 B.使用催化剂
C.再充入2.4molA和1.6molB D.降低温度.

T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示.
(1)写出该反应的方程式:
(2)计算该温度下该反应的平衡常数:
(3)已知:K(300℃)>K(350℃),该反应是 热反应.
(4)0~4分钟时,A的平均反应速率为:
(5)到达平衡时B的转化率为:
(6)恒容条件下,下列措施中能使n(A)/n(C)降低的有 .
A.充入氦气 B.使用催化剂
C.再充入2.4molA和1.6molB D.降低温度.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)写出该反应的方程式:
(2)计算该温度下该反应的平衡常数:
(3)已知:K(300℃)>K(350℃),该反应是 热反应.
(4)0~4分钟时,A的平均反应速率为:
(5)到达平衡时B的转化率为:
(6)恒容条件下,下列措施中能使n(A)/n(C)降低的有 .
A.充入氦气 B.使用催化剂
C.再充入2.4molA和1.6molB D.降低温度.
 查看习题详情和答案>>
查看习题详情和答案>>
在一定条件下发生化学反应:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol.现有容积均为1L的甲、乙、丙、丁 四个容器,在上述条件下分别充入气体,到达平衡时,反应放出的热量(Q),及平衡时的转化率(X)如下表所示:
(1)下列说法一定正确的是______
a、2Q3=2Q2<Q1<197kJ b、2X3=2X2<X1<100%
c、Q1>Q4 且 X1>X4 d、SO3的质量m:m甲=m丁>2m乙
e、容器内压强p:p甲=p丁>2p乙 f、c(SO2)与c(O2)之比k:k甲=k丙>k乙
h、若乙的体积为2L,则到达平衡时放出的热量小于39.4kJ
(2)某时刻甲容器内反应达到平衡,保持恒温恒容;
①假设又向容器内加入一定量的SO2气体,则X(SO2)______(填“增大”或“减小”),O2的浓度______(填“增大”或“减小”)
②假设又向容器中加入一定量的SO3(g),X(SO2)______ (填“增大”或“减小”)
(3)平衡时,乙容器中SO2的体积分数为______%(保留两位有效数字),该反应的平衡常数为______(填具体值和单位,保留两位有效数字)
(4)如图表示某一时间段中该反应反应速率与反应过程的关系(t2、t4、t5)时刻改变的条件都只有一个).
①t 2时改变的条件是______;
②若t5时降低压强,试画出t-v图象
③若各阶段对应的平衡常数如图所示
则各平衡常数间的大小关系为______(由大到小排列)
查看习题详情和答案>>
| 容器 | 起始时各物质的量 | 到达平衡时放出的热量(QkJ) | 平衡时SO2转化率 (X) | |||
| SO2(mol) | O2(mol) | SO3(mol) | N2 | |||
| 甲 | 2 | 1 | Q1 | X1 | ||
| 乙 | 1 | 0.5 | Q2=39.4 | X2 | ||
| 丙 | 1 | 0.5 | 1 | Q3 | X3 | |
| 丁 | 1.8 | 0.9 | 0.2 | Q4 | X4 | |
a、2Q3=2Q2<Q1<197kJ b、2X3=2X2<X1<100%
c、Q1>Q4 且 X1>X4 d、SO3的质量m:m甲=m丁>2m乙
e、容器内压强p:p甲=p丁>2p乙 f、c(SO2)与c(O2)之比k:k甲=k丙>k乙
h、若乙的体积为2L,则到达平衡时放出的热量小于39.4kJ
(2)某时刻甲容器内反应达到平衡,保持恒温恒容;
①假设又向容器内加入一定量的SO2气体,则X(SO2)______(填“增大”或“减小”),O2的浓度______(填“增大”或“减小”)
②假设又向容器中加入一定量的SO3(g),X(SO2)______ (填“增大”或“减小”)
(3)平衡时,乙容器中SO2的体积分数为______%(保留两位有效数字),该反应的平衡常数为______(填具体值和单位,保留两位有效数字)
(4)如图表示某一时间段中该反应反应速率与反应过程的关系(t2、t4、t5)时刻改变的条件都只有一个).

①t 2时改变的条件是______;
②若t5时降低压强,试画出t-v图象
③若各阶段对应的平衡常数如图所示
| t 1-t 2 | t 3-t 4 | t 4-t 5 | t 6-t 7 |
| K1 | K2 | K3 | K4 |
查看习题详情和答案>>
(12 分)T℃时,在某容积恒为2L密闭容器中充入2molN2、4molH2,在催化剂辅助下发生反应:N2(g)+3H2(g) 2NH3(g) △H=-92.0kJ /mol。t0时刻,建立平衡后,测得生成NH3的量为2mol;从t1时刻开始,改变反应的一个条件,体系中反应速率随时间变化的情况,如下图所示。
2NH3(g) △H=-92.0kJ /mol。t0时刻,建立平衡后,测得生成NH3的量为2mol;从t1时刻开始,改变反应的一个条件,体系中反应速率随时间变化的情况,如下图所示。
试回答下列问题:
(1)T℃时,N2的转化率为:___________,该反应的平衡常数K=___________。
(2)T℃时,下列能证明该反应已经建立平衡状态的是:__________________。
| A.体系总压强不再改变 |
| B.混合气体颜色不再改变 |
| C.H2的质量百分含量不再改变 |
| D.c(N2)与c(NH3)的比值不再改变 |
(4)T℃时,建立平衡后,向容器中加入2molN2和2molNH3,则此时 v正 ___ v逆。 查看习题详情和答案>>