题目内容
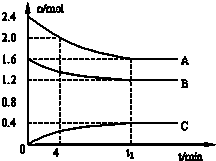
 T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示.
T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示.(1)写出该反应的方程式:
 C
C C
C(2)计算该温度下该反应的平衡常数:
(3)已知:K(300℃)>K(350℃),该反应是
(4)0~4分钟时,A的平均反应速率为:
(5)到达平衡时B的转化率为:
(6)恒容条件下,下列措施中能使n(A)/n(C)降低的有
A.充入氦气 B.使用催化剂
C.再充入2.4molA和1.6molB D.降低温度.
(2)根据平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积计算;
(3)根据温度对平衡常数的影响分析;
(4)根据v=
| △c |
| △t |
(5)根据图象中B的物质的量的变化计算转化率;
(6)
| n(A) |
| n(C) |
且△n(A):△n(B):△n(C)=0.8mol:0.4mol:0.4mol=2:1:1,则反应的化学方程式为:2A+B
 C,
C,故答案为:2A+B
 C;
C;(2)k=
| c(C) |
| c2(A)?c(B) |
| 0.2mol/L |
| (0.8mol/L)2?0.6mol/L |
(3)K(300℃)>K(350℃),说明温度升高,平衡向逆反应方向移动,则正反应为放热反应,故答案为:放;
(4)0~4分钟时,A的平均反应速率为:v(A)=
| ||
| 4min |
(5)到达平衡时B的转化率为:
| 1.6mol-1.2mol |
| 1.6mol |
(6)
| n(A) |
| n(C) |
A.充入氦气,各物质的物质的量浓度不变,平衡不移动,故A错误;
B.使用催化剂,平衡不移动,故B错误;
C.再充入2.4molA和1.6molB,反应物的浓度增大,平衡向正反应方向移动,故C正确;
D.降低温度,平衡向正反应方向移动,故D正确,
故答案为:CD.

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案化学在能源开发与利用中起着十分关键的作用。
(1)蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体。甲烷气体燃烧的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3 kJ/mol。
356g“可燃冰”(分子式为CH4·9H2O)释放的甲烷气体完全燃烧生成液态水.放出的热量为 _______ 。
(2)某种燃料电池,一个电极通入空气,另一电极通入液化石油气(以C4H10表示),电池的电解质是掺入了Y2O3的ZrO2晶体,它在高温下传导O2-。
已知该电池负极的电极反应为:C4H10+2O2--4e-=CO2+H2O,则该电池正极的电极反应式为 _______ ,电池工作时,固体电解质里的O2-向 _______ 极移动。
![]() (3)已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g) CO2(g)+H2(g)
(3)已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g) CO2(g)+H2(g)
①T℃时,在一定体积的容器中,通入一定量的CO(g)和H2O(g),发生反应并保持温度不变,各物质浓度随时间变化如下表: T℃时物质的浓度(mol/L)变化
| 时间 / min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
第5、6min时的数据是保持温度和体积不变时,改变某一条件后测得的。第4~5min之间,改变的条件是 _______ ,第5~6min之间,改变的条件是 _______ 。T℃时该化 学反应的平衡常数是 _______ 。
②已知420℃时,该化学反应的平衡常数为9。如果反应开始时,CO和H2O(g)的浓度都是0.01 mol/L,则CO在此条件下的转化率为 _______ 。
③397℃时该反应的平衡常数为12,请判断该反应的△H _______ 0(填“>”、“=”、“<”).