摘要:3.导出式--质子守恒: 如碳酸钠溶液中由电荷守恒和物料守恒将Na+离子消掉可得:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3).此关系式也可以按下列方法进行分析.由于指定溶液中氢原子的物质的量为定值.所以无论溶液中结合氢离子还是失去氢离子.但氢原子总数始终为定值.也就是说结合的氢离子的量和失去氢离子的量相等.可以用图示分析如下: .由得失氢离子守恒可得:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3). 又如醋酸钠溶液中由电荷守恒和物料守恒将钠离子消掉可得:c(OH-)=c(H+)+c(CH3COOH). [规律总结]
网址:http://m.1010jiajiao.com/timu3_id_323569[举报]
 A、B、C、D、E五种物质(或离子)均含有同一种短周期元素,它们之间有如转化关系:
A、B、C、D、E五种物质(或离子)均含有同一种短周期元素,它们之间有如转化关系:(1)若A为非金属单质,C、D的相对分子质量相差16.0.1mol/L E溶液中只有3种离子,且常温下溶液中的pH=1.A→C的反应中,每转移1mol e-就会吸热45kJ,写出该反应的热化学方程式:
N2(g)+O2(g)=2NO(g)△H=+180 kJ/mol
N2(g)+O2(g)=2NO(g)△H=+180 kJ/mol
.(2)若A为金属单质,B、C均属于盐类,D是一种白色沉淀.若B的水溶液呈酸性,C的水溶液呈碱性.写出C→D反应的离子方程式:
AlO2-+H++H2O=Al(OH)3↓
AlO2-+H++H2O=Al(OH)3↓
;写出金属A的电子排布式:1s22s22p63s23p1
1s22s22p63s23p1
.(3)若A-E均为化合物.A是淡黄色固体;B、C、E三种溶液在物质的量浓度相等时,B溶液的pH最大,E溶液的pH最小.
请书写C溶液中的物料守恒式:
| 1 |
| 2 |
| 1 |
| 2 |
c(H+)=c(OH-)+2c(H2CO3)+c(HCO3-)
c(H+)=c(OH-)+2c(H2CO3)+c(HCO3-)
.(2013?烟台模拟)氯化钠、乙烯是化学工业的重要原料.
(1)工业上由NaCl制Na的化学方程式为
(2)如图为电解食盐水与乙烯和Cl2加成制l,2-=氯乙烷的联合装置示意图:
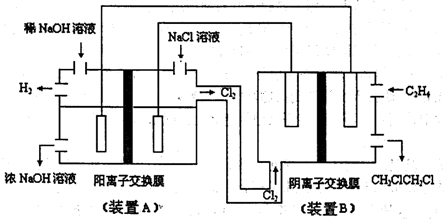
在该装置中,
(3)常温下,NaHCO3溶液中存在的质子守恒关系式为:c(OH-)+
加热0.5mol?L-1NaHCO3溶液,使NaHCO380%分解,然后恢复至室温.假设反应前后溶液的体积不变,则反应后的溶液中c(CO2-3)+c(HCO3+c(H2CO3)=
查看习题详情和答案>>
(1)工业上由NaCl制Na的化学方程式为
2NaCl
2Na+Cl2↑
| ||
| 熔融 |
2NaCl
2Na+Cl2↑
;实验室中金属钠应保存在盛有
| ||
| 熔融 |
煤油
煤油
的广口瓶中;若将一小块钠长期暴露在空气中,最终钠将转化为Na2CO3
Na2CO3
.(2)如图为电解食盐水与乙烯和Cl2加成制l,2-=氯乙烷的联合装置示意图:

在该装置中,
B
B
为原电池(填“A”或“B”)提供电能,其负极的电极反应式为C2H4+2Cl-+2e-=CH2ClCH2Cl
C2H4+2Cl-+2e-=CH2ClCH2Cl
.在A装置中,阳离子交换膜的作用是传导钠离子、氢离子形成闭合回路,防止氢气和氯气及氯气和氢氧化钠接触而发生副反应
传导钠离子、氢离子形成闭合回路,防止氢气和氯气及氯气和氢氧化钠接触而发生副反应
.(3)常温下,NaHCO3溶液中存在的质子守恒关系式为:c(OH-)+
c(CO32-)
c(CO32-)
=c(H+)+c(H2CO3);加热0.5mol?L-1NaHCO3溶液,使NaHCO380%分解,然后恢复至室温.假设反应前后溶液的体积不变,则反应后的溶液中c(CO2-3)+c(HCO3+c(H2CO3)=
0.3
0.3
_mol?L-1.化学在环境保护中起着十分重要的作用,催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
(1) 催化反硝化法中,H2能将NO3—还原为N2,25℃时,反应进行10min,溶液的pH由7变为12。
①N2的结构式为 。
②上述反应离子方程式为 ,其平均反应速率v(NO3—)为 。
|
。
④在NaNO2 溶液中,质子守恒表达式为
___________________________________________。
(2)电化学降解NO3—的原理如右图所示。
| |
阴极反应式为:
。
查看习题详情和答案>>二元酸H2A在水中的电离情况是:H2A=H++HA-和HA-![]() H++A2-,写出下列物质的水溶液的相应关系式:
H++A2-,写出下列物质的水溶液的相应关系式:
(1)NaHA溶液中的离子浓度大小关系:________
(2)NaHA溶液的物料守恒式:________
(3)溶液的电荷守恒式:________
(4)NaHA溶液的质子守恒式:________
25℃时,用浓度为0.100mol/L的氢氧化钠溶液分别滴定20.00mL浓度均为0.100mol/L的二种酸HX、HY(忽略体积变化),实验数据如下表,下列判断正确的是( )
数据编号 |
NaOH加入的体积/mL |
溶液的pH | ||
| C(HX) | c(HY) | |||
| ① | 0 | 3 | 1 | |
| ② | a | 7 | ||
| ③ | 20.00 | x | y | |
| A、在相同温度下,同浓度的两种酸溶液的导电能力顺序HX<HY |
| B、由表中数据可估算出Ka(HX)≈10-5 |
| C、HY和HX混合,达到平衡时满足质子守恒 |
| D、上述②反应后的HY溶液中:c(Na+)>c(Y-)>c(OH-)>c(H+) |
