摘要:略 [基础训练]
网址:http://m.1010jiajiao.com/timu3_id_321505[举报]
(2011?北京)甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验).
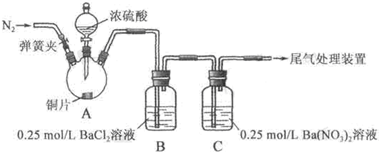
实验操作和现象:
(1)A中反应的化学方程式是
(2)C中白色沉淀是
(3)C中液面上方生成浅棕色气体的化学方程式是
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是
乙在A、B间增加洗气瓶D,D中盛放的试剂是
②进行实验,B中现象:
检验白色沉淀,发现均不溶于稀盐酸.结合离子方程式解释实验现象异同的原因:
(5)合并(4)中两同学的方案进行实验.B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是
查看习题详情和答案>>

实验操作和现象:
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | --- |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
Cu+2H2SO4
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4
CuSO4+SO2↑+2H2O
.
| ||
(2)C中白色沉淀是
BaSO4
BaSO4
,该沉淀的生成表明SO2具有还原
还原
性.(3)C中液面上方生成浅棕色气体的化学方程式是
2NO+O2═2NO2
2NO+O2═2NO2
.(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是
通N2一段时间,排除装置中的空气
通N2一段时间,排除装置中的空气
;乙在A、B间增加洗气瓶D,D中盛放的试剂是
饱和NaHSO3溶液
饱和NaHSO3溶液
.②进行实验,B中现象:
| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |
甲:SO42-+Ba2═BaSO4↓,乙:2Ba2++2SO2+O2+2H2O═2BaSO4↓+4H+,白雾的量远多于装置中O2的量
甲:SO42-+Ba2═BaSO4↓,乙:2Ba2++2SO2+O2+2H2O═2BaSO4↓+4H+,白雾的量远多于装置中O2的量
.(5)合并(4)中两同学的方案进行实验.B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是
SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀
SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀
.甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)
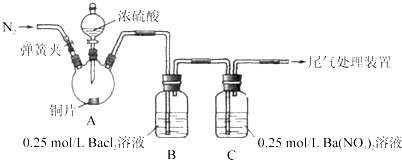
实验操作和现象:(BaCl2提示:A中产生的白雾,是H2SO4的酸雾)
(1)A中反应的化学方程式是
(2)C中白色沉淀是
(3)C中液面上方生成浅棕色气体的化学方程式是
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是
乙在A、B间增加洗气瓶D,D中盛放的试剂是足量饱和NaHSO3溶液.其目的是
②甲、乙分别进行实验,B中现象:
检验白色沉淀,发现均不溶于稀盐酸.结合离子方程式解释白色沉淀产生原因:
甲:
(5)合并(4)中两同学的方案进行试验.B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是
查看习题详情和答案>>

实验操作和现象:(BaCl2提示:A中产生的白雾,是H2SO4的酸雾)
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.
| ||
(2)C中白色沉淀是
BaSO4
BaSO4
,该沉淀的生成表明SO2具有还原
还原
性.(3)C中液面上方生成浅棕色气体的化学方程式是
2NO+O2=2NO2
2NO+O2=2NO2
.(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是
通N2一段时间,排除装置的空气
通N2一段时间,排除装置的空气
;乙在A、B间增加洗气瓶D,D中盛放的试剂是足量饱和NaHSO3溶液.其目的是
吸收H2SO4酸雾
吸收H2SO4酸雾
.②甲、乙分别进行实验,B中现象:
| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |
甲:
SO42-+Ba2+=BaSO4↓
SO42-+Ba2+=BaSO4↓
;乙:2Ba2++2SO2+O2+2H2O=2BaSO4+4H+
2Ba2++2SO2+O2+2H2O=2BaSO4+4H+
.(5)合并(4)中两同学的方案进行试验.B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是
SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀
SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀
.(2012?奉贤区二模)为探究SO2与可溶性钡盐能否反应生成白色BaSO3沉淀,甲、乙两同学用下图所示装置进行实验(夹持装置、加热装置已略,气密性已检验)
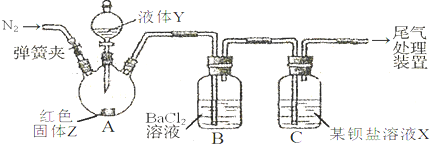
实验操作和现象:
(1)A中反应的化学方程式是
(2)C中可溶性钡盐溶液X为
(3)分析B中不溶于稀盐酸的沉淀的产生原因,甲同学认为是
甲、乙各自进行实验,B中现象分别如下表:由此得出的结论是
(4)丙将甲乙两同学的方案进行联合试验,发现B中无沉淀生成,而C中产生白色沉淀,但无红棕色气体.C中反应的化学方程式是
(5)丁同学认为丙选择的两种钡盐比较相似,于是丁在丙的基础上将B、C中的钡盐分别换成过量新制的醋酸钡溶液、Ba(AlO2)2溶液,发现B、C中均立即产生大量白色沉淀,该沉淀可溶于稀盐酸,并产生能使澄清石灰水浑浊的气体.C中沉淀为
(6)结合实验目的,根据四位同学的实验操作和实验现象,你得出的结论是
查看习题详情和答案>>

实验操作和现象:
| 操 作 | 现 象 |
| 关闭弹簧夹,滴加一定量液体Y,加强热; | A中有白雾生成,红色固体Z的表面产生气泡.B中有气泡冒出,产生大量白色沉淀.C中产生白色沉淀,液面上方略显红棕色并逐渐消失. |
| 打开弹簧夹,通入气体N2,停止加热,一段时间后关闭; | |
| 从B、C中分别取少量白色沉淀,加稀盐酸. | 均未发现白色沉淀溶解 |
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.
| ||
(2)C中可溶性钡盐溶液X为
硝酸钡
硝酸钡
.实验过程中,发现液体Y不能很顺利地滴下,则可如何改进:将分液漏斗改为恒压漏斗
将分液漏斗改为恒压漏斗
.(3)分析B中不溶于稀盐酸的沉淀的产生原因,甲同学认为是
空气参与了反应
空气参与了反应
,乙同学认为是白雾参与反应.为证实各自的观点,在原实验基础上;甲同学在原有操作之前,先通N2一段时间.乙同学则在A、B间增加盛有饱和NaHSO3溶液的洗气瓶D.甲、乙各自进行实验,B中现象分别如下表:由此得出的结论是
空气、白雾均是产生白色沉淀的原因,白雾是主要原因
空气、白雾均是产生白色沉淀的原因,白雾是主要原因
.| 甲 | 大量不溶于稀盐酸的白色沉定 |
| 乙 | 少量不溶于稀盐酸的白色沉淀 |
3SO2+2H2O+3Ba(NO3)2═3BaSO4↓+2NO↑+4HNO3
3SO2+2H2O+3Ba(NO3)2═3BaSO4↓+2NO↑+4HNO3
.(5)丁同学认为丙选择的两种钡盐比较相似,于是丁在丙的基础上将B、C中的钡盐分别换成过量新制的醋酸钡溶液、Ba(AlO2)2溶液,发现B、C中均立即产生大量白色沉淀,该沉淀可溶于稀盐酸,并产生能使澄清石灰水浑浊的气体.C中沉淀为
BaSO3、氢氧化铝
BaSO3、氢氧化铝
.实验室里欲获得该沉淀,所需要的玻璃仪器是烧杯、漏斗、玻璃棒
烧杯、漏斗、玻璃棒
.(6)结合实验目的,根据四位同学的实验操作和实验现象,你得出的结论是
SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀,SO2与可溶性钡的弱酸盐能反应生成BaSO3沉淀
SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀,SO2与可溶性钡的弱酸盐能反应生成BaSO3沉淀
.(2008?枣庄一模)学习元素周期律后,某研究性学习小组的同学们对第四周期过渡元素的氧化物产生了浓厚的兴趣.在已知二氧化锰对氯酸钾催化分解知识的基础上,联想到氧化铁、氧化铜、氧化铬等对氯酸钾的分解是否有催化作用,对此他们进行了实验研究.
请根据要求完成下列部分实验报告:
(1)课题名称:
(2)实验仪器及试剂:
实验仪器:带铁夹的铁架台、带橡皮塞的导管、量气装置、过滤装置、电子天平、药匙、
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾
(3)实验步骤:略
(4)实验数据:
(5)实验讨论:
①在氧化物的回放过程中,要进行的操作是溶解、
②实验编号3的实验中KClO3的分解率为
③在和Cr2O3做研究实验时,发现有刺激性气味的气体产生,同时绿色的混合物变成了橘黄色.该刺激性气味的气体是
(6)实验结论
查看习题详情和答案>>
请根据要求完成下列部分实验报告:
(1)课题名称:
探究氧化铁、氧化铜、氧化铬等对氯酸钾分配是否有催化作用
探究氧化铁、氧化铜、氧化铬等对氯酸钾分配是否有催化作用
.(2)实验仪器及试剂:
实验仪器:带铁夹的铁架台、带橡皮塞的导管、量气装置、过滤装置、电子天平、药匙、
试管、酒精灯、秒表
试管、酒精灯、秒表
等.实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾
(3)实验步骤:略
(4)实验数据:
| 实验 编号 |
KClO3/g | 氧化物 | 产生气体/mL (已折算到标况) |
耗时/s | ||
| 化学式 | 质量/g | 回收 | ||||
| 1 | 0.60 | - | - | - | 10 | 480 |
| 2 | 0.60 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.60 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.60 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.60 | Cr2O3 | 0.20 | 90% | 67.2 | 188.3 |
①在氧化物的回放过程中,要进行的操作是溶解、
过滤
过滤
、洗涤、干燥
干燥
、称量.②实验编号3的实验中KClO3的分解率为
40.8
40.8
(保留一位小数).③在和Cr2O3做研究实验时,发现有刺激性气味的气体产生,同时绿色的混合物变成了橘黄色.该刺激性气味的气体是
C12
C12
,可用湿润的KI淀粉
湿润的KI淀粉
试纸检验.上述异常现象产生的原因是Cr2O3与KC1O3发生氧化还原反应
Cr2O3与KC1O3发生氧化还原反应
.(6)实验结论
Fe2O3、CuO能对KC1O(3分)解起催化作用
Fe2O3、CuO能对KC1O(3分)解起催化作用
.
同学们为探究Na2SO3和SO2有关性质进了相关的实验(已知:H2S是一种酸性气体,且具有很强的还原性).
(1)取一定量没有变质纯净的Na2SO3?7H2O晶体,经600℃以上的强热至恒重,通过分析及计算表明,恒重后的样品质量恰好等于无水亚硫酸钠质量的计算值,而且各元素的组成也同样与亚硫酸钠组成符合.但将加热恒重后的样品溶于水,却发现溶液的碱性大大高于亚硫酸钠溶液的期望值.经过仔细思考,同学们提出了对这种反常现象的合理解析.
①你对这结论的解释是(用化学方程式表达) ;
②请设计相应的实验方案,验证以上的解释.(只要求写出实验设计的原理和判断结论,不要求具体的实验操作) .
(2)为探究SO2与氯化钡溶液能否生成白色BaSO3沉淀,甲、乙两同学共同设计了下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验).关闭装置A中弹簧夹,滴加一定量浓硫酸,加热,A中有白雾生成,铜片表面产生气泡,B中有气泡冒出,产生大量白色沉淀,C中产生白色沉淀,液面上方略显浅棕色并逐渐消失.打开弹簧夹,通入N2,停止加热,一段时间后关闭.从B、C中分别取少量白色沉淀,加稀盐酸,均未发现白色沉淀溶解.

①写出构成装置A的玻璃仪器的名称 .
②A中发生反应的化学方程式是 .
③生成C中白色沉淀的离子方程式 .
④分析B中不溶于稀盐酸的沉淀产生的原因,请你提出合理的解释(只要求讲出一种情况) .为证实你自己的观点,只要在原实验基础上,再多进行一步实验操作,该操作是 .
⑤通过本实验探究,可以得出的结论是 .
查看习题详情和答案>>
(1)取一定量没有变质纯净的Na2SO3?7H2O晶体,经600℃以上的强热至恒重,通过分析及计算表明,恒重后的样品质量恰好等于无水亚硫酸钠质量的计算值,而且各元素的组成也同样与亚硫酸钠组成符合.但将加热恒重后的样品溶于水,却发现溶液的碱性大大高于亚硫酸钠溶液的期望值.经过仔细思考,同学们提出了对这种反常现象的合理解析.
①你对这结论的解释是(用化学方程式表达)
②请设计相应的实验方案,验证以上的解释.(只要求写出实验设计的原理和判断结论,不要求具体的实验操作)
(2)为探究SO2与氯化钡溶液能否生成白色BaSO3沉淀,甲、乙两同学共同设计了下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验).关闭装置A中弹簧夹,滴加一定量浓硫酸,加热,A中有白雾生成,铜片表面产生气泡,B中有气泡冒出,产生大量白色沉淀,C中产生白色沉淀,液面上方略显浅棕色并逐渐消失.打开弹簧夹,通入N2,停止加热,一段时间后关闭.从B、C中分别取少量白色沉淀,加稀盐酸,均未发现白色沉淀溶解.

①写出构成装置A的玻璃仪器的名称
②A中发生反应的化学方程式是
③生成C中白色沉淀的离子方程式
④分析B中不溶于稀盐酸的沉淀产生的原因,请你提出合理的解释(只要求讲出一种情况)
⑤通过本实验探究,可以得出的结论是