网址:http://m.1010jiajiao.com/timu3_id_321173[举报]
(1)黄铁矿(FeS2,其中S为-1价)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为3FeS2+8O2
| ||
(2)与明矾相似,硫酸铁也可用作净水剂.某自来水厂用氯气和绿矾
 (FeSO4?7H2O)一起净水,其原理为
(FeSO4?7H2O)一起净水,其原理为Fe3++3H2O?Fe(OH)3(胶体)+3H+
Fe3++3H2O?Fe(OH)3(胶体)+3H+
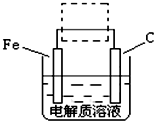
(3)①钢铁的电化腐蚀简单示意图如右,将该图稍作修改 即可成为钢铁电化学防护的简单示意图,请在右图虚线框内作出修改,并用箭头标出电子流动方向.
②写出修改前的钢铁吸氧腐蚀石墨电极的电极反应式
(4)高铁酸钾(K2FeO4)可用作净水剂,也可用于制造高铁电池.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为
3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH该电池放电时正极反应式为
用该电池电解100mL 1mol?L-1的AgNO3溶液,当电路中通过0.1mol 电子时,被电解
 溶液的pH为
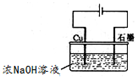
溶液的pH为(5)氧化亚铜是一种半导体材料,常用作制造整流器的材料,还可以用于光照条件下水分解的催化剂和农作物的杀菌剂.
用右图装置可制得氧化亚铜,试写出阳极的电极反应式
(1)M在元素周期表中的位置为
(2)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为
a.+99.7kJ?mol-1 b.+29.7kJ?mol-1
c.-20.6 1kJ?mol-1 d.-241.8kJ?mol-1
(3)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热可分解.写出生成R的反应式:
(1)五种元素的原子半径从大到小的顺序是
(2)X与Z形成的3:1的化合物A,它与Z的最高价氧化物对应的水化物B反应的化学方程式
(3)硒是人体必需的微量元素,与L同一主族,其最高价氧化物对应的水化物化学式为
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q.写出阳极生成R的电极反应式:
X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。回答下列问题:
(1)五种元素的原子半径从大到小的顺序是 (用元素符号表示)。
(2)X与Z形成的3∶1的化合物A,它与Z的最高价氧化物对应的水化物B反应的化学方程式 ,该水溶液显 性,用离子方程式解释原因 。
(3)硒是人体必需的微量元素,与L同一主族,其最高价氧化物对应的水化物化学式为 。该元素固体单质与H2反应生成0.5 mol气态氢化物时吸收了14.87kJ的热量,请写出1mol该物质与氢气化合的热化学方程式 。
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q 。写出阳极生成R的电极反应式: ;由R生成Q的化学方程式: 。
查看习题详情和答案>>X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。回答下列问题:
(1)五种元素的原子半径从大到小的顺序是 (用元素符号表示)。
(2)X与Z形成的3∶1的化合物A,它与Z的最高价氧化物对应的水化物B反应的化学方程式 ,该水溶液显 性,用离子方程式解释原因 。
(3)硒是人体必需的微量元素,与L同一主族,其最高价氧化物对应的水化物化学式为 。该元素固体单质与H2反应生成0.5 mol气态氢化物时吸收了14.87kJ的热量,请写出1mol该物质与氢气化合的热化学方程式 。
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q 。写出阳极生成R的电极反应式: ;由R生成Q的化学方程式: 。
查看习题详情和答案>>