摘要:8.下列反应中.HCl既作氧化剂又作还原剂的是( ) 通电 A.CuO+2HCl==CuCl2+H2O B.NaOH+HCl==NaCl+H2O C.Zn+2HCl==ZnCl2+H2↑ D.2HCl====H2↑+Cl2↑
网址:http://m.1010jiajiao.com/timu3_id_318444[举报]
Ⅰ.(1)在饱和Na2CO3溶液中通入足量的CO2气体,会有晶体析出,此晶体是_______________。析出晶体的原因有:①_______________,②_______________,③_______________。
(2)向Na2CO3溶液中逐滴滴入稀盐酸,溶液中的![]() 浓度的变化情况是_______。
浓度的变化情况是_______。
A.逐渐增大 B.逐渐变小
C.先逐渐增大而后减小 D.先逐渐减小后变大
试用离子方程式和简要文字说明理由______________________________。
Ⅱ.已知下列4个反应:
①2Na+2H2O====2NaOH+H2↑
②2F2+2H2O====4HF+O2
③Cl2+H2O====HCl+HClO
④C+H2O![]() CO+H2
CO+H2
试从氧化还原反应的角度,完成下列问题:
(1)水只作氧化剂的是________(填数码代号,下同)。
(2)水只作还原剂的是________。
(3)水既不作氧化剂,又不作还原剂的是________。
查看习题详情和答案>>(2011?百色模拟)印刷电路的废腐蚀液含有大量CuC12、FeC12和FeC13,任意排放将导致环境污染及资源的浪费.可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用.测得某废腐蚀液中含CuCl2 1.5mol/L、FeCl2 3.0mol/L、FeCl3 1.0mol/L、HCl 3.0mol/L.取废腐蚀液200mL按如下流程在实验室进行实验:
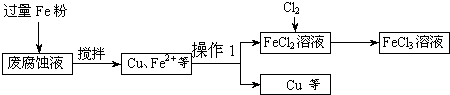
回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂质所需试剂是
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物.反应的化学方程式为
(3)如图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置.
从图中挑选所需的仪器,完成上述装置简图(添加必要的塞子、玻璃导管、胶皮管.固定装置不用画),并标明容器中所装试剂.
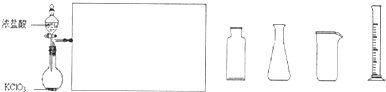
(4)实验中,必需控制氯气的速度,使导管口逸出的气泡每秒1~2个,以便被FeCl2溶液完全吸收.控制生成氯气速率的操作是:
(5)按上述流程操作,需称取Fe粉的质量应不少于
查看习题详情和答案>>

回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂质所需试剂是
HCl
HCl
(填化学式).(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物.反应的化学方程式为
KClO3+6HCl
KCl+3Cl2↑+3H2O
| ||
KClO3+6HCl
KCl+3Cl2↑+3H2O
.
| ||
(3)如图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置.
从图中挑选所需的仪器,完成上述装置简图(添加必要的塞子、玻璃导管、胶皮管.固定装置不用画),并标明容器中所装试剂.

(4)实验中,必需控制氯气的速度,使导管口逸出的气泡每秒1~2个,以便被FeCl2溶液完全吸收.控制生成氯气速率的操作是:
缓慢旋转分液漏斗的活塞,调节浓盐酸滴下的速度
缓慢旋转分液漏斗的活塞,调节浓盐酸滴下的速度
.(5)按上述流程操作,需称取Fe粉的质量应不少于
39.2
39.2
g(精确到0.1g),需通入Cl2的物质的量不少于0.75
0.75
mol,加入烧瓶中的KClO3的质量应不少于30.6
30.6
g(精确到0.1g).印刷电路的废腐蚀液含有大量CuC12、FeC12和FeC13,任意排放将导致环境污染及资源的浪费.可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用.测得某废腐蚀液中含CuCl2 1.5mol/L、FeCl2 3.0mol/L、FeCl3 1.0mol/L、HCl 3.0mol/L.取废腐蚀液200mL按如下流程在实验室进行实验:
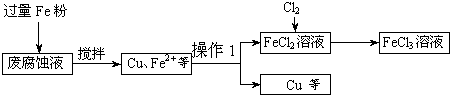
回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂质所需试剂是______(填化学式).
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物.反应的化学方程式为______.
(3)如图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置.
从图中挑选所需的仪器,完成上述装置简图(添加必要的塞子、玻璃导管、胶皮管.固定装置不用画),并标明容器中所装试剂.
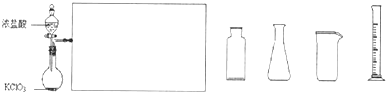
(4)实验中,必需控制氯气的速度,使导管口逸出的气泡每秒1~2个,以便被FeCl2溶液完全吸收.控制生成氯气速率的操作是:______.
(5)按上述流程操作,需称取Fe粉的质量应不少于______g(精确到0.1g),需通入Cl2的物质的量不少于______mol,加入烧瓶中的KClO3的质量应不少于______g(精确到0.1g).
查看习题详情和答案>>
(A)针对以下A~D四个涉及H2O2的反应(未配平),填写空白:
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O2→Ag+O2+H2O
C.H2O2→H2O+O2
D. H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(1)H2O2仅体现氧化性的反应是(填代号)
(2)H2O2既体现氧化性又体现还原性的反应是(填代号)
(3)H2O2体现弱酸性的反应是(填代号)
(B)某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置.

请回答下列问题:
(1)装置F中发生反应的离子方程式为
(2)装置A的烧瓶中可装试剂
(3)B装置的名称是
(4)通入C装置的两根导管左边较长、右边较短,目的是
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.请写出反应的化学方程式:
查看习题详情和答案>>
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O2→Ag+O2+H2O
C.H2O2→H2O+O2
D. H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(1)H2O2仅体现氧化性的反应是(填代号)
D
D
,该反应配平的化学方程式为3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
.(2)H2O2既体现氧化性又体现还原性的反应是(填代号)
C
C
.(3)H2O2体现弱酸性的反应是(填代号)
A
A
,其理由为这一反应可看作是强酸制取弱酸的反应
这一反应可看作是强酸制取弱酸的反应
.(B)某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置.

请回答下列问题:
(1)装置F中发生反应的离子方程式为
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
.
| ||
(2)装置A的烧瓶中可装试剂
生石灰或固体氢氧化钠
生石灰或固体氢氧化钠
.(3)B装置的名称是
球形干燥管
球形干燥管
;E装置的作用除去氯气中的HCl
除去氯气中的HCl
.(4)通入C装置的两根导管左边较长、右边较短,目的是
使密度大的氯气与密度小的氨气较快地均匀混合
使密度大的氯气与密度小的氨气较快地均匀混合
.(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.请写出反应的化学方程式:
3Cl2+8NH3═N2+6NH4Cl
3Cl2+8NH3═N2+6NH4Cl
. 海水占地球总蓄水量的97.2%,若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源.
海水占地球总蓄水量的97.2%,若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源.