题目内容
Ⅰ.(1)在饱和Na2CO3溶液中通入足量的CO2气体,会有晶体析出,此晶体是_______________。析出晶体的原因有:①_______________,②_______________,③_______________。(2)向Na2CO3溶液中逐滴滴入稀盐酸,溶液中的![]() 浓度的变化情况是_______。
浓度的变化情况是_______。
A.逐渐增大 B.逐渐变小
C.先逐渐增大而后减小 D.先逐渐减小后变大
试用离子方程式和简要文字说明理由______________________________。
Ⅱ.已知下列4个反应:
①2Na+2H2O====2NaOH+H2↑
②2F2+2H2O====4HF+O2
③Cl2+H2O====HCl+HClO
④C+H2O![]() CO+H2
CO+H2
试从氧化还原反应的角度,完成下列问题:
(1)水只作氧化剂的是________(填数码代号,下同)。
(2)水只作还原剂的是________。
(3)水既不作氧化剂,又不作还原剂的是________。
Ⅰ.(1)NaHCO3 ①NaHCO3的溶解度比Na2CO3小 ②因为水参加反应,溶剂减少?③因为Na2CO3与H2O、CO2化合成NaHCO3,溶质质量增大
(2)C 向Na2CO3中逐滴加入HCl,先发生反应:![]() +H+====
+H+====![]() ,使
,使![]() 浓度逐渐增大,后发生
浓度逐渐增大,后发生![]() +H+====H2O+CO2↑,导致
+H+====H2O+CO2↑,导致![]() 浓度逐渐减少
浓度逐渐减少
Ⅱ.(1)①④ (2)② (3)③

练习册系列答案
相关题目
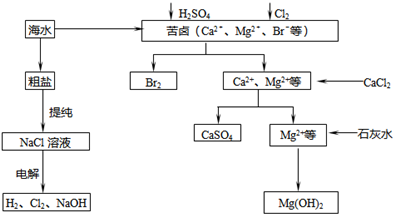 工业上对海水资源综合开发利用的部分工艺流程如图所示.
工业上对海水资源综合开发利用的部分工艺流程如图所示.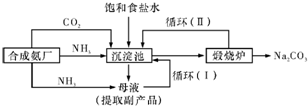 (2011?湖南二模)[化学一选修化学与技术]
(2011?湖南二模)[化学一选修化学与技术]