网址:http://m.1010jiajiao.com/timu3_id_303871[举报]
25℃时,在0.01mol·L-1的硫酸溶液中,水电离出的c(H+)是( )
A.5×10-13mol·L-1 B.0.02mol·L-1 C.1×10-7mol·L-1 D.1×10-12mol·L-1
查看习题详情和答案>>
25℃时,在0.01mol·L-1的硫酸溶液中,水电离出的c(H+)是( )
A.5×10-13mol·L-1 B.0.02mol·L-1 C.1×10-7mol·L-1 D.1×10-12mol·L-1
查看习题详情和答案>>25℃时,在0.01mol·L-1的硫酸溶液中,水电离出的c(H+)是( )
A.5×10-13mol·L-1 B.0.02mol·L-1 C.1×10-7mol·L-1 D.1×10-12mol·L-1
查看习题详情和答案>>
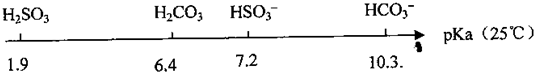
(1)比较H2SO3的Ka1和HSO3-的Ka2,Ka1
(2)0.01mol.L-1NaHSO3溶液的pH=bl,0.01mol?L-1NaHCO3溶液的pH=b2,b1
(3)向10mL 0.01mol?L-1的H2SO3溶液中,滴加0.0l mol?L-1KOH溶液V(mL),
①当V=10mL时,溶液中存在:c(K+)>c(HSO3-)>c(SO32-)>c(H2SO3),则c(H+)
②当V=a mL时,溶液中离子浓度有如下关系:c(K+)=2c(SO32-)+c(HSO3-);当V=b mL时,溶液中离子浓度有如下关系:
c(K+)=c(SO32-)+c(HSO3-)+c(H2SO3);则a
(4)已知25℃时,Ksp(BaSO4)=1×10-10,将0.1gBaSO4沉淀,分别用100mL蒸馏水和100mL 0.01mol?L-1H2SO4溶液洗涤,两种洗涤方法中BaSO4沉淀的损耗量之比为
(11分)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:
2IO3-+5SO32- +2H+ = I2+5SO42-+H2O
生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:[来源:学&科&网]
|
|
0.01mol·L-1KIO3酸性溶液(含淀粉)的体积/mL |
0.01mol·L-1 Na2SO3溶液的体积/mL |
H2O的体积/mL |
实验温度 /℃ |
溶液出现蓝色时所需时间/s |
|
实验1 |
5 |
V1 |
35 |
25 |
t 1 |
|
实验2 |
5 |
5 |
40 |
25 |
t 2 |
|
实验3 |
5 |
5 |
V2 |
0 |
t 3[来源:] |
(1) 碘酸钾与亚硫酸钠的反应是 ___________________(填反应类型);
(2)该实验的目的是①____________________________________________,
②_____________________________________________________________;
(3)表中V2=___________mL, V1=___________mL
(4)t1_______ t2_________t3(填“<”、“>”或“=”)
查看习题详情和答案>>