题目内容
饱和亚硫酸溶液的pKa(电离平衡常数的负对数,即pKa=-lgKa)数据如下:
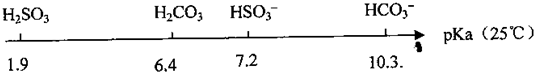
(1)比较H2SO3的Ka1和HSO3-的Ka2,Ka1
(2)0.01mol.L-1NaHSO3溶液的pH=bl,0.01mol?L-1NaHCO3溶液的pH=b2,b1
(3)向10mL 0.01mol?L-1的H2SO3溶液中,滴加0.0l mol?L-1KOH溶液V(mL),
①当V=10mL时,溶液中存在:c(K+)>c(HSO3-)>c(SO32-)>c(H2SO3),则c(H+)
②当V=a mL时,溶液中离子浓度有如下关系:c(K+)=2c(SO32-)+c(HSO3-);当V=b mL时,溶液中离子浓度有如下关系:
c(K+)=c(SO32-)+c(HSO3-)+c(H2SO3);则a
(4)已知25℃时,Ksp(BaSO4)=1×10-10,将0.1gBaSO4沉淀,分别用100mL蒸馏水和100mL 0.01mol?L-1H2SO4溶液洗涤,两种洗涤方法中BaSO4沉淀的损耗量之比为
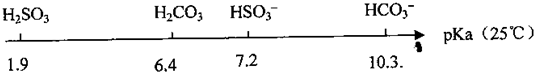
(1)比较H2SO3的Ka1和HSO3-的Ka2,Ka1
>
>
Ka2(填‘‘>”、“<’’或“=”,下同)(2)0.01mol.L-1NaHSO3溶液的pH=bl,0.01mol?L-1NaHCO3溶液的pH=b2,b1
<
<
b2(3)向10mL 0.01mol?L-1的H2SO3溶液中,滴加0.0l mol?L-1KOH溶液V(mL),
①当V=10mL时,溶液中存在:c(K+)>c(HSO3-)>c(SO32-)>c(H2SO3),则c(H+)
>
>
c(OH-)②当V=a mL时,溶液中离子浓度有如下关系:c(K+)=2c(SO32-)+c(HSO3-);当V=b mL时,溶液中离子浓度有如下关系:
c(K+)=c(SO32-)+c(HSO3-)+c(H2SO3);则a
>
>
b.(4)已知25℃时,Ksp(BaSO4)=1×10-10,将0.1gBaSO4沉淀,分别用100mL蒸馏水和100mL 0.01mol?L-1H2SO4溶液洗涤,两种洗涤方法中BaSO4沉淀的损耗量之比为
1000
1000
.分析:(1)根据pKa为电离平衡常数的负对数,即pKa=-lgKa,则pKa越小,电离平衡常数Ka越大;
(2)根据pKa越小,电离平衡常数Ka越大,则对应酸的酸性就强,利用酸越弱则强碱弱酸盐的水解程度越大来分析;
(3)①V=10mL,溶液中的溶质为NaHSO3,由c(HSO3-)>c(SO32-)>c(H2SO3),可知HSO3-的电离大于其水解来分析;
②V=a mL时由c(K+)=2c(SO32-)+c(HSO3-),则c(H+)=c(OH-);V=b mL时,c(K+)=c(SO32-)+c(HSO3-)+c(H2SO3),即溶液中的溶质为KHSO3,溶液显酸性;
(4)利用离子对溶解平衡的影响及Ksp(BaSO4)来计算溶解的硫酸钡的质量,然后确定两种洗涤方法中BaSO4沉淀的损耗量之比.
(2)根据pKa越小,电离平衡常数Ka越大,则对应酸的酸性就强,利用酸越弱则强碱弱酸盐的水解程度越大来分析;
(3)①V=10mL,溶液中的溶质为NaHSO3,由c(HSO3-)>c(SO32-)>c(H2SO3),可知HSO3-的电离大于其水解来分析;
②V=a mL时由c(K+)=2c(SO32-)+c(HSO3-),则c(H+)=c(OH-);V=b mL时,c(K+)=c(SO32-)+c(HSO3-)+c(H2SO3),即溶液中的溶质为KHSO3,溶液显酸性;
(4)利用离子对溶解平衡的影响及Ksp(BaSO4)来计算溶解的硫酸钡的质量,然后确定两种洗涤方法中BaSO4沉淀的损耗量之比.
解答:解:(1)由pKa数据可知,1.9<7.2,由pKa=-lgKa,则pKa越小,电离平衡常数Ka越大,则H2SO3的Ka1>HSO3-的Ka2,
故答案为:>;
(2)由pKa数据可知,亚硫酸的pKa小于碳酸,则酸性比碳酸的强,相同浓度的NaHSO3溶液比NaHCO3溶液中酸根离子的水解程度弱,则NaHSO3溶液的pH小,即bl<b2,故答案为:<;
(3)①V=10mL,溶液中的溶质为NaHSO3,由c(HSO3-)>c(SO32-)>c(H2SO3),可知HSO3-的电离大于其水解,电离生成氢离子,水解生成氢氧根离子,即c(H+)>c(OH-),故答案为:>;
②V=b mL时,c(K+)=c(SO32-)+c(HSO3-)+c(H2SO3),即溶液中的溶质为KHSO3,溶液显酸性;当V=a mL时,溶液中离子浓度有如下关系:c(K+)=2c(SO32-)+c(HSO3-),由电荷守恒可知c(H+)=c(OH-),即溶液显中性,则向10mL0.01mol?L-1的H2SO3溶液中,滴加0.0l mol?L-1KOH溶液,由酸性变为中性时碱的体积在变大,即a>b,故答案为:>;
(4)用100mL蒸馏水洗涤沉淀时,溶解的BaSO4的物质的量为0.1L×c(Ba2+)=0.1L×
=0.1L×
mol/L=10-6mol,
用100mL 0.01mol?L-1H2SO4溶液洗涤时,硫酸根离子抑制了沉淀的溶解,则溶解的BaSO4的物质的量为0.1L×c(Ba2+)=0.1L×
=0.1L×
mol/L=10-9mol,
由同种物质的质量之比等于物质的量之比,则两种洗涤方法中BaSO4沉淀的损耗量之比为
=1000,故答案为:1000.
故答案为:>;
(2)由pKa数据可知,亚硫酸的pKa小于碳酸,则酸性比碳酸的强,相同浓度的NaHSO3溶液比NaHCO3溶液中酸根离子的水解程度弱,则NaHSO3溶液的pH小,即bl<b2,故答案为:<;
(3)①V=10mL,溶液中的溶质为NaHSO3,由c(HSO3-)>c(SO32-)>c(H2SO3),可知HSO3-的电离大于其水解,电离生成氢离子,水解生成氢氧根离子,即c(H+)>c(OH-),故答案为:>;
②V=b mL时,c(K+)=c(SO32-)+c(HSO3-)+c(H2SO3),即溶液中的溶质为KHSO3,溶液显酸性;当V=a mL时,溶液中离子浓度有如下关系:c(K+)=2c(SO32-)+c(HSO3-),由电荷守恒可知c(H+)=c(OH-),即溶液显中性,则向10mL0.01mol?L-1的H2SO3溶液中,滴加0.0l mol?L-1KOH溶液,由酸性变为中性时碱的体积在变大,即a>b,故答案为:>;
(4)用100mL蒸馏水洗涤沉淀时,溶解的BaSO4的物质的量为0.1L×c(Ba2+)=0.1L×
| Ksp(BaSO4) |
| 1×10-10 |
用100mL 0.01mol?L-1H2SO4溶液洗涤时,硫酸根离子抑制了沉淀的溶解,则溶解的BaSO4的物质的量为0.1L×c(Ba2+)=0.1L×
|
|
由同种物质的质量之比等于物质的量之比,则两种洗涤方法中BaSO4沉淀的损耗量之比为
| 10-6mol |
| 10-9mol |
点评:本题考查溶液中的电离及离子的浓度关系,考查知识点为高考的热点,学生应学会利用信息中的数据来分析是解答本题的关键,然后注重结合所学知识来解答即可.

练习册系列答案
相关题目



