摘要:在2升密闭容器内加入4molA和6molB.发生如下反应: 4A+5D(g)经5s后剩下A2.5mol.则用B表示的该反应速率为( ) A.0.1mol/L·s B.0.225mol/L·s C.0.15mol/L·s D.0.9mol/L·s
网址:http://m.1010jiajiao.com/timu3_id_290365[举报]
在一定温度下,向一容积为2L升的恒容密闭容器内加入0.2mol的N2和0.6mol的H2,发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0.反应中NH3的物质的量浓度的变化的情况如图所示:
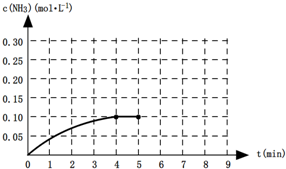
(1)根据上图,计算从反应开始到平衡时,平均反应速率v(NH3)= .
(2)反应达到平衡后,第5分钟时,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为 (选填字母编号).
a.0.20mol?L-1 b.0.16mol?L-1 c.0.10mol?L-1 d.0.05mol?L-1
(3)该反应的化学平衡常数表达式为 .反应达到平衡后,第5分钟时,若保持其它条件不变,只把容器的体积缩小一半,平衡 移动(选填“正向”、“逆向”或“不”),化学平衡常数K (选填“增大”、“减小”或“不变”).
(4)第5分钟时把容器的体积缩小一半后,若在第8分钟达到新的平衡(此时NH3的浓度约为0.25mol?L-1),请在图中画出从第5分钟开始变化直至到达新平衡时NH3浓度的变化曲线.
(5)常温下,向0.001mol?L-1的AlCl3 溶液中通入NH3直至过量,现象 ,当pH= 时,开始生成沉淀(已知:Ksp[Al(OH)3]=1.0×10-33).
查看习题详情和答案>>

(1)根据上图,计算从反应开始到平衡时,平均反应速率v(NH3)=
(2)反应达到平衡后,第5分钟时,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
a.0.20mol?L-1 b.0.16mol?L-1 c.0.10mol?L-1 d.0.05mol?L-1
(3)该反应的化学平衡常数表达式为
(4)第5分钟时把容器的体积缩小一半后,若在第8分钟达到新的平衡(此时NH3的浓度约为0.25mol?L-1),请在图中画出从第5分钟开始变化直至到达新平衡时NH3浓度的变化曲线.
(5)常温下,向0.001mol?L-1的AlCl3 溶液中通入NH3直至过量,现象
 在一容积为2升的密闭容器内加入0.2mol的N2和0.6mol 的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)+Q(Q>0).反应中NH3的物质的量浓度的变化的情况如右图:
在一容积为2升的密闭容器内加入0.2mol的N2和0.6mol 的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)+Q(Q>0).反应中NH3的物质的量浓度的变化的情况如右图:(1)根据右图,计算从反应开始到平衡时,平均反应速率v(NH3)为
(2)该反应的化学平衡常数表达式为
(3)反应达到平衡后,第5分钟时,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
A、0.20mol/L B、0.16mol/L C、0.10mol/L D、0.05mol/L
(4)反应达到平衡后,第5分钟时,保持其它条件不变,若只把容器的体积缩小一半,平衡
(5)第5分钟把容器的体积缩小一半后,若在第8分钟达到新的平衡(此时NH3的浓度约为0.25mol/L),请在上图中画出第5分钟到此平衡时NH3浓度的变化曲线.
T °C时,在2 L密闭容器中,X、Y、Z三种气体的物质的量随时间变化如下图I所示。若起始时加入一定量的Y,在不同温度下改变X的量时Z的体积分数变化情况如图II所示。则下列结论正确的是
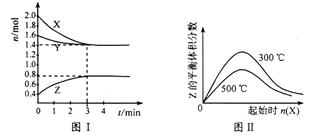
A.该反应的化学方程式为: 2X(g) + Y(g) 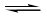 2Z(g)
2Z(g)
B.反应进行的前3min内,用X表示的平均反应速率v(x)=0.067mol/(L·min)
C.由图II可知,其他条件不变,增大X的量时Y的转化率先增大后减小
D.其他条件不变,升髙温度,平衡逆向移动
查看习题详情和答案>>
在一定温度下,向一容积为2L升的恒容密闭容器内加入0.2 mol的N2和0.6 mol 的H2,发生如下反应:N2(g)+ 3H2(g) 2NH3(g) △H<0。反应中NH3的物质的量浓度的变化的情况如下图所示:
2NH3(g) △H<0。反应中NH3的物质的量浓度的变化的情况如下图所示:
 2NH3(g) △H<0。反应中NH3的物质的量浓度的变化的情况如下图所示:
2NH3(g) △H<0。反应中NH3的物质的量浓度的变化的情况如下图所示: 
(1)根据上图,计算从反应开始到平衡时,平均反应速率v(NH3)= _________。
(2)反应达到平衡后,第5分钟时,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为______ (选填字母编号)。
a.0.20 mol/L b.0.16 mol/L c.0.10 mol/L d.0.05 mol/L
(3)该反应的化学平衡常数表达式为___________________。反应达到平衡后,第5分钟时,若保持其它条件不变,只把容器的体积缩小一半,平衡______移动(选 填“正向”、“逆向”或“不”),化学平衡常数K________(选填“增大”、“减小”或“不变”)。
(4)第5分钟时把容器的体积缩小一半后,若在第8分钟达到新的平衡(此时NH3的浓度约为0.25 mol/L),请在上图中画出从第5分钟开始变化直至到达新平衡时NH3浓度的变化曲线。
(5) 常温下,向0.001 mol/L的AlCl3溶液中通入NH3直至过量,现象____________,当pH=________时,开始生成沉淀(已知:Ksp[Al(OH)3]= 1.0×10-33)。
查看习题详情和答案>>
(2)反应达到平衡后,第5分钟时,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为______ (选填字母编号)。
a.0.20 mol/L b.0.16 mol/L c.0.10 mol/L d.0.05 mol/L
(3)该反应的化学平衡常数表达式为___________________。反应达到平衡后,第5分钟时,若保持其它条件不变,只把容器的体积缩小一半,平衡______移动(选 填“正向”、“逆向”或“不”),化学平衡常数K________(选填“增大”、“减小”或“不变”)。
(4)第5分钟时把容器的体积缩小一半后,若在第8分钟达到新的平衡(此时NH3的浓度约为0.25 mol/L),请在上图中画出从第5分钟开始变化直至到达新平衡时NH3浓度的变化曲线。
(5) 常温下,向0.001 mol/L的AlCl3溶液中通入NH3直至过量,现象____________,当pH=________时,开始生成沉淀(已知:Ksp[Al(OH)3]= 1.0×10-33)。
T °C时,在2 L密闭容器中,X、Y、Z三种气体的物质的量随时间变化如下图I所示。若起始时加入一定量的Y,在不同温度下改变X的量时Z的体积分数变化情况如图II所示。则下列结论正确的是
A.该反应的化学方程式为: 2X(g) + Y(g)  2Z(g) 2Z(g) |
| B.反应进行的前3min内,用X表示的平均反应速率v(x)=0.067mol/(L·min) |
| C.由图II可知,其他条件不变,增大X的量时Y的转化率先增大后减小 |
| D.其他条件不变,升髙温度,平衡逆向移动 |