摘要:下表是周期表的一部分,试回答下列问题: (1)写出下列元素的符号:① .⑥ .⑦ .⑩ (2)这些元素中.第一电离能最小的元素是 .电负性最大的元素是 . (3)在这些元素的最高价氧化物对应水化物中.酸性最强的是 .碱性最强的是 .呈两性的氢氧化物是 .写出三者之间相互反应的离子方程式: ; . . (4)在这些元素中.原子半径最小的是 .原子半径最大的是 . (5)在③与④中.化学性质较活泼的是 .怎样用化学实验证明?
网址:http://m.1010jiajiao.com/timu3_id_286889[举报]
下表是周期表的一部分,试回答下列问题:

(1)写出下列元素的符号:① ,⑥ ,⑦ ,⑩
(2)这些元素中,第一电离能最小的元素是 (填序号,下同),电负性最大的元素是 。
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 ,写出三者之间相互反应的离子方程式: ;
.
(4)在这些元素中,原子半径最小的是 (填元素符号,下同),原子半径最大的是 。
(5)在③与④中,化学性质较活泼的是 。怎样用化学实验证明?
查看习题详情和答案>>下表为周期表的一部分,其中的字母代表对应的元素
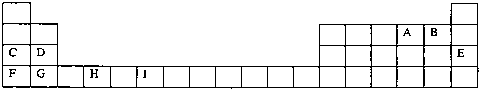
请回答下列问题:
(1)写出元素I的基态原子的价电子排布式 ;已知M2+离子3d轨道中有6个电子,试推出M元素位于周期表的 周期 族.
(2)请列举F的金属性比C强的实验事实: ,并用原子结构理论解释其原因: .
(3)在标准状况下,根据M=
测定B的气态氢化物的相对分子质量,结果发现,测定结果总比理论值高,其原因是 .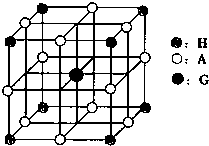
(4)H、A、G三种元素形成的晶体是一种矿物的主要成分,其晶胞结构如图,则该晶体的化学式为 ;在该晶体中,G离子的配位数为 ;若晶胞的边长为acm,则晶体的密度为 g/cm3.
查看习题详情和答案>>

请回答下列问题:
(1)写出元素I的基态原子的价电子排布式
(2)请列举F的金属性比C强的实验事实:
(3)在标准状况下,根据M=
| m | n |

(4)H、A、G三种元素形成的晶体是一种矿物的主要成分,其晶胞结构如图,则该晶体的化学式为
下图是周期表的一部分,试回答下列问题:
(1)元素②有两种原子10X和9X,下列说法正确的是______
a.是同一种核素 b.具有相同的中子数
c.几乎具有相同的化学性质 d.具有相同的物理性质
①与⑦具有相似的化学性质,写出①的氯化物水解反应的化学方程式______.
(2)⑩和(11)两元素形成的某化合物可作为干燥剂,试写出其电子式______.
(3)③④⑤⑥四种元素氢化物的沸点由低到高排列为______(用元素符号表示).
(4)元素⑨X的单质和元素④Y的最高价氧化物的水化物反应的还原产物为YO和YO2,且YO和YO2的物质的量之比为1:1,写出该反应的化学方程式______.
(5)⑧号元素M形成的盐K2MO4是一种强氧化剂,可作为水处理剂和高容量电池的材料.与MnO2-Zn电池相似,K2MO4-Zn也可以组成碱性电池,其正极反应式为______总反应的离子反应式为______.
查看习题详情和答案>>
| ① | ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||||
| ⑦ | ⑩ | |||||||||||||||||||
| ⑾ | ⑧ | ⑨ | ||||||||||||||||||
a.是同一种核素 b.具有相同的中子数
c.几乎具有相同的化学性质 d.具有相同的物理性质
①与⑦具有相似的化学性质,写出①的氯化物水解反应的化学方程式______.
(2)⑩和(11)两元素形成的某化合物可作为干燥剂,试写出其电子式______.
(3)③④⑤⑥四种元素氢化物的沸点由低到高排列为______(用元素符号表示).
(4)元素⑨X的单质和元素④Y的最高价氧化物的水化物反应的还原产物为YO和YO2,且YO和YO2的物质的量之比为1:1,写出该反应的化学方程式______.
(5)⑧号元素M形成的盐K2MO4是一种强氧化剂,可作为水处理剂和高容量电池的材料.与MnO2-Zn电池相似,K2MO4-Zn也可以组成碱性电池,其正极反应式为______总反应的离子反应式为______.
查看习题详情和答案>>
 下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.| a | b | ||||||||||||||||
| c | d | e | |||||||||||||||
| f | g | ||||||||||||||||
(1)a的氢化物的分子构型为
三角锥形
三角锥形
,中心原子的杂化形式为sp3
sp3
;d在空气中燃烧产物的分子构型为V形
V形
,中心原子的杂化形式为sp2
sp2
,该分子是极性
极性
(填“极性”或“非极性”)分子.(2)b、d、e三种元素的氢化物中的沸点最高的是
HF
HF
,原因是:HF分子间形成氢键,HCl、H2S分子间没有氢键
HF分子间形成氢键,HCl、H2S分子间没有氢键
.(3)将g的无水硫酸盐溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子.此配合离子空间构型为
平面正方形
平面正方形
,请写出生成此配合离子的离子方程式:Cu2++4H2O=[Cu(H2O)4]2+
Cu2++4H2O=[Cu(H2O)4]2+
.(4)f(NH3)5BrSO4可形成两种配合物,已知f3+的配位数是6,为确定f的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2 溶液时,产生白色沉淀,在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,第二种配合物的化学式为
[Co(NH3)5SO4]Br
[Co(NH3)5SO4]Br
,该配合物的配体是NH3
NH3
、SO42-
SO42-
;(5)c单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.
c单质晶体中原子的配位数为
12
12
.若已知c的原子半径为r,NA代表阿伏加德罗常数,c的相对原子质量为M.该晶体的密度为| M | ||
4
|
| M | ||
4
|
下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
试回答下列问题:
(1)请写出元素m的基态原子电子排布式
(2)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表
(3)由a原子跟f原子以1:1相互交替结合而形成的晶体,晶型与晶体f相同.两者相比熔点更高的是
(4)b、n、m元素化合物的晶体中的晶胞堆积方式如图2所示:
请回答:该化合物的化学式是:
查看习题详情和答案>>
| a | b | ||||||||||||||||
| c | d | e | f | i | j | k | l | ||||||||||
| n | m | ||||||||||||||||
(1)请写出元素m的基态原子电子排布式
1s22s22p63s23p63d24s2
1s22s22p63s23p63d24s2
.(2)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表
Si
Si
(填元素符号);其中电负性最大的是2
2
(填图1中的序号).(3)由a原子跟f原子以1:1相互交替结合而形成的晶体,晶型与晶体f相同.两者相比熔点更高的是
SiC
SiC
(填化学式).(4)b、n、m元素化合物的晶体中的晶胞堆积方式如图2所示:

请回答:该化合物的化学式是:
CaTiO3
CaTiO3
(用元素符号表示),与m原子距离相等且最接近的m原子数为6
6
.